Clear Sky Science · it
Meccanismi strutturali e funzionali alla base della dinamica del cancello di attivazione e dell'accessibilità del motivo IFM in Nav1.5 umano
Perché contano quei piccoli cancelli del cuore
Il battito elettrico di ogni battito cardiaco dipende da cancelli microscopici nelle cellule del cuore che si aprono brevemente per permettere il rapido ingresso di ioni sodio. Questi cancelli sono proteine chiamate canali del sodio e, quando funzionano in modo anomalo, possono provocare pericolosi disturbi del ritmo cardiaco. Questo studio si concentra sul principale canale del sodio cardiaco, noto come Nav1.5, e rivela uno stato intermedio del suo cancello finora inesplorato, oltre a una tasca ionica nascosta accanto a un “fermaglio” chiave che spegne il canale. Comprendere questa macchina a questo livello di dettaglio potrebbe orientare farmaci migliori per le aritmie, con azione più precisa e meno effetti collaterali.
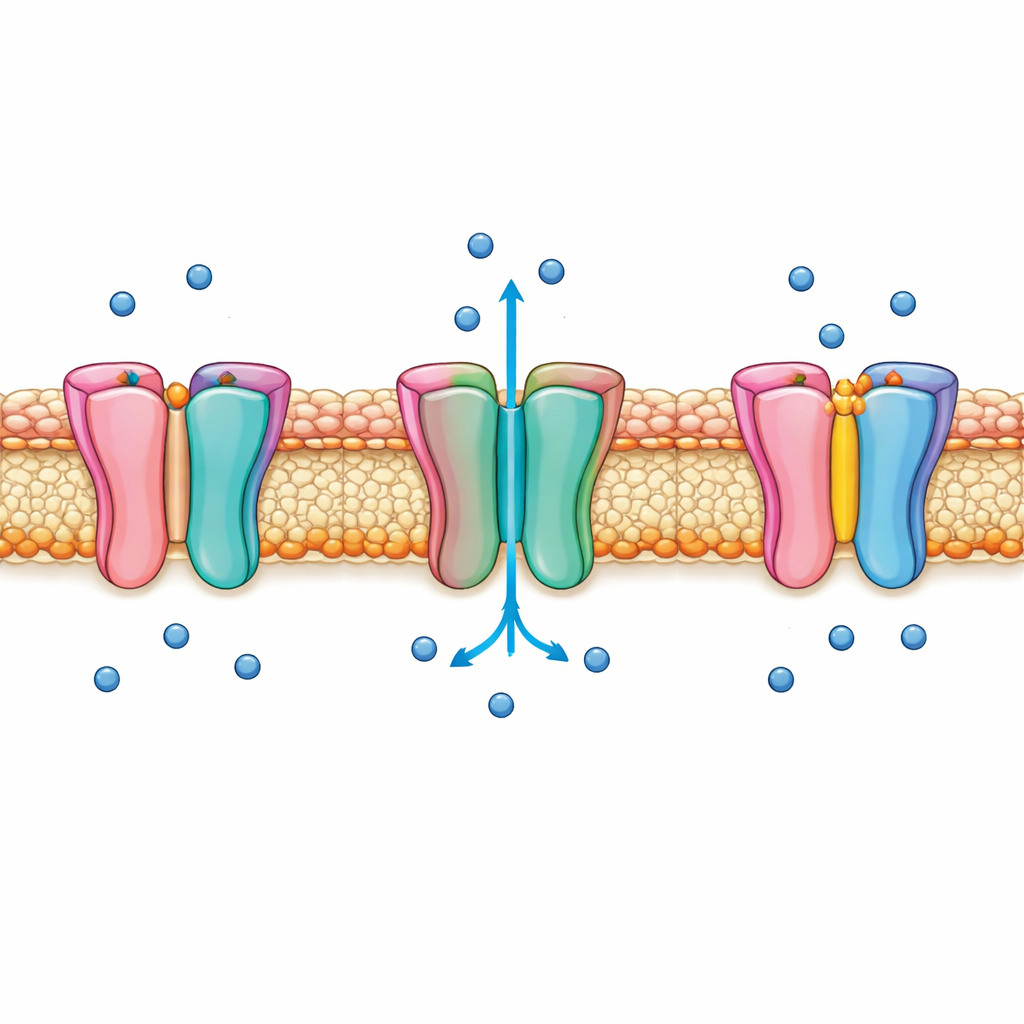
Uno sguardo più vicino alla porta del sodio cardiaco
Nav1.5 è inserito nella membrana della cellula cardiaca e si apre per solo pochi millesimi di secondo per generare il rapido aumento del segnale elettrico che innesca la contrazione. Quasi immediatamente, si spegne da solo in un processo chiamato inattivazione rapida, evitando un ingresso eccessivo di sodio. Per decenni, un segmento di tre amminoacidi, soprannominato motivo IFM, è stato considerato come un tappo che si infila per fermare il flusso. Tuttavia molti dettagli su come si muove il cancello principale alla base del canale, e su come il motivo IFM controlli realmente questo movimento, sono rimasti poco chiari. Queste lacune hanno limitato gli sforzi per progettare medicinali che prendano di mira il canale senza perturbare il suo timing finemente sintonizzato.
Catturare uno stato aperto intermedio
Utilizzando la crio‑microscopia elettronica ad alta risoluzione, gli autori hanno catturato il canale Nav1.5 umano a lunghezza intera in quello che chiamano uno stato aperto intermedio. In questa configurazione, le quattro eliche interne che formano il cancello di attivazione sono separate quanto basta per permettere il passaggio di ioni sodio idratati, ma non tanto quanto nelle strutture completamente aperte descritte in precedenza. Simulazioni molecolari sotto tensione applicata hanno mostrato che acqua e ioni sodio possono attraversare il poro, sebbene solo a voltaggi più elevati rispetto a un canale pienamente aperto, confermando che questo stato conduce ma si colloca tra le forme usuali aperta e inattivata. Una molecola detergente incastrata al cancello contribuisce a mantenere questo delicato assetto, illustrando come piccole variazioni di forma possano sintonizzare finemente se il canale lascia passare ioni o resta chiuso.
Come i contatti laterali aiutano a controllare il cancello
Il gruppo ha inoltre risolto una superficie di interazione tra il dominio N‑terminale del canale, che penzola all’interno della cellula, e una delle eliche che formano il cancello nota come S6 nel dominio I. Specifici amminoacidi carichi in queste regioni formano ponti salini che agiscono come piccoli fermi, aiutando a stabilizzare il cancello aperto. Quando i ricercatori hanno modificato questi residui, la forma complessiva delle correnti elettriche è cambiata: in particolare, alcune mutazioni hanno rallentato la velocità con cui il canale si spegneva dopo l’apertura. Ulteriori analisi hanno rivelato che l’elica S6 può oscillare verso l’interno e verso l’esterno, restringendo o allargando il cancello. Differenti schemi di contatto con il dominio N‑terminale corrispondevano a questi spostamenti, collegando il moto microscopico di una singola elica alla capacità del canale di passare da forme aperte a forme più chiuse, simili all’inattivazione.
Una tasca nascosta accanto al fermaglio dell’inattivazione
Forse la scoperta più sorprendente si trova accanto al motivo IFM stesso. Nella struttura aperta intermedia, il segmento IFM conserva la sua caratteristica posa a U ben incastrata in una tasca idrofobica, invece di allontanarsi completamente come propongono alcuni modelli. Accanto a essa, tuttavia, gli autori hanno identificato una seconda tasca rivestita da residui carichi negativamente che trattiene un ione sodio. Simulazioni ed esperimenti suggeriscono che anche altri ioni positivi possano occupare questa nicchia. Mutazioni che cambiavano la carica o la chimica della tasca hanno alterato la facilità con cui il canale si inattivava e il comportamento del motivo IFM, indicando che il legame ionico qui allenta o stringe il fermaglio IFM senza richiedere che esso lasci completamente la sua culla. Questa reinterpretazione aiuta a spiegare esperimenti passati in cui ioni reattivi potevano marcare cisteine ingegnerizzate vicino al motivo IFM anche se il motivo sembrava rimanere sepolto.

Che cosa significa per il ritmo cardiaco e per i farmaci futuri
Congiuntamente, questi risultati aggiornano l’iconica immagine a “porta e cuneo” dell’inattivazione dei canali del sodio. Piuttosto che un semplice tappo che viene inserito e rimosso, Nav1.5 sembra usare una danza coordinata: un cancello che può trovarsi in una posizione aperta intermedia, contatti laterali che stabilizzano o rilassano questa configurazione e una tasca vicina sintonizzata dagli ioni che regola quanto saldamente il motivo IFM tiene chiuso il cancello. Rivelando questo percorso ionico alternativo e il suo impatto sulla gating, il lavoro offre una mappa strutturale più raffinata di come i canali del sodio cardiaci falliscano nelle malattie e indica nuovi bersagli più selettivi per terapie antiaritmiche.
Citazione: Biswas, R., López-Serrano, A.L., Purohit, A. et al. Structural and functional mechanisms underlying activation gate dynamics and IFM motif accessibility in human Nav1.5. Nat Commun 17, 2820 (2026). https://doi.org/10.1038/s41467-026-69672-x
Parole chiave: canale del sodio cardiaco, Nav1.5, inattivazione rapida, crio‑EM, aritmia cardiaca