Clear Sky Science · nl
Structurele en functionele mechanismen die de dynamiek van het activatiepoortje en de toegankelijkheid van het IFM-motief in humane Nav1.5 onderbouwen
Waarom kleine hartpoortjes ertoe doen
Het elektrische ritme van elk hartslagje hangt af van microscopische poortjes in hartcellen die even opengaan zodat natriumionen naar binnen kunnen stromen. Deze poortjes zijn eiwitten die natriumkanalen worden genoemd, en als ze niet goed werken kan dat leiden tot gevaarlijke ritmestoornissen. Deze studie richt zich op het belangrijkste cardiale natriumkanaal, bekend als Nav1.5, en onthult een eerder onzichtbare tussentoestand van zijn poort, plus een verborgen ionenholte naast een sleutel-"sluiting" die het kanaal uitschakelt. Het begrijpen van dit mechanisme in zulke detail kan helpen bij het ontwikkelen van betere geneesmiddelen tegen aritmieën die preciezer werken en minder bijwerkingen hebben.
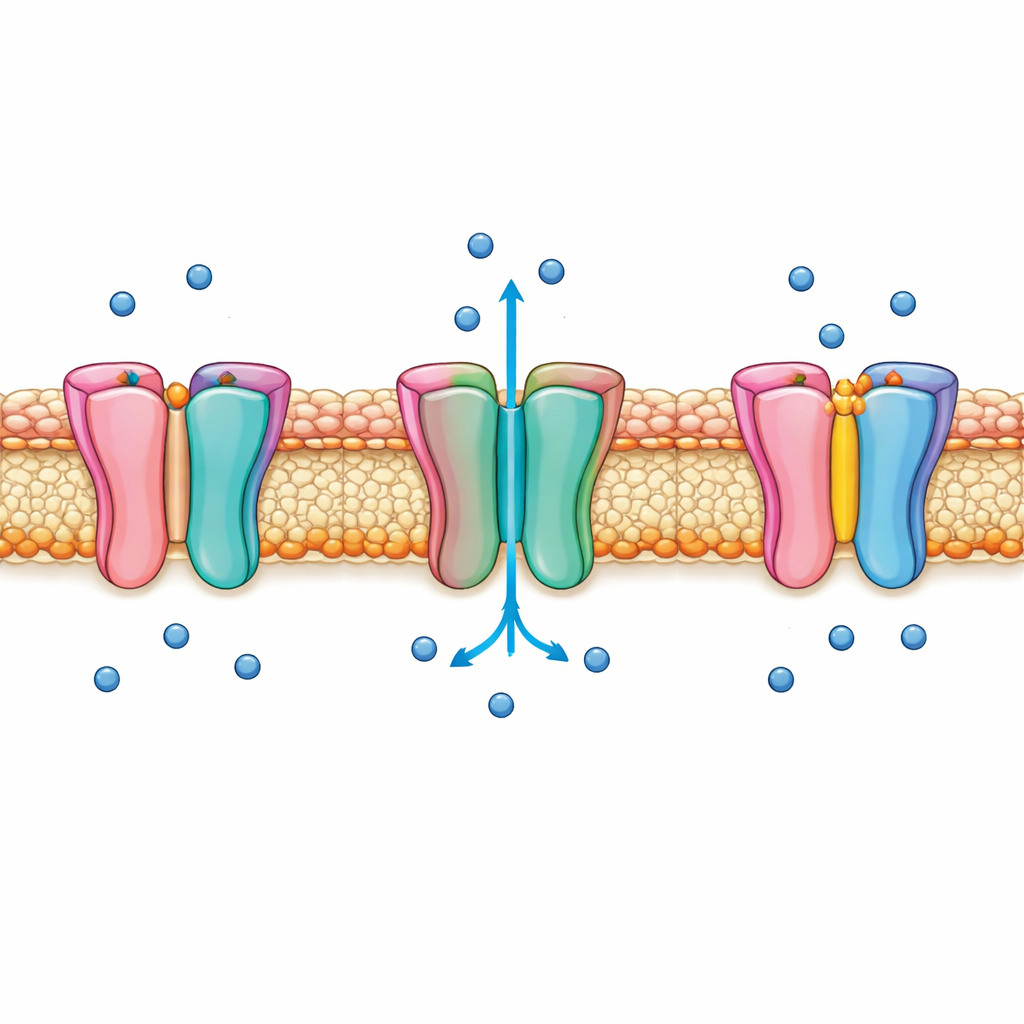
Een nadere blik op de natriumdeur van het hart
Nav1.5 zit in het membraan van hartcellen en opent maar een paar duizendtallen van een seconde om de scherpe stijging van het elektrische signaal te genereren die de contractie op gang brengt. Vrij snel schakelt het zichzelf uit via een proces dat snelle inactivatie wordt genoemd, waarmee overmatige natriuminstroom wordt voorkomen. Al decennialang werd gedacht dat een korte drie‑aminozuursegment, bijgenaamd het IFM-motief, als een stopje zou inslaan om de stroom te blokkeren. Toch bleven veel details onduidelijk over hoe het hoofdpoortje aan de onderkant van het kanaal beweegt en hoe het IFM-motief deze beweging precies aanstuurt. Die leemtes hebben pogingen belemmerd om geneesmiddelen te ontwerpen die het kanaal richten zonder de fijn afgestemde timing te verstoren.
Het vastleggen van een tussentijds open state
Met behulp van hoogresolutie kryo-elektronenmicroscopie brachten de auteurs het volledige menselijke Nav1.5-kanaal in kaart in wat zij een intermediaire open toestand noemen. In deze configuratie staan de vier binnenste helices die het activatiepoortje vormen net wijd genoeg uit elkaar om gehydrateerde natriumionen door te laten, maar niet zo wijd als in volledig open structuren die eerder zijn beschreven. Moleculaire simulaties onder aangelegde spanning toonden aan dat water en natriumionen de pore kunnen passeren, hoewel alleen bij hogere spanningen dan in een volledig open kanaal, wat bevestigt dat deze toestand geleidt maar tussen de gebruikelijke open en geïnactiveerde vormen in zit. Een detergentmolecuul dat in het poortje vastzit helpt deze gevoelige ordening vast te houden, wat illustreert hoe kleine vormveranderingen nauwkeurig kunnen afstemmen of het kanaal ionen doorlaat of gesloten blijft.
Hoe zijcontacten het poortje helpen beheersen
Het team bracht ook een interactievlak in kaart tussen het N‑terminaal domein van het kanaal, dat in de cel naar binnen hangt, en een van de poortvormende helices die bekendstaat als S6 in domein I. Specifieke geladen aminozuren in deze regio’s vormen zoutbruggen die fungeren als kleine sluitingen die helpen de open poort te stabiliseren. Wanneer de onderzoekers deze residuen veranderden, veranderde de algemene vorm van de elektrische stromen: met name vertraagden sommige mutaties hoe snel het kanaal uitschakelde na opening. Verdere analyses lieten zien dat de S6-helix naar binnen en naar buiten kan wiegen, waardoor het poortje nauwer of wijder wordt. Verschillende patronen van contact met het N‑terminaal domein kwamen overeen met deze verschuivingen, waarmee de microscopische beweging van één enkele helix werd gekoppeld aan het vermogen van het kanaal om te schakelen tussen open en meer gesloten, geïnactiveerde vormen.
Een verborgen holte naast de inactivatiesluiting
Misschien wel de meest opvallende ontdekking ligt naast het IFM-motief zelf. In de intermediaire open structuur behoudt het IFM-segment zijn karakteristieke U‑vormige houding, strak gedokt in een hydrofoob pocketje, in plaats van volledig weg te zwaaien zoals sommige modellen voorstellen. Ernaast identificeerden de auteurs echter een tweede holte bekleed met negatief geladen residuen die een natriumion vasthoudt. Simulaties en experimenten suggereren dat ook andere positief geladen ionen dit nisje kunnen bezetten. Mutaties die de lading of chemie van de holte veranderden, beïnvloedden hoe makkelijk het kanaal inactieveert en hoe het IFM-motief zich gedraagt, wat aangeeft dat ionbinding hier de IFM-sluiting losser of strakker zet zonder dat het motief volledig uit zijn bekken hoeft te komen. Deze herinterpretatie helpt eerdere experimenten te verklaren waarin reactieve ionen gemodificeerde cysteïnes nabij het IFM-motief konden labelen, ook al leek het motief begraven te blijven.

Wat dit betekent voor hartritme en toekomstige geneesmiddelen
Samen werken deze bevindingen het klassieke "deur‑en‑wig" beeld van natriumkanaalinactivatie bij. In plaats van een simpel stopje dat in en uit wordt getrokken, lijkt Nav1.5 een gecoördineerde dans te gebruiken: een poort die in een intermediaire open positie kan blijven, zijcontacten die deze configuratie bestendigen of versoepelen, en een nabijgelegen ion‑afgestemde holte die bepaalt hoe stevig het IFM-motief het poortje gesloten houdt. Door deze alternatieve ionentoegangsweg en de invloed daarvan op gating te onthullen, biedt het werk een verfijnd structureel plan voor hoe cardiale natriumkanalen falen bij ziekte en wijst het op nieuwe, meer selectieve doelen voor anti‑aritmische therapieën.
Bronvermelding: Biswas, R., López-Serrano, A.L., Purohit, A. et al. Structural and functional mechanisms underlying activation gate dynamics and IFM motif accessibility in human Nav1.5. Nat Commun 17, 2820 (2026). https://doi.org/10.1038/s41467-026-69672-x
Trefwoorden: cardiale natriumkanaal, Nav1.5, snelle inactivatie, kryo-EM, cardiale aritmie