Clear Sky Science · ru
Неоадъювантная иммунохеморадиотерапия с ниволумабом, паклитакселом и цисплатином с последующей езофагэктомией при локально распространяющемся плоскоклеточном раке пищевода
Почему это важно для людей с раком пищевода
Рак пищевода — одно из самых смертоносных онкологических заболеваний в мире, и многие пациенты диагностируются только на стадии локально распространённого процесса. Врачи уже применяют тяжёлую комбинацию химиотерапии, облучения и хирургии в попытке вылечить таких пациентов, но выживаемость остаётся низкой. В этом исследовании проверяли, может ли добавление современного препарата иммунотерапии — ниволумаба — к стандартной предоперационной схеме лучше сократить опухоль и улучшить исходы у людей с распространённой формой заболевания — плоскоклеточным раком пищевода.
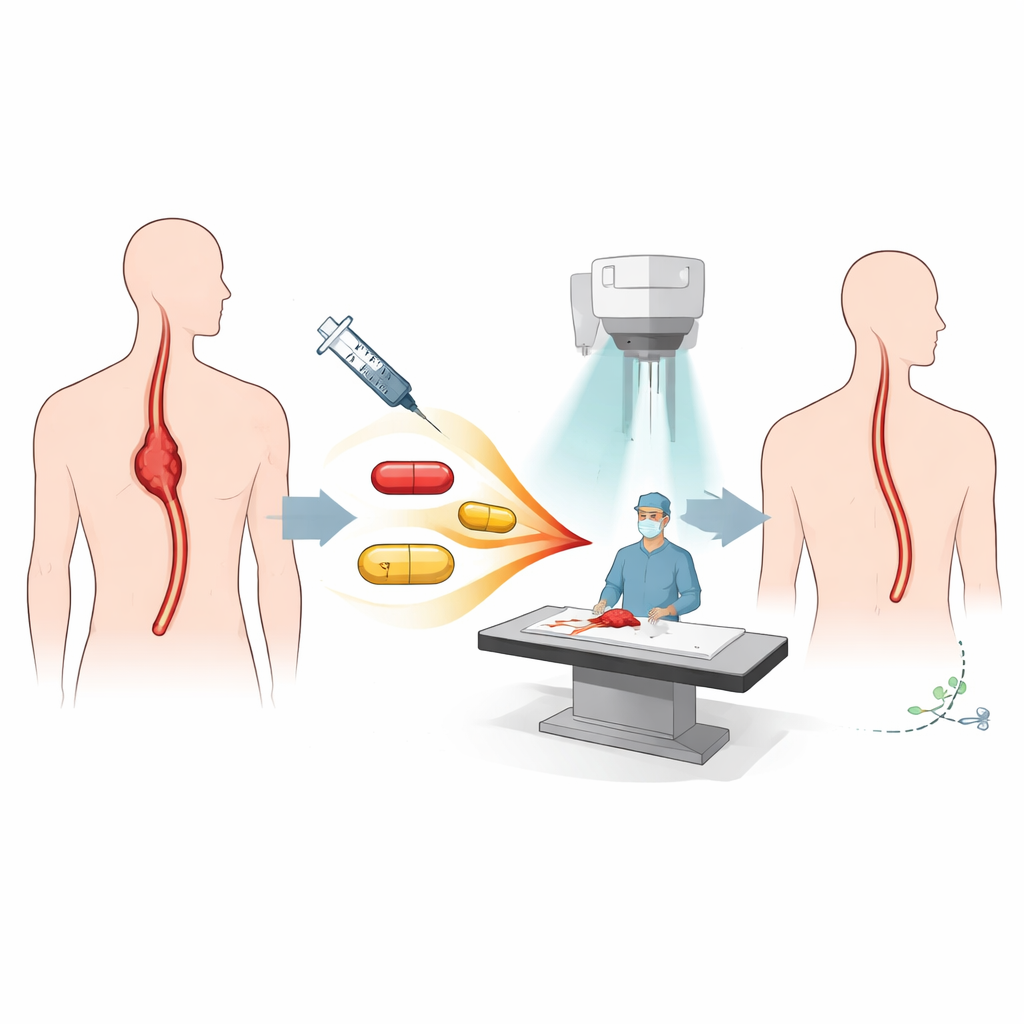
Ближе к стратегии лечения
Пациенты в этом исследовании имели локально распространяющийся плоскоклеточный рак пищевода в пределах грудной клетки и считались технически резектабельными. До операции им провели так называемую «неоадъювантную» терапию: пять недель химиотерапии (паклитаксел и цисплатин) одновременно с облучением грудной клетки, а также четыре введения ниволумаба — антитела, усиливающего иммунный ответ и помогающего Т‑клеткам организма атаковать опухоль. После завершения этой комбинированной схемы большинство пациентов перенесли минимально инвазивную езофагэктомию, при которой удаляется поражённая часть пищевода и реконструируется пищеварительный тракт.
Чего надеялись увидеть исследователи
Главным критерием успеха была частота патологоанатомического полного ответа — когда при удалении пищевода и лимфатических узлов и последующем микроскопическом исследовании не находят жизнеспособных раковых клеток. Предыдущие данные по одной лишь хеморадиотерапии показывали полный ответ примерно у четверти таких пациентов. Исследователи рассчитали, что если новая комбинация сможет повысить этот показатель примерно до половины пациентов, то её сочтут достаточно перспективной для продолжения в большем испытании.
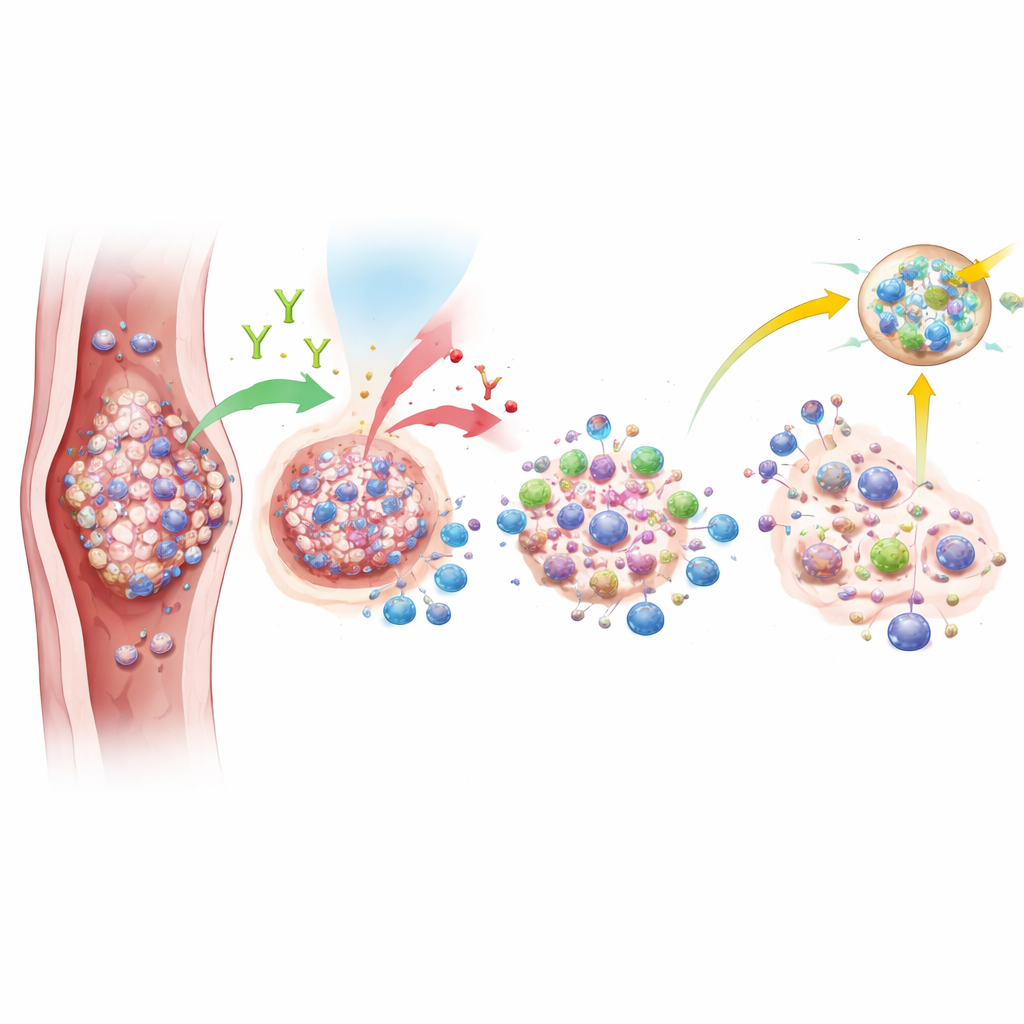
Что произошло на самом деле в испытании
В исследование было включено семнадцать пациентов. Комбинированное лечение в основном было проведено по плану: почти все получили полный курс облучения, большинство получили все дозы ниволумаба, а схему химиотерапии корректировали по показаниям при снижении показателей крови. Четырнадцать пациентов дошли до операции; трое не были оперированы из‑за прогрессирования болезни или других серьёзных проблем. Среди оперированных у четырёх не обнаружили оставшейся опухоли в удалённых тканях. Это соответствует 24% частоте полного ответа среди всех 17 пролеченных пациентов — почти идентично историческим результатам при одной хеморадиотерапии и ниже порога, необходимого для перехода ко второму этапу исследования. Показатели выживаемости также были скромными: у половины пациентов болезнь вернулась или прогрессировала примерно в течение года, а половина умерла к немного более чем двум годам наблюдения.
Безопасность и побочные эффекты сочетания
С точки зрения безопасности усиленная предоперационная схема была управляемой, но не без значимых проблем. Почти девять из десяти пациентов испытывали побочные эффекты, связанные с лечением, и примерно у каждого четвёртого развивалось тяжёлое снижение лейкоцитов на фоне химиотерапии и облучения. Иммунные побочные эффекты, связанные с ниволумабом — например, сыпь, лёгкий колит или нарушения работы эндокринных желёз — возникали почти у половины пациентов, но были преимущественно низкой степени тяжести; ни в одном случае не потребовались сильные стероиды и не было зарегистрировано смерть, напрямую связанная с лечением. Хирургическое вмешательство оставалось технически выполнимым после комбинированной терапии, хотя у нескольких пациентов случились серьёзные послеоперационные осложнения, включая два крупных расхождения в месте реконнекции пищеварительного тракта.
Сигналы из иммунной системы
Хотя общий эффект был ограничен, исследователи обнаружили любопытные свидетельства того, что опухоли некоторых пациентов значительно более чувствительны к такому подходу, чем у других. Предлечебные образцы опухоли исследовали на PD-L1 — белок, указывающий на то, насколько опухоль заметна иммунной системе — и на наличие специализированных иммунных скоплений, называемых третичными лимфоидными структурами. У пациентов с высокой экспрессией PD-L1 опухоль гораздо чаще полностью исчезала после терапии. Эти пациенты также, как правило, жили дольше. Генетические тесты показали, что опухоли, отвечавшие полностью, имели более активные иммунные клетки и меньше подавляющих клеток, а также усиленные сигналы, связанные с В‑клетками и функциями уничтожения раковых клеток. Эти данные намекают, что определённые иммунные характеристики опухоли могут помочь предсказать, кто действительно получает выгоду от добавления ниволумаба.
Что это означает в дальнейшем
Для среднего пациента с локально распространяющимся плоскоклеточным раком пищевода это небольшое исследование указывает на то, что простое добавление ниволумаба к стандартной хеморадиотерапии перед операцией не приводит к драматическому улучшению показателей излечения и пока не оправдывает изменения рутинной практики. В то же время оно показывает, что комбинацию можно проводить относительно безопасно, и что подгруппа пациентов — с высокой экспрессией PD-L1 и специфическими иммунными сигнатурами в опухоли — может получить большую пользу от этой стратегии. Потребуются более крупные, тщательно спланированные испытания и лучшие тесты для отбора вероятных респондентов, чтобы решить, может ли таргетирование иммунотерапии по этим иммунным маркёрам действительно изменить прогноз при этом тяжёлом заболевании.
Цитирование: Huang, TC., Guo, JC., Lin, CC. et al. Neoadjuvant immunochemoradiotherapy with nivolumab, paclitaxel, and cisplatin followed by esophagectomy for locally advanced esophageal squamous cell carcinoma. Br J Cancer 134, 1403–1412 (2026). https://doi.org/10.1038/s41416-026-03349-6
Ключевые слова: плоскоклеточный рак пищевода, неоадъювантная терапия, иммунотерапия, хеморадиотерапия, биомаркер PD-L1