Clear Sky Science · pl
Neoadjuwante immunochemioradioterapia z niwolumabem, paklitakselem i cisplatyną, a następnie esofagektomia w przypadku miejscowo zaawansowanego płaskonabłonkowego raka przełyku
Dlaczego to ma znaczenie dla osób z rakiem przełyku
Rak przełyku jest jednym z najbardziej śmiertelnych nowotworów na świecie, a wielu pacjentów jest diagnozowanych dopiero, gdy choroba osiąga stadium miejscowo zaawansowane. Lekarze już stosują intensywne połączenie chemioterapii, radioterapii i operacji, aby próbować wyleczyć tych pacjentów, jednak przeżycia nadal są niskie. W tym badaniu sprawdzano, czy dodanie nowoczesnego leku immunoterapeutycznego — niwolumabu — do standardowego leczenia przedoperacyjnego może lepiej zmniejszyć guzy i poprawić wyniki u osób z powszechną postacią choroby, tj. płaskonabłonkowym rakiem przełyku.
Dokładniej o strategii leczenia
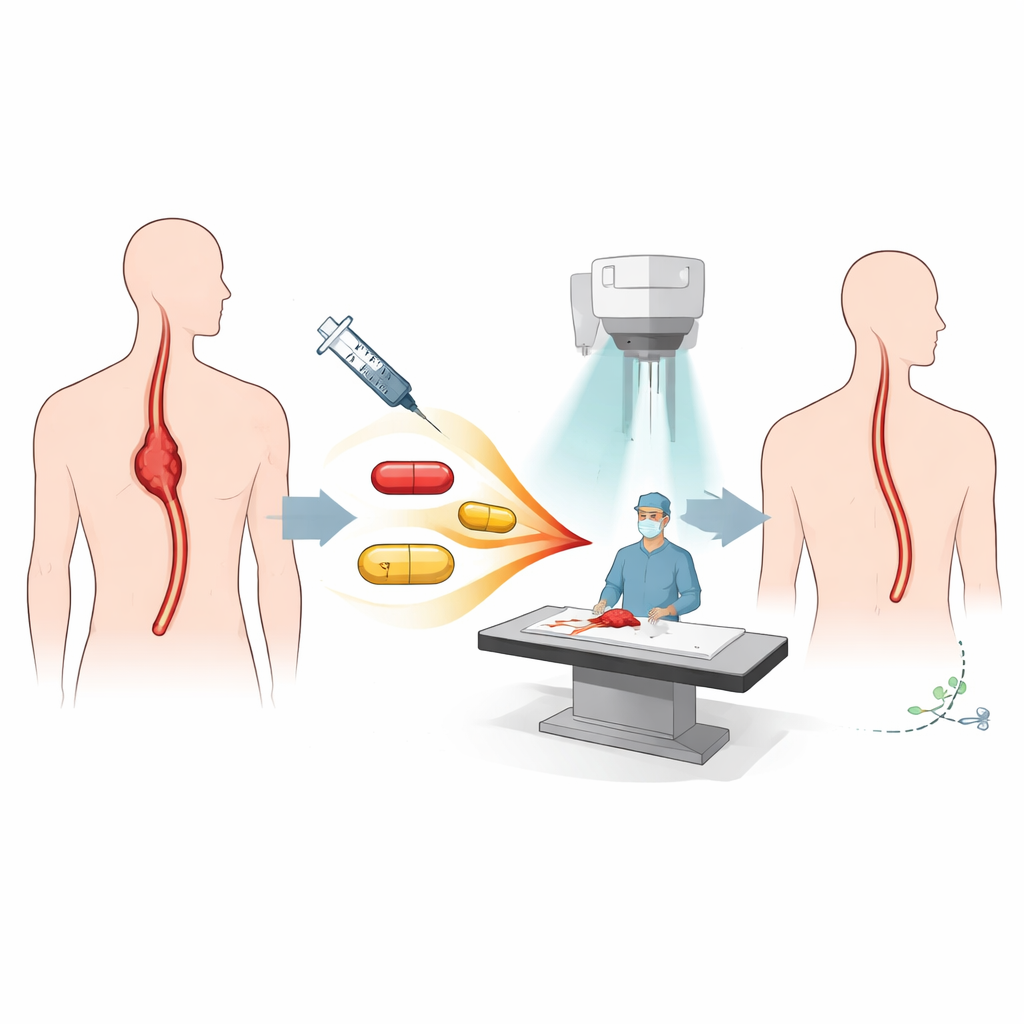
Pacjenci w tym badaniu mieli miejscowo zaawansowanego płaskonabłonkowego raka przełyku ograniczonego do klatki piersiowej i nadal uznanego za możliwy do usunięcia chirurgicznie. Przed operacją otrzymali tzw. terapię neoadiuwantową: pięć tygodni chemioterapii (paklitaksel i cisplatyna) podawanej jednocześnie z radioterapią na klatkę piersiową, oraz cztery dawki niwolumabu — przeciwciała wzmacniającego odpowiedź immunologiczną, które pomaga limfocytom T atakować nowotwór. Po zakończeniu tego skojarzonego kursu większość pacjentów przeszła minimalnie inwazyjną esofagektomię, podczas której usuwana jest chorobowo zmieniona część przełyku, a przewód pokarmowy jest odbudowywany.
Co badacze mieli nadzieję zobaczyć
Głównym miernikiem powodzenia była odsetek pacjentów osiągających patologiczne całkowite wyleczenie (pathologic complete response) — co oznacza, że po usunięciu przełyku i węzłów chłonnych oraz badaniu patologicznym pod mikroskopem nie stwierdzono żywych komórek nowotworowych. Wcześniejsze badania z samą chemioradioterapią dają całkowitą odpowiedź u około jednej czwartej takich pacjentów. Zespół zaprojektował badanie tak, że jeśli nowe skojarzenie podniosłoby ten odsetek do około połowy pacjentów, uznano by je za obiecujące i warte dalszego badania w większej próbie.
Co faktycznie wydarzyło się w badaniu
Do badania zapisano siedemnastu pacjentów. Leczenie skojarzone zostało w dużej mierze przeprowadzone zgodnie z planem: niemal wszyscy otrzymali pełną dawkę radioterapii, większość otrzymała wszystkie dawki niwolumabu, a chemioterapia była modyfikowana w razie potrzeby z powodu zaburzeń w morfologii krwi. Czternastu pacjentów przeszło operację; trzech nie przeszło, ponieważ ich choroba postępowała lub pojawiły się inne poważne problemy. Spośród tych, którzy mieli operację, u czterech nie stwierdzono pozostałości raka w usuniętych tkankach. Odpowiada to 24% odsetkowi całkowitej odpowiedzi wśród wszystkich 17 leczonych pacjentów — niemal identycznemu z historycznymi wynikami przy samej chemioradioterapii i poniżej progu potrzebnego do przejścia do drugiego etapu badania. Czasy przeżycia były również umiarkowane: połowa pacjentów doświadczyła nawrotu lub progresji choroby około roku, a połowa zmarła po nieco ponad dwóch latach.
Bezpieczeństwo i działania niepożądane kombinacji
Pod względem bezpieczeństwa zintensyfikowany schemat przedoperacyjny był możliwy do przeprowadzenia, lecz nie pozbawiony istotnych skutków. Prawie dziewięciu na dziesięciu pacjentów doświadczyło jakichś działań niepożądanych związanych z leczeniem, a około jedna czwarta rozwinęła ciężkie obniżenia liczby białych krwinek w wyniku chemioterapii i radioterapii. Problemy związane z układem odpornościowym wywołane niwolumabem, takie jak wysypka skórna, łagodne zapalenie okrężnicy czy zaburzenia czynności gruczołów dokrewnych, wystąpiły u prawie połowy pacjentów, ale miały łagodny stopień nasilenia; żadne nie wymagało silnych steroidów ani nie doprowadziło bezpośrednio do zgonu związanego z leczeniem. Sama operacja pozostała technicznie wykonalna po terapii skojarzonej, chociaż kilku pacjentów doświadczyło poważnych powikłań chirurgicznych, w tym dwóch z istotnymi przeciekami w miejscu zespolenia przewodu pokarmowego.
Sygnały z układu odpornościowego
Choć ogólny efekt był ograniczony, badacze zauważyli intrygujące wskazówki, że guzy niektórych pacjentów były znacznie bardziej wrażliwe na to podejście niż u innych. Próbki guzów pobrane przed leczeniem oceniano pod kątem PD-L1 — białka, które może wskazywać, jak rozpoznawalny jest nowotwór dla układu odpornościowego — oraz obecności wyspecjalizowanych skupisk komórek odpornościowych zwanych trzeciorzędowymi strukturami limfatycznymi. Pacjenci, u których guzy wykazywały wysokie poziomy PD-L1, mieli znacznie większe szanse na osiągnięcie całkowitego zniknięcia nowotworu po terapii. Mieli też tendencję do dłuższego przeżycia. Testy genetyczne sugerowały, że guzy, które odpowiedziały całkowicie, miały więcej aktywnych komórek odpornościowych i mniej komórek supresyjnych, a także silniejsze sygnały związane z komórkami B i funkcjami zabijającymi komórki nowotworowe. Wyniki te sugerują, że określone cechy immunologiczne w guzie mogą pomóc przewidzieć, kto rzeczywiście odnosi korzyść z dodania niwolumabu.
Co to oznacza na przyszłość
Dla przeciętnego pacjenta z miejscowo zaawansowanym płaskonabłonkowym rakiem przełyku to małe badanie sugeruje, że samo dodanie niwolumabu do standardowej chemioradioterapii przed operacją nie zwiększa znacząco wskaźników wyleczeń i nie uzasadnia jeszcze zmiany rutynowej praktyki. Pokazuje jednak także, że połączenie to można stosować bezpiecznie oraz że podgrupa pacjentów — ci, których guzy silnie wykazują ekspresję PD-L1 i określone sygnatury immunologiczne — może czerpać większą korzyść z tej strategii. Potrzebne będą większe, starannie zaprojektowane badania oraz lepsze testy do wyboru prawdopodobnych responderów, aby rozstrzygnąć, czy dostosowanie immunoterapii na podstawie tych markerów immunologicznych w końcu przyniesie istotną poprawę dla tej trudnej choroby.
Cytowanie: Huang, TC., Guo, JC., Lin, CC. et al. Neoadjuvant immunochemoradiotherapy with nivolumab, paclitaxel, and cisplatin followed by esophagectomy for locally advanced esophageal squamous cell carcinoma. Br J Cancer 134, 1403–1412 (2026). https://doi.org/10.1038/s41416-026-03349-6
Słowa kluczowe: płaskonabłonkowy rak przełyku, terapia neoadiuwantowa, immunoterapia, chemioterapia skojarzona z radioterapią, biomarker PD-L1