Clear Sky Science · fr
Immunochimioradiothérapie néoadjuvante par nivolumab, paclitaxel et cisplatine suivie d’une oesophagectomie pour le carcinome épidermoïde œsophagien localement avancé
Pourquoi cela compte pour les personnes confrontées au cancer de l’œsophage
Le cancer de l’œsophage est l’un des cancers les plus mortels au monde, et de nombreux patients sont diagnostiqués seulement une fois la maladie devenue localement avancée. Les médecins utilisent déjà une association agressive de chimiothérapie, de radiothérapie et de chirurgie pour tenter de guérir ces patients, mais la survie reste faible. Cette étude a testé si l’ajout d’un médicament d’immunothérapie moderne, le nivolumab, au traitement préopératoire standard pouvait mieux réduire les tumeurs et améliorer les résultats pour des personnes atteintes d’une forme courante de la maladie appelée carcinome épidermoïde de l’œsophage.
Un examen plus détaillé de la stratégie thérapeutique
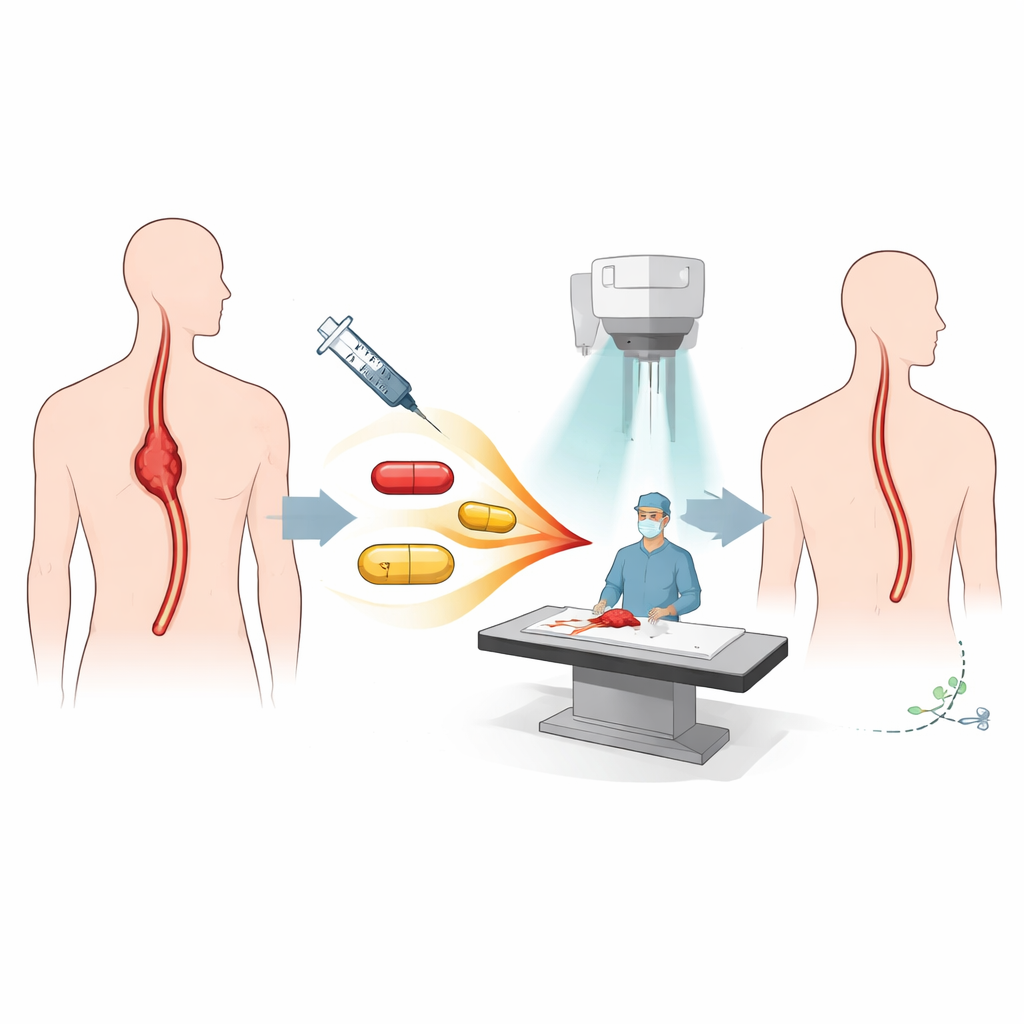
Les patients inclus dans cet essai avaient tous un carcinome épidermoïde œsophagien localement avancé, limité au thorax et encore considéré comme résécable par chirurgie. Avant la chirurgie, ils ont reçu ce que les médecins appellent une thérapie « néoadjuvante » : cinq semaines de chimiothérapie (paclitaxel et cisplatine) administrée simultanément à la radiothérapie thoracique, plus quatre doses de nivolumab, un anticorps qui stimule le système immunitaire en aidant les lymphocytes T à attaquer le cancer. Après avoir terminé ce traitement combiné, la plupart des patients ont subi une oesophagectomie mini-invasive, au cours de laquelle la portion atteinte de l’œsophage est retirée et le tube digestif est reconstruit.
Ce que les chercheurs espéraient observer
Le critère principal de succès était le nombre de patients présentant une réponse pathologique complète — c’est‑à‑dire qu’après ablation de l’œsophage et des ganglions lymphatiques et examen au microscope, aucun cellule cancéreuse viable n’était détectée. Les travaux antérieurs avec la seule chimioradiothérapie aboutissent à une réponse complète chez environ un quart de ces patients. L’équipe a conçu l’étude de sorte que si la nouvelle combinaison pouvait porter ce taux à environ la moitié des patients, elle serait jugée suffisamment prometteuse pour être étudiée dans un essai de plus grande envergure.
Ce qui s’est réellement passé dans l’essai
Sept‑à‑dix-sept patients ont été inclus. Le traitement combiné a été administré pour l’essentiel comme prévu : quasiment tous ont reçu la radiothérapie à dose complète, la plupart ont reçu toutes les doses de nivolumab, et la chimiothérapie a été adaptée selon les effets sur les numérations sanguines. Quatorze patients sont allés en chirurgie ; trois ne l’ont pas faite parce que leur cancer a progressé ou en raison d’autres problèmes graves. Parmi ceux opérés, quatre n’avaient plus de cancer dans les tissus retirés. Cela correspond à un taux de réponse complète de 24 % sur les 17 patients traités — presque identique aux résultats historiques avec la seule chimioradiothérapie, et inférieur au seuil nécessaire pour passer à une deuxième phase de l’essai. Les durées de survie étaient également modestes : la moitié des patients a vu la maladie récidiver ou progresser autour d’un an, et la moitié était décédée à un peu plus de deux ans.
Sécurité et effets secondaires de la combinaison
Du point de vue de la sécurité, le schéma intensifié avant chirurgie était gérable mais non négligeable. Près de neuf patients sur dix ont présenté des effets indésirables liés au traitement, et environ un sur quatre a développé des chutes sévères de globules blancs dues à la chimiothérapie et à la radiothérapie. Des effets immunitaires liés au nivolumab, tels qu’éruption cutanée, colite légère ou perturbations des glandes hormonales, sont survenus chez près de la moitié des patients mais étaient de faible grade ; aucun n’a requis de fortes doses de corticoïdes ni n’a directement entraîné un décès lié au traitement. La chirurgie est restée techniquement faisable après la thérapie combinée, même si plusieurs patients ont connu des complications chirurgicales graves, dont deux avec des fuites majeures au niveau de la réconnexion du tube digestif.
Signaux provenant du système immunitaire
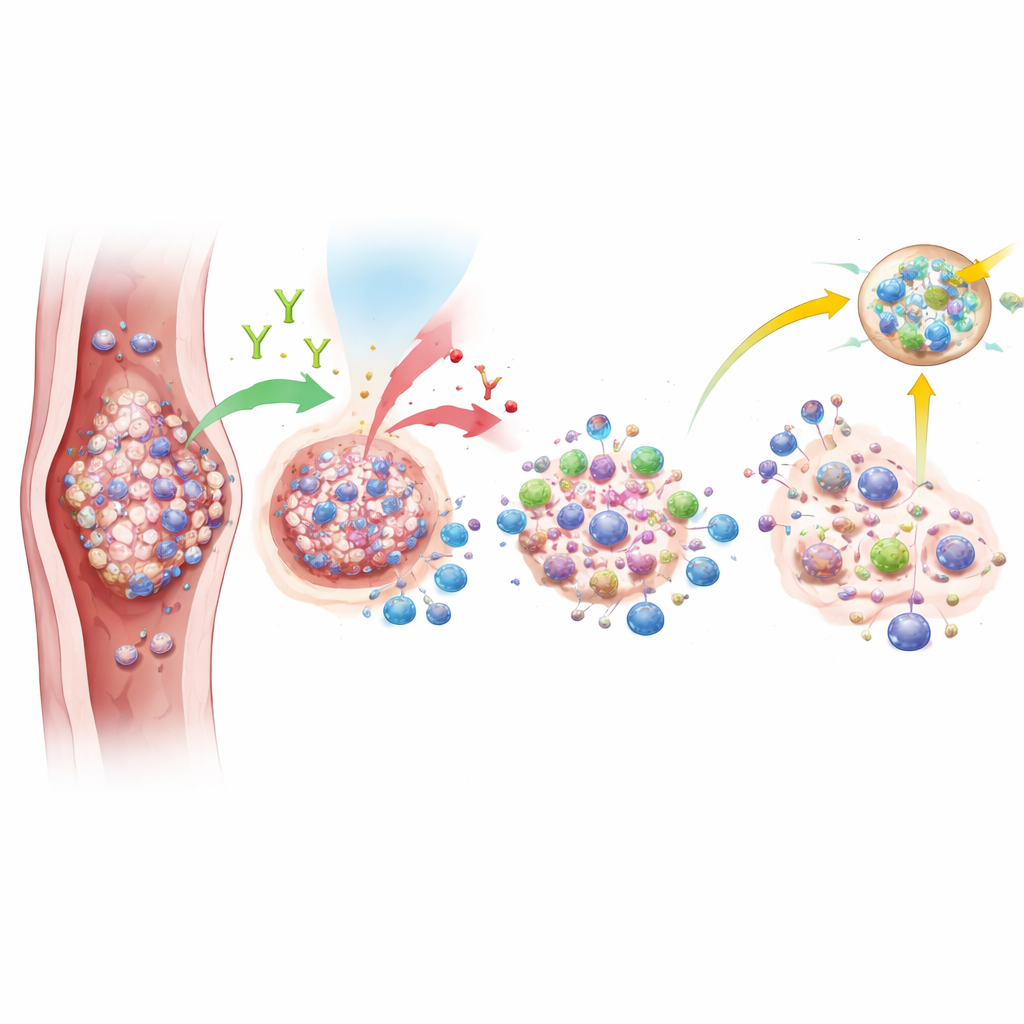
Bien que le bénéfice global ait été limité, les chercheurs ont observé des indices intrigants montrant que les tumeurs de certains patients étaient bien plus sensibles à cette approche que d’autres. Des échantillons tumoraux prétraitement ont été examinés pour le PD-L1, une protéine pouvant indiquer la visibilité d’un cancer par le système immunitaire, et pour la présence de structures immunitaires spécialisées appelées structures lymphoïdes tertiaires. Les patients dont les tumeurs présentaient des taux élevés de PD-L1 étaient beaucoup plus susceptibles d’obtenir une disparition complète du cancer après la thérapie. Ils semblaient aussi vivre plus longtemps. Les analyses génétiques suggèrent que les tumeurs répondant complètement avaient des cellules immunitaires plus actives et moins de cellules suppressives, ainsi que des signaux plus marqués liés aux cellules B et aux fonctions cytotoxiques. Ces observations laissent penser que certaines caractéristiques immunitaires tumorales pourraient aider à prédire qui bénéficie réellement de l’ajout de nivolumab.
Ce que cela signifie pour l’avenir
Pour le patient moyen atteint d’un carcinome épidermoïde œsophagien localement avancé, ce petit essai suggère que l’ajout simple du nivolumab à la chimioradiothérapie standard avant chirurgie n’améliore pas de manière spectaculaire les taux de guérison et ne justifie pas encore de changer la pratique courante. Cependant, il montre aussi que la combinaison peut être administrée en toute sécurité et qu’un sous‑groupe de patients — ceux dont les tumeurs expriment fortement le PD-L1 et présentent des signatures immunitaires spécifiques — pourrait tirer davantage parti de cette stratégie. Des essais plus larges et mieux conçus et de meilleurs tests pour sélectionner les répondeurs potentiels seront nécessaires pour décider si le recours ciblé à l’immunothérapie en fonction de ces marqueurs immunitaires peut enfin faire progresser les résultats pour cette maladie difficile.
Citation: Huang, TC., Guo, JC., Lin, CC. et al. Neoadjuvant immunochemoradiotherapy with nivolumab, paclitaxel, and cisplatin followed by esophagectomy for locally advanced esophageal squamous cell carcinoma. Br J Cancer 134, 1403–1412 (2026). https://doi.org/10.1038/s41416-026-03349-6
Mots-clés: carcinome épidermoïde œsophagien, thérapie néoadjuvante, immunothérapie, chimioradiothérapie, biomarqueur PD-L1