Clear Sky Science · ru
ADAMTS4 вызывает привлечение миелоидных иммунных клеток и фиброгенез печени при печеночной болезни, связанной с метаболической дисфункцией
Почему рубцевание печени важно для повседневного здоровья
Метаболически обусловленная стеатотическая болезнь печени (MASLD) становится всё более распространённой по мере роста окружностей талии во всём мире. У многих людей скопление жира в печени бессимптомно прогрессирует в воспаление и образование рубцов, что в конечном итоге может привести к циррозу, печёночной недостаточности или раку. В этом исследовании обнаружен ранее недооценённый молекулярный участник — белок ADAMTS4, который, по-видимому, способствует замкнутому циклу воспаления и образования рубцовой ткани в жирной печени. Понимание роли этого виновника может открыть путь к более точным анализам крови и новым методам лечения, которые прервут повреждение печени до того, как оно станет необратимым.
Скрытый фермент в рубцующейся печени
Учёные начали с сравнения тканей печени почти 300 человек — от тех, у кого нет MASLD, до пациентов с выраженным воспалением и рубцеванием при жировой болезни печени. Они обнаружили, что уровень ADAMTS4, фермента, который обрезает крупные белки вне клеток, последовательно повышался по мере ухудшения болезни. Этот фермент был особенно обилен в активированных звездчатых клетках — специализированном типе клеток, который обычно находится в состоянии покоя, но при активации превращается в основного производителя рубцовой ткани. Команда подтвердила аналогичное повышение ADAMTS4 в нескольких мышиных моделях повреждения печени, независимо от того, были ли они вызваны нездоровой диетой или токсическими химикатами, и показала, что родственные члены этого семейства ферментов не повышались так же выраженно. 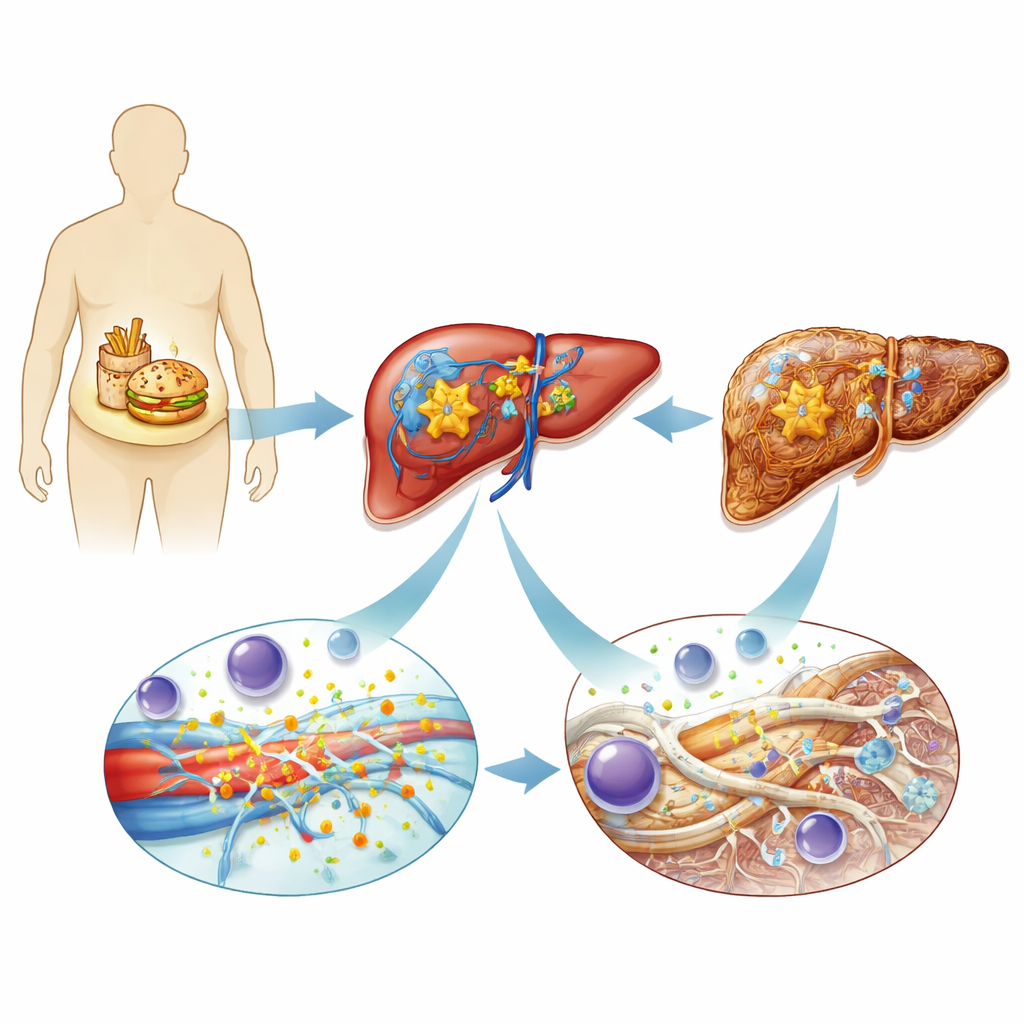
Выключение фермента смягчает повреждение печени
Чтобы проверить, является ли ADAMTS4 просто наблюдателем или активным драйвером болезни, учёные создали мышей, лишённых гена этого фермента. Когда этих животных кормили фиброгенной диетой с высоким содержанием жира и сахара или подвергали воздействию химических токсинов для печени, их печень демонстрировала меньше рубцевания, более низкие маркёры повреждения в крови и меньше фибротических полос под микроскопом по сравнению с нормальными мышами. Улучшение не было связано со снижением накопления жира — оно оставалось примерно таким же — а объяснялось заметным снижением притока миелоидных иммунных клеток, особенно макрофагов, которые являются ключевыми усилителями воспаления. Напротив, вынужденная сверхэкспрессия ADAMTS4 в печени у защищённых нокаутных мышей восстановила интенсивное накопление коллагена и активный приток воспалительных клеток, что подчёркивает роль фермента как активного промоутера фиброза.
Как ADAMTS4 вызывает воспаление и образует рубцовую ткань
Углубляясь, команда изучала, как ADAMTS4 перестраивает печёночную среду. Звездчатые клетки с высоким содержанием ADAMTS4 расщепляют большой матриксный молекул версикан на фрагменты меньшего размера, известные как версикин. Эти фрагменты, производимые преимущественно звездчатыми клетками, а не другими клетками печени, стимулировали в культуре движение макрофагов к повреждённой области и их переход в более провоспалительное состояние, особенно в присутствии дополнительных иммунных стимулов. Параллельно исследователи обнаружили, что ADAMTS4 может прямо усиливать синтез коллагена — основного компонента рубцовой ткани — в человеческих звездчатых клетках путём активации сигнального белка STAT3, не полагаясь на классический путь TGF-β, часто обвиняемый в фиброзе. Когда STAT3 блокировали, ADAMTS4 больше не мог повышать уровни коллагена, связывая этот фермент как с привлечением иммунных клеток, так и с прямым образованием рубца. 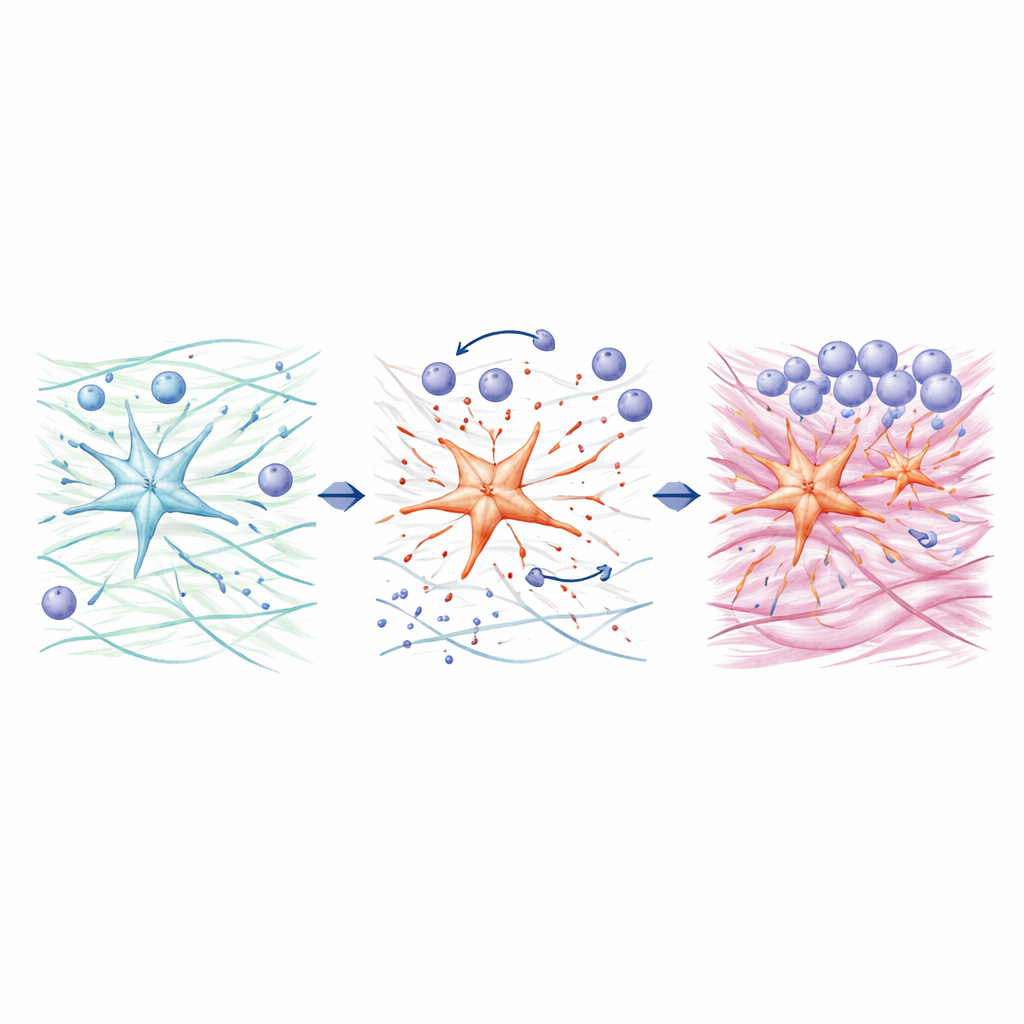
Генетические подсказки и кто может получить наибольшую пользу
Не у всех с жировой печенью развивается выраженное рубцевание, поэтому команда искала генетические варианты, которые могли бы регулировать активность ADAMTS4. Интегрируя данные экспрессии генов в печени с различиями в ДНК между пациентами, они выявили конкретные однонуклеотидные изменения в геноме, которые меняют, насколько сильно включается ADAMTS4 при MASLD. Один вариант, расположенный выше по потоку от гена ADAMTS4, был связан с особенно высокими уровнями фермента у пациентов с жировой печенью, но не у незатронутых индивидов. Лабораторные репортерные анализы показали, что этот участок ДНК может усиливать активность гена в зависимости от того, какая версия варианта присутствует. Эти данные позволяют предположить, что некоторые люди генетически предрасположены к более сильным ответам, опосредованным ADAMTS4, и могут получить наибольшую выгоду от терапии, нацеленной на этот фермент.
Что это значит для пациентов
Проще говоря, эта работа показывает, что ADAMTS4 действует как молекулярная педаль газа для рубцевания печени при жировой болезни. Он помогает призывать воспалительные иммунные клетки и побуждает клетки, производящие рубец, откладывать больше коллагена, со временем уплотняя орган. Поскольку фермент обнаруживается в крови и повышается с тяжестью болезни, он может войти в состав будущего анализа крови для выявления пациентов с высоким риском. Ещё важнее то, что препараты или антитела, нацеленные на блокирование ADAMTS4 — либо прерывающие его воздействие через фрагменты версикана или STAT3 — могли бы замедлить или остановить прогрессирование от жировой печени к циррозу, особенно у людей, чья генетика делает их особенно уязвимыми.
Цитирование: Park, J., Kim, T., Shim, W.S. et al. ADAMTS4 elicits myeloid-derived immune cell recruitment and liver fibrogenesis in metabolic dysfunction-associated steatotic liver disease. Sig Transduct Target Ther 11, 168 (2026). https://doi.org/10.1038/s41392-026-02679-4
Ключевые слова: жировая болезнь печени, фиброз печени, ADAMTS4, иммунные клетки, генетический риск