Clear Sky Science · fr
ADAMTS4 provoque le recrutement de cellules immunitaires d’origine myéloïde et la fibrogenèse hépatique dans la stéatose hépatique associée à un dysfonctionnement métabolique
Pourquoi la cicatrisation du foie compte pour la santé quotidienne
La stéatose hépatique associée à un dysfonctionnement métabolique (MASLD) devient de plus en plus fréquente à mesure que les tours de taille augmentent dans le monde. Chez de nombreuses personnes, cette accumulation de graisse dans le foie évolue silencieusement vers une inflammation et une cicatrisation, menant éventuellement à la cirrhose, à l’insuffisance hépatique ou au cancer. Cette étude met en lumière un acteur moléculaire jusque-là sous-estimé, une protéine nommée ADAMTS4, qui semble contribuer au cercle vicieux d’inflammation et de formation de tissu cicatriciel dans le foie gras. Comprendre ce coupable pourrait ouvrir la voie à des tests sanguins plus précis et à de nouveaux traitements qui interrompent les lésions hépatiques avant qu’elles ne deviennent irréversibles.
Une enzyme discrète dans le foie cicatrisé
Les chercheurs ont commencé par comparer des tissus hépatiques provenant de près de 300 personnes, allant d’individus sans MASLD à des patients présentant une inflammation et une fibrose hépatiques avancées. Ils ont constaté que les niveaux d’ADAMTS4, une enzyme qui taille de grosses protéines en dehors des cellules, augmentaient progressivement avec l’aggravation de la maladie. L’enzyme était particulièrement abondante dans les cellules étoilées activées, un type cellulaire spécialisé qui reste normalement silencieux mais qui, une fois activé, se transforme en un important producteur de tissu cicatriciel. L’équipe a confirmé des augmentations similaires d’ADAMTS4 dans plusieurs modèles murins de lésion hépatique, qu’elles soient déclenchées par des régimes malsains ou par des produits chimiques toxiques, et a montré que d’autres membres apparentés de cette famille enzymatique n’augmentaient pas de la même manière. 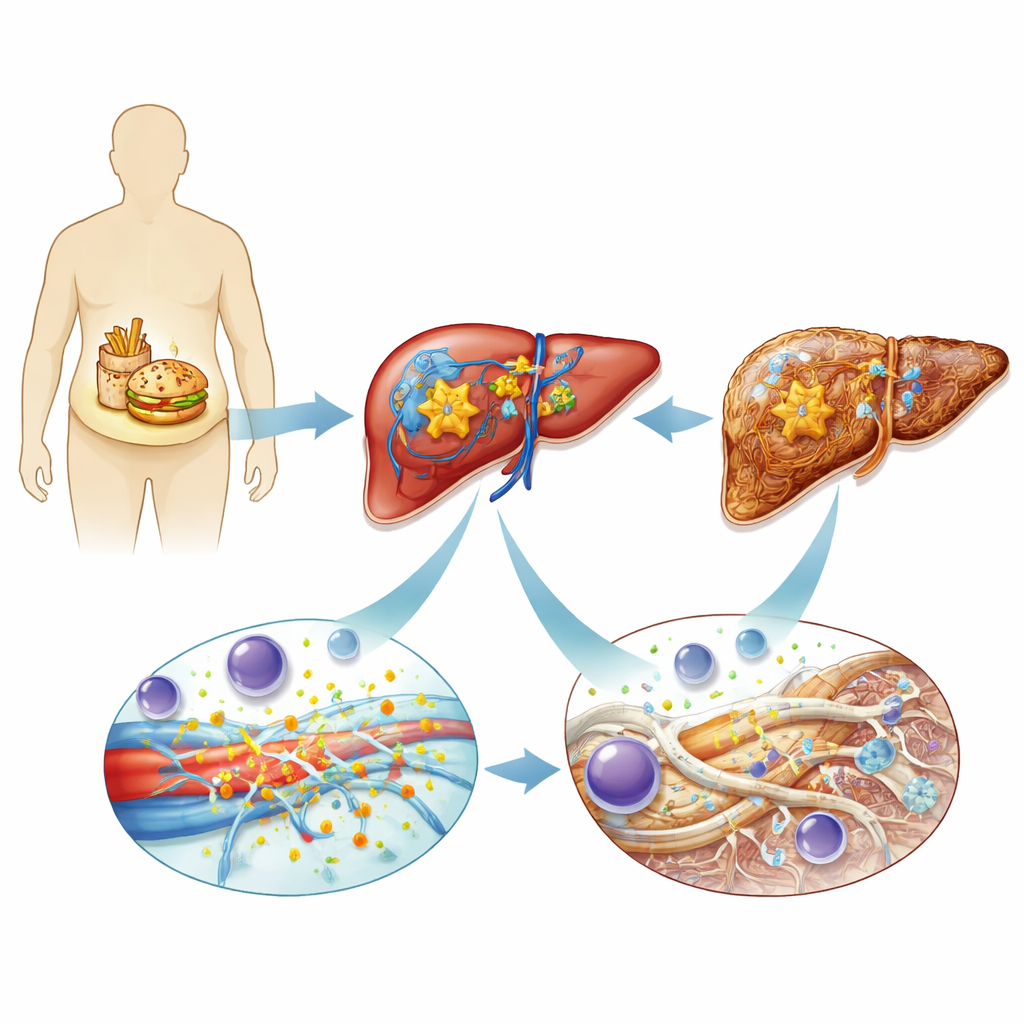
Éteindre l’enzyme atténue les lésions hépatiques
Pour tester si ADAMTS4 n’était qu’un témoin ou un moteur actif de la maladie, les scientifiques ont créé des souris dépourvues du gène codant cette enzyme. Lorsque ces animaux ont été nourris avec des régimes riches en graisses et en sucres favorisant la fibrose, ou exposés à des toxines hépatiques chimiques, leurs foies présentaient moins de cicatrisation, des marqueurs de lésion sanguins plus faibles et moins de bandes fibreuses au microscope que chez les souris normales. L’amélioration ne provenait pas d’une réduction de l’accumulation de graisse, qui restait similaire, mais d’une baisse marquée de l’afflux de cellules immunitaires d’origine myéloïde, en particulier des macrophages, qui amplifient l’inflammation. À l’inverse, forcer une surexpression d’ADAMTS4 dans le foie de souris knock-out autrement protégées a restauré une forte accumulation de collagène et un important recrutement de cellules inflammatoires, soulignant que l’enzyme favorise activement la fibrose.
Comment ADAMTS4 déclenche l’inflammation et construit le tissu cicatriciel
En approfondissant, l’équipe a examiné comment ADAMTS4 reconfigure l’environnement hépatique. Les cellules étoilées riches en ADAMTS4 coupent une grande molécule de matrice appelée versican en fragments plus petits connus sous le nom de versikine. Ces fragments, produits principalement par les cellules étoilées plutôt que par d’autres cellules hépatiques, encouragent les macrophages en culture cellulaire à migrer vers la zone lésée et à adopter un profil plus pro-inflammatoire, surtout en présence de déclencheurs immunitaires supplémentaires. Parallèlement, les chercheurs ont découvert qu’ADAMTS4 peut directement augmenter la production de collagène, principal composant du tissu cicatriciel, dans des cellules étoilées humaines en activant une protéine de signalisation appelée STAT3, sans dépendre de la voie classique TGF-β souvent incriminée dans la fibrose. Lorsque STAT3 était bloqué, ADAMTS4 ne pouvait plus élever les niveaux de collagène, reliant ainsi cette enzyme à la fois au recrutement des cellules immunitaires et à la formation directe de cicatrices. 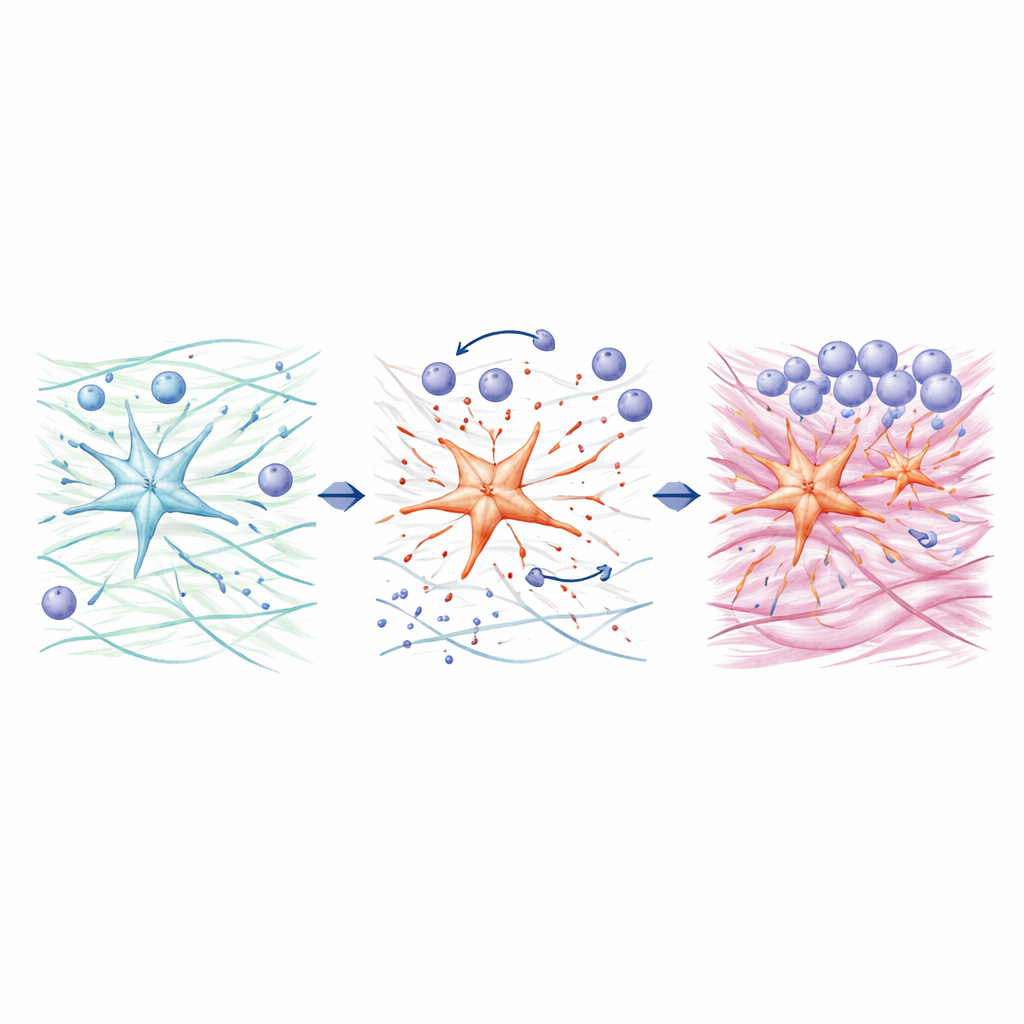
Indices génétiques et personnes susceptibles d’en bénéficier
Tout le monde ne développant pas une fibrose sévère même en cas de foie gras, l’équipe a recherché des variantes génétiques pouvant moduler l’activité d’ADAMTS4. En intégrant des données d’expression génique hépatique avec des différences d’ADN parmi les patients, ils ont identifié des changements d’une seule lettre dans le génome qui modifient l’intensité d’activation d’ADAMTS4 dans la MASLD. Une variante, située en amont du gène ADAMTS4, était associée à des niveaux d’enzyme particulièrement élevés chez les patients atteints de foie gras mais pas chez les individus indemnes. Des essais rapporteurs en laboratoire ont montré que cette région d’ADN peut renforcer l’activité du gène selon la version de la variante présente. Ces résultats suggèrent que certaines personnes pourraient être génétiquement prédisposées à des réponses plus marquées dépendant d’ADAMTS4 et bénéficier ainsi davantage de thérapies ciblant cette enzyme.
Ce que cela signifie pour les patients
En termes simples, ce travail suggère qu’ADAMTS4 agit comme un accélérateur moléculaire de la cicatrisation hépatique dans la maladie du foie gras. Il contribue à attirer des cellules immunitaires inflammatoires et incite les cellules productrices de cicatrices à déposer davantage de collagène, rigidifiant progressivement l’organe. Parce que l’enzyme se retrouve dans le sang et augmente avec la gravité de la maladie, elle pourrait faire partie d’un futur test sanguin visant à identifier les patients à haut risque. Plus important encore, des médicaments ou des anticorps conçus pour bloquer ADAMTS4 — ou pour interrompre ses effets en aval sur les fragments de versican ou STAT3 — pourraient ralentir ou arrêter la progression d’un foie gras vers la cirrhose, en particulier chez les personnes dont la génétique les rend particulièrement vulnérables.
Citation: Park, J., Kim, T., Shim, W.S. et al. ADAMTS4 elicits myeloid-derived immune cell recruitment and liver fibrogenesis in metabolic dysfunction-associated steatotic liver disease. Sig Transduct Target Ther 11, 168 (2026). https://doi.org/10.1038/s41392-026-02679-4
Mots-clés: maladie du foie gras, fibrose hépatique, ADAMTS4, cellules immunitaires, risque génétique