Clear Sky Science · it
ADAMTS4 induce il reclutamento di cellule immunitarie di derivazione mieloide e la fibrogenesi epatica nella malattia epatica steatosica associata a disfunzione metabolica
Perché la cicatrizzazione del fegato conta per la salute quotidiana
La malattia epatica steatosica associata a disfunzione metabolica (MASLD) sta diventando sempre più diffusa con l’aumento delle circonferenze vita nel mondo. In molte persone, l’accumulo di grasso nel fegato progredisce silenziosamente verso infiammazione e formazione di tessuto cicatriziale, portando infine a cirrosi, insufficienza epatica o cancro. Questo studio mette in luce un attore molecolare fino ad ora sottovalutato, una proteina chiamata ADAMTS4, che sembra favorire il ciclo vizioso di infiammazione e formazione di cicatrici nel fegato steatosico. Capire questo colpevole potrebbe aprire la strada a test del sangue più precisi e a nuovi trattamenti che interrompono il danno epatico prima che diventi irreversibile.
Un enzima nascosto nel fegato cicatrizzato
I ricercatori hanno iniziato confrontando tessuto epatico di quasi 300 persone, da individui senza MASLD fino a pazienti con infiammazione e fibrosi epatica avanzata. Hanno osservato che i livelli di ADAMTS4, un enzima che taglia grandi proteine al di fuori delle cellule, aumentavano progressivamente con il peggiorare della malattia. L’enzima era particolarmente abbondante nelle cellule stellate attivate, un tipo cellulare specializzato che normalmente rimane quiescente ma che, una volta attivato, si trasforma in un importante produttore di tessuto cicatriziale. Il gruppo ha confermato aumenti simili di ADAMTS4 in diversi modelli murini di danno epatico, sia indotti da diete malsane sia da sostanze tossiche, e ha mostrato che membri correlati della stessa famiglia enzimatica non aumentavano nella stessa misura. 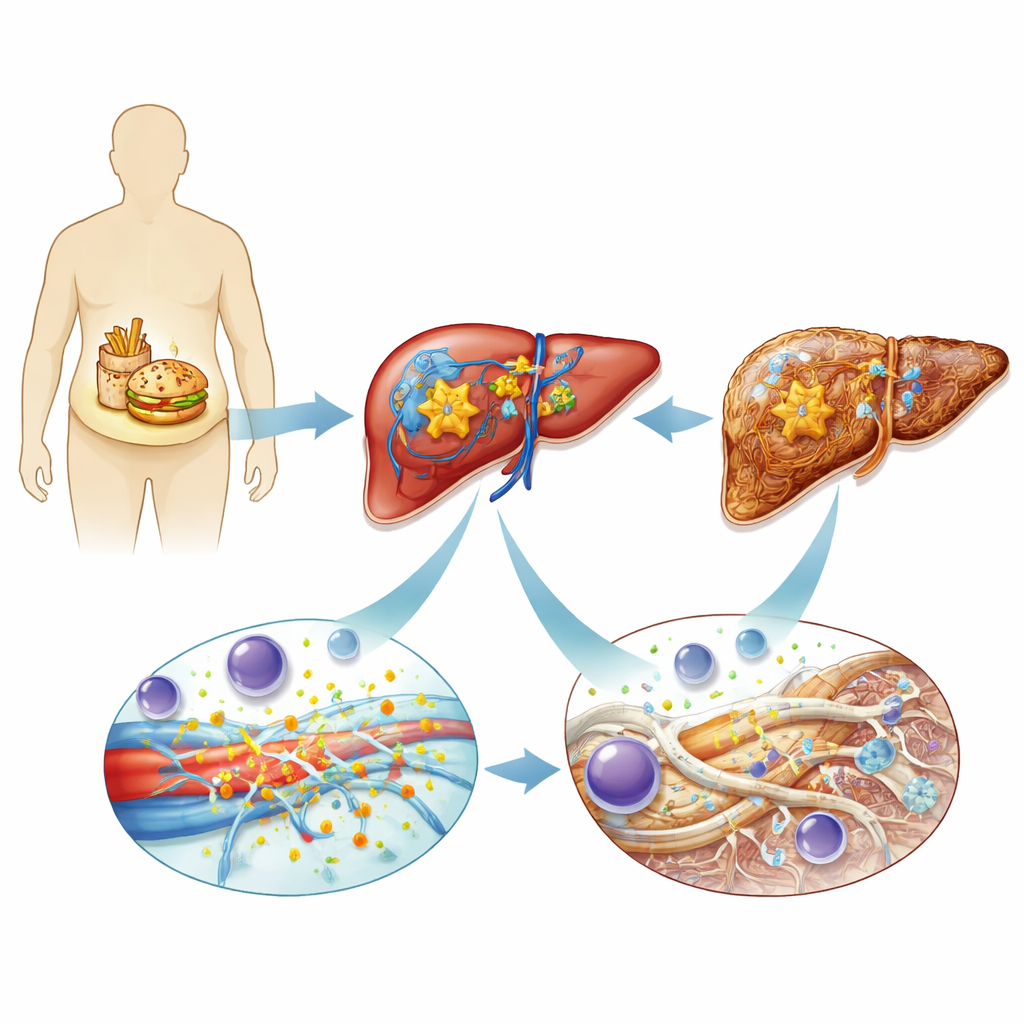
Spegnere l’enzima attenua il danno epatico
Per verificare se ADAMTS4 fosse solo un spettatore o un effettivo promotore della malattia, gli scienziati hanno creato topi privi del gene per questo enzima. Quando questi animali sono stati alimentati con diete fibrogeniche ad alto contenuto di grassi e zuccheri, o esposti a tossine epatiche chimiche, i loro fegati mostravano meno cicatrici, livelli ematici di danno più bassi e meno bande fibrotiche al microscopio rispetto ai topi normali. Il miglioramento non dipendeva da una riduzione dell’accumulo di grasso, che rimaneva simile, ma da una marcata diminuzione dell’afflusso di cellule immunitarie di derivazione mieloide, in particolare macrofagi, che sono amplificatori chiave dell’infiammazione. Al contrario, forzare la sovraespressione di ADAMTS4 nel fegato di topi knockout altrimenti protetti ha ripristinato l’abbondante deposito di collagene e il forte reclutamento di cellule infiammatorie, sottolineando che l’enzima promuove attivamente la fibrosi.
Come ADAMTS4 alimenta l’infiammazione e costruisce la cicatrice
Approfondendo, il team ha indagato come ADAMTS4 rimodelli l’ambiente epatico. Le cellule stellate ricche di ADAMTS4 tagliano una grande molecola della matrice chiamata versican in frammenti più piccoli noti come versikine. Questi frammenti, prodotti principalmente dalle cellule stellate piuttosto che da altre cellule del fegato, incoraggiavano i macrofagi in coltura cellulare a muoversi verso l’area danneggiata e ad adottare uno stato più pro-infiammatorio, specialmente in presenza di ulteriori stimoli immunitari. Parallelamente, i ricercatori hanno scoperto che ADAMTS4 può aumentare direttamente la produzione di collagene, componente principale del tessuto cicatriziale, nelle cellule stellate umane attivando una proteina di segnalazione chiamata STAT3, senza fare affidamento sulla via classica del TGF-β spesso implicata nella fibrosi. Quando STAT3 veniva bloccato, ADAMTS4 non riusciva più ad aumentare i livelli di collagene, collegando questo enzima sia al reclutamento delle cellule immunitarie sia alla formazione diretta di cicatrice. 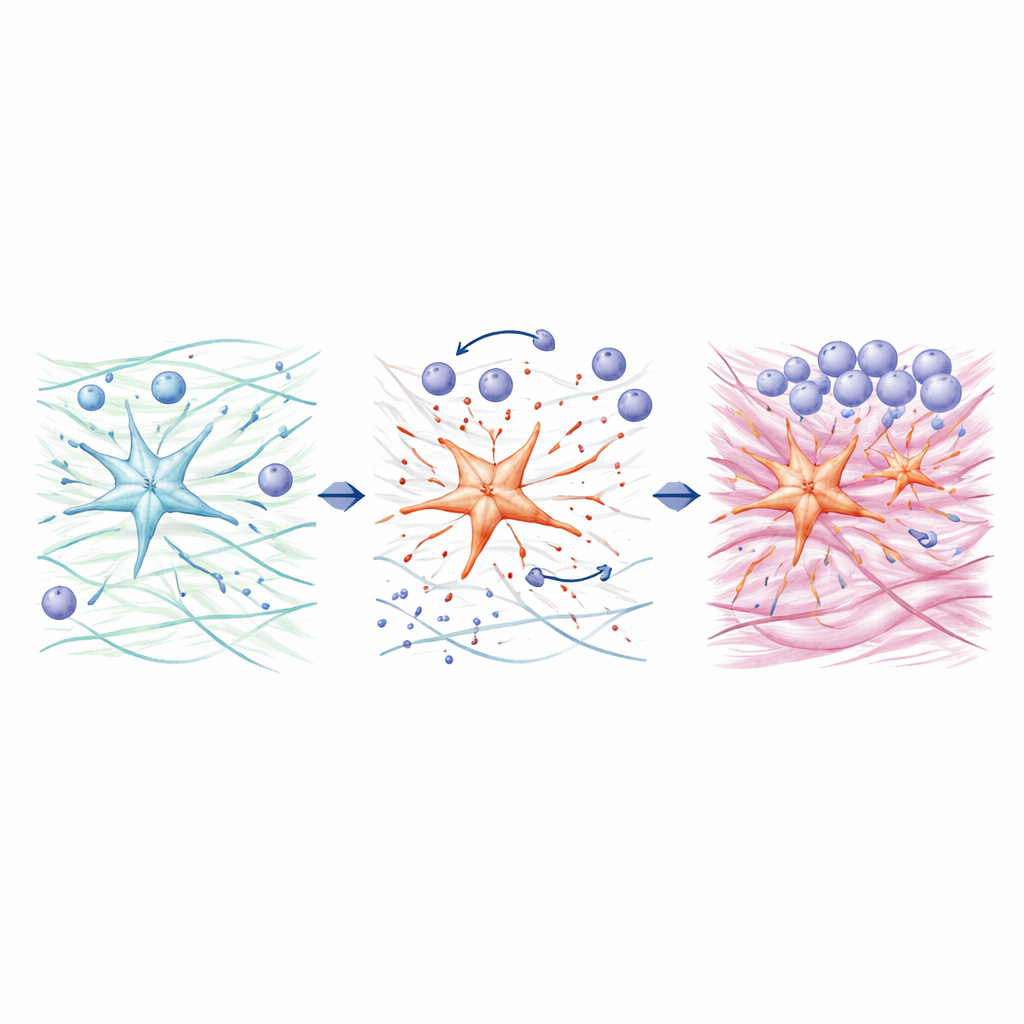
Indizi genetici e chi potrebbe trarne più beneficio
Non tutti i pazienti con fegato grasso sviluppano fibrosi severa, quindi il gruppo ha cercato varianti genetiche che potessero modulare l’attività di ADAMTS4. Integrando dati di espressione genica epatica con differenze nel DNA tra i pazienti, hanno identificato specifiche varianti a singola lettera nel genoma che alterano quanto intensamente ADAMTS4 viene attivato nella MASLD. Una variante, situata a monte del gene ADAMTS4, era associata a livelli particolarmente elevati dell’enzima nei pazienti con fegato steatosico ma non negli individui non affetti. Saggi di reporter di laboratorio hanno mostrato che questa regione di DNA può aumentare l’attività genica in modo dipendente dalla versione della variante presente. I risultati suggeriscono che alcune persone potrebbero essere geneticamente predisposte a risposte ADAMTS4 più forti e potrebbero trarre il massimo beneficio da terapie mirate contro questo enzima.
Cosa significa per i pazienti
In termini semplici, questo lavoro suggerisce che ADAMTS4 agisce come un acceleratore molecolare della cicatrizzazione epatica nella malattia del fegato grasso. Aiuta a richiamare cellule immunitarie infiammatorie e incoraggia le cellule produttrici di cicatrice a depositare più collagene, indurendo l’organo nel tempo. Poiché l’enzima è rilevabile nel sangue e aumenta con la gravità della malattia, potrebbe far parte di un futuro test ematico per individuare i pazienti ad alto rischio. Ancora più importante, farmaci o anticorpi progettati per bloccare ADAMTS4—or interrompere i suoi effetti a valle sui frammenti di versican o su STAT3—potrebbero rallentare o arrestare la progressione da fegato grasso a cirrosi, specialmente in individui la cui genetica li rende particolarmente vulnerabili.
Citazione: Park, J., Kim, T., Shim, W.S. et al. ADAMTS4 elicits myeloid-derived immune cell recruitment and liver fibrogenesis in metabolic dysfunction-associated steatotic liver disease. Sig Transduct Target Ther 11, 168 (2026). https://doi.org/10.1038/s41392-026-02679-4
Parole chiave: steatosi epatica, fibrosi epatica, ADAMTS4, cellule immunitarie, rischio genetico