Clear Sky Science · ru
Фотоакустическая микроскопия выявляет глубинные ангиогенные ответы в 3D-биопечатных моделях опухоль–сосуд
Почему важно заглядывать внутрь крошечных опухолей
Раковые опухоли не растут в изоляции — они выстраивают собственную сеть кровеносных сосудов, чтобы доставлять кислород и питательные вещества. Многие современные препараты пытаются перерезать эту «линию жизни», но оценка их эффективности обычно опирается на животные модели или плоские монослои клеток в чашках Петри, что имеет существенные недостатки. В этом исследовании представлен способ вырастить в лаборатории миниатюрные трёхмерные системы «опухоль–сосуд» и затем заглянуть глубоко внутрь них без вскрытия, используя звуковой метод визуализации — фотоакустическую микроскопию.
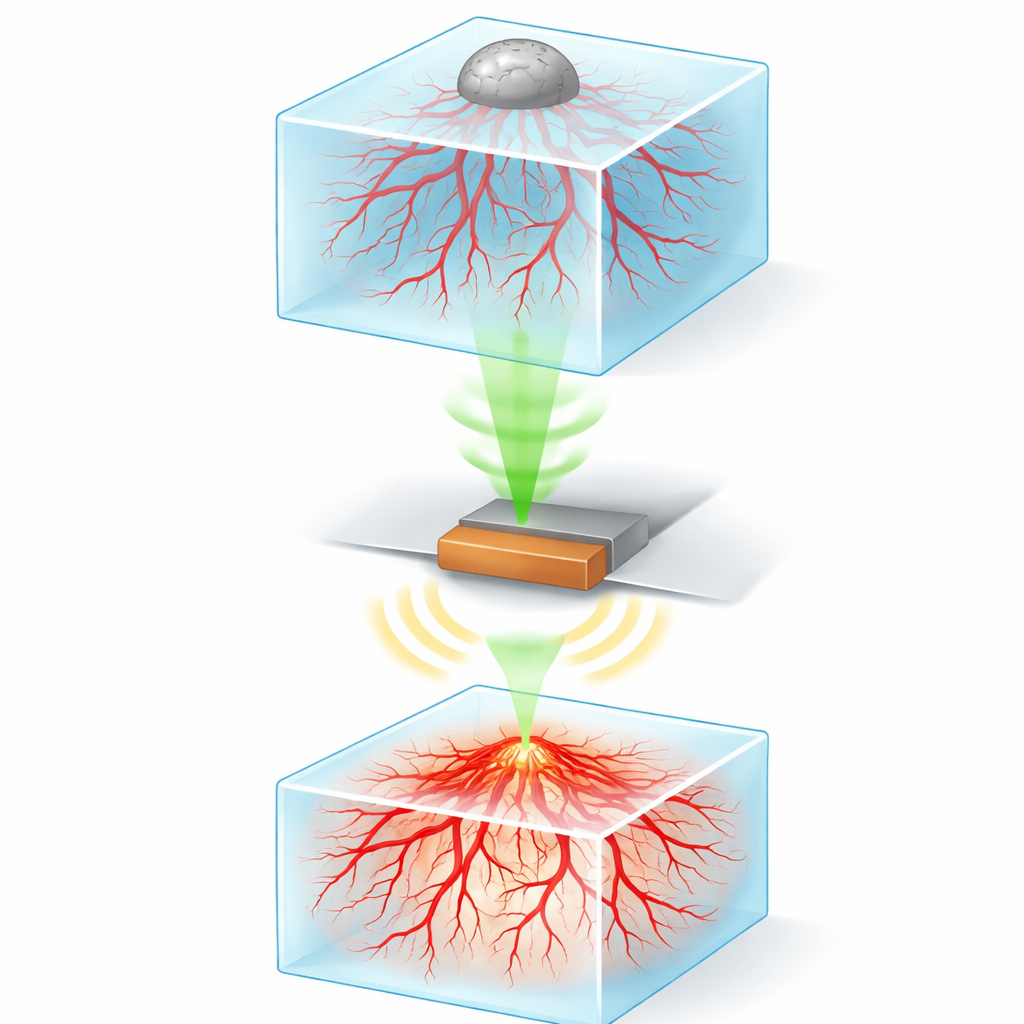
Создание мини-органов на чипе
Исследователи сначала создали правдоподобные модели рака размером с большой палец, используя 3D-биопечать. Они напечатали мягкие гидрогелевые блоки, загруженные клетками человеческих сосудов и поддерживающими клетками, чтобы на протяжении нескольких дней в геле естественным образом формировались крошечные капилляроподобные сети. На эти живые сосудистые слои аккуратно поместили кластеры клеток опухоли мозга (сфероиды опухоли). Со временем эти опухоли начали взаимодействовать с сосудами снизу, стимулируя рост новых отростков в их направлении, подобно тому, как это происходит в организме.
Слушая свет, чтобы увидеть глубже
Увидеть, что происходит глубоко в этих матовых, наполненных клетками гелях, для стандартных микроскопов сложно, потому что свет рассеивается и быстро затухает с глубиной. Команда решила эту проблему, используя высокоразрешающую фотоакустическую микроскопию. В этой технике короткие лазерные импульсы направляются в образец и поглощаются определёнными молекулами, вызывая небольшие быстрые расширения, которые порождают ультразвуковые волны. Маленький детектор улавливает эти волны, а компьютер реконструирует детальные трёхмерные изображения. Чтобы сделать видимыми сосуды и раковые клетки, исследователи использовали распространённый лабораторный краситель (MTT), который живые клетки превращают в тёмные кристаллы, сильно поглощающие лазерный свет и дающие чёткие сигналы по всему образцу.
Наблюдение роста сосудов в 3D
С этой установкой авторы показали, что их фотоакустическая система может видеть значительно глубже в биопечатной ткани, чем стандартный конфокальный микроскоп — приблизительно в 1,6 раза глубже, достигая почти миллиметра. Они отслеживали изменения сосудистых сетей в течение нескольких дней: сначала появлялись короткие, редкие веточки, затем они удлинялись, переплетались и формировали более длинные, сложные траектории. Цифровым отслеживанием каждой сосуда в трёх измерениях они количественно оценили, как средние и максимальные длины сосудов увеличивались со временем, подтверждая, что модель достоверно отражает постепенное формирование кровоснабжения, похожего на опухолевое.
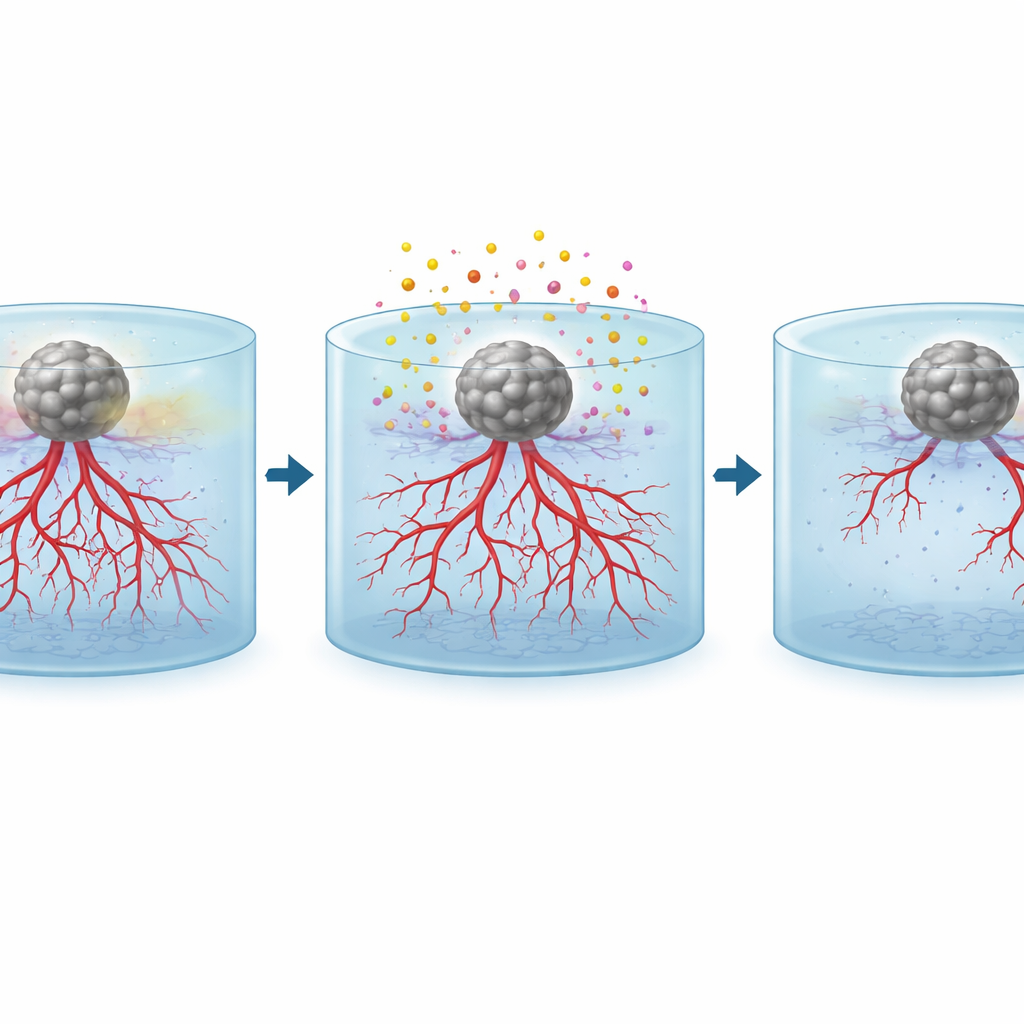
Тестирование противораковых препаратов в миниатюрной лаборатории
Реальная ценность платформы проявляется при тестировании лечебных средств. После того как сфероиды опухоли начали влиять на близлежащие сосуды, команда применяла два широко используемых противораковых препарата: темозоломид, который в основном наносит вред быстро делящимся опухолевым клеткам, и сунитиниб, который напрямую блокирует сигналы, стимулирующие рост сосудов. Их пробовали по отдельности и в комбинации. Фотоакустические изображения ясно показали, что по сравнению с необработанными образцами, наполненными плотными, расходящимися сосудистыми сетями, в образцах после применения препаратов сосудов стало меньше, они были короче и более фрагментированы, особенно вблизи опухолей. Комбинированная терапия дала наибольшее снижение плотности сосудов на всех глубинах, демонстрируя, что этот подход может измерять, как разные терапии изменяют опухоль‑индуцированный рост сосудов в 3D.
Что это значит для будущего онкологической помощи
Эта работа показывает, что возможно вырастить реалистичные трёхмерные системы «опухоль–сосуд» в лаборатории и затем неинвазивно «увидеть» их внутренние сети кровеносных сосудов с помощью звука, порождённого светом. Поскольку метод захватывает весь объём, а не только поверхность, он может выявлять, где и насколько эффективно препарат перекрывает кровоснабжение опухоли по всему образцу. В будущем аналогичные биопечатные конструкции, изготовленные из клеток самого пациента, могли бы помочь врачам сравнивать варианты лечения до их назначения, прокладывая путь к более быстрым, этичным и персонализированным тестам противораковой терапии.
Цитирование: Jo, Y., Han, S., Kye, H. et al. Photoacoustic microscopy reveals deep angiogenic responses in 3D bioprinted tumor–vessel models. Microsyst Nanoeng 12, 129 (2026). https://doi.org/10.1038/s41378-026-01243-y
Ключевые слова: ангиогенез опухоли, фотоакустическая микроскопия, 3D-биопечать, скрининг противораковых препаратов, визуализация сосудов