Clear Sky Science · nl
Fotoakoestische microscopie onthult diepe angiogene reacties in 3D-biogeprinte tumor–vaatmodellen
Waarom het belangrijk is in kleine tumoren te kijken
Kankertumoren groeien niet in isolatie; ze bouwen hun eigen levensader van bloedvaten om zuurstof en voedingsstoffen aan te voeren. Veel moderne geneesmiddelen proberen deze levensader af te snijden, maar het testen van de effectiviteit van zulke behandelingen berust meestal op diermodellen of platte cellagen in schaaltjes, elk met serieuze beperkingen. Deze studie presenteert een methode om miniatuur driedimensionale tumor–bloedvat‑systemen in het laboratorium te kweken en daarna diep in deze modellen te kijken zonder ze open te snijden, met een door geluid gebaseerde beeldvormingstechniek genaamd fotoakoestische microscopie.
Mini‑organen op een chip bouwen
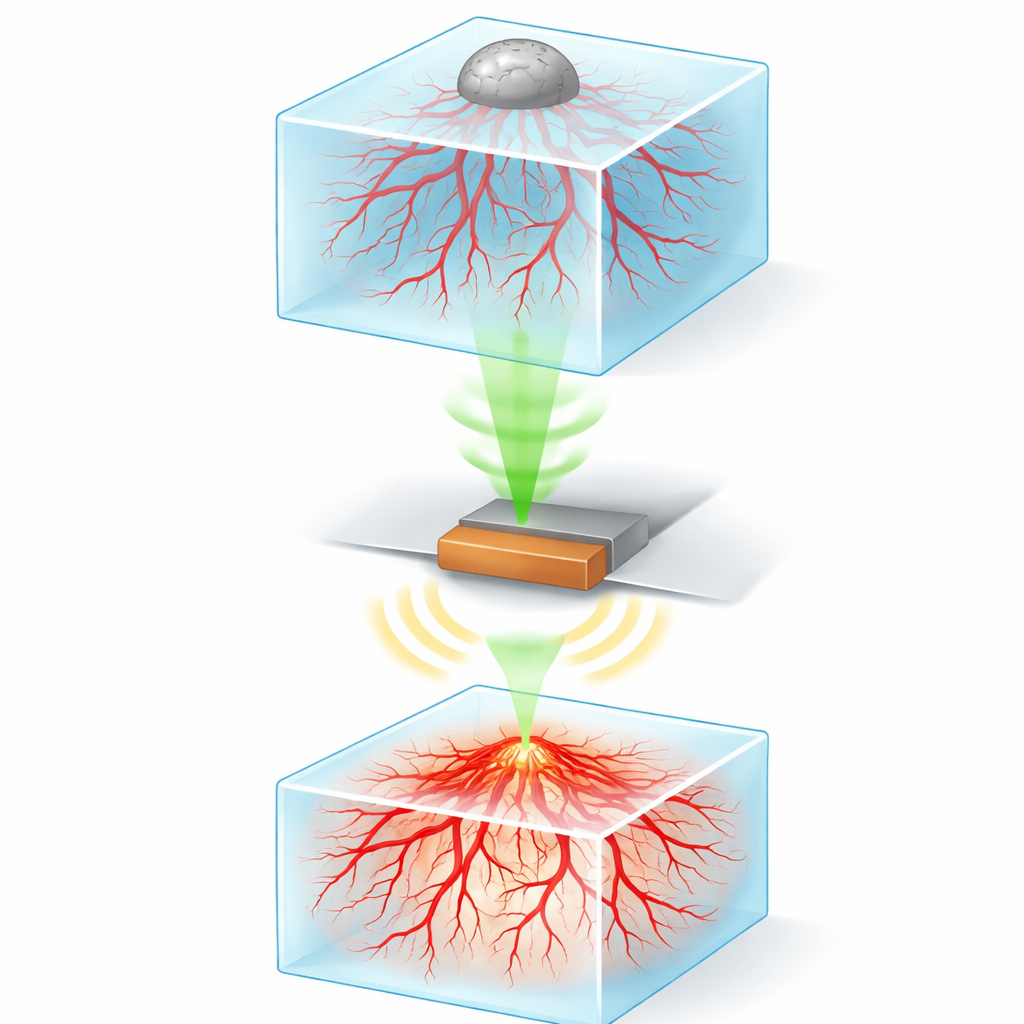
De onderzoekers maakten eerst realistische duimgrote kanker‑modellen met behulp van 3D‑bioprinten. Ze printten zachte hydrogelblokken geladen met menselijke bloedvatcellen en ondersteunende cellen, zodat kleine capillairachtige netwerken zich in de loop van enkele dagen vanzelf door de gel zouden vormen. Boven op deze levende vasculaire lagen plaatsten ze voorzichtig clusters van hersenkankercellen (tumorsferoïden). In de loop van de tijd begonnen deze tumoren te interageren met de vaten eronder en stimuleerden ze de groei van nieuwe uitlopers naar zich toe, vergelijkbaar met wat tumoren in het lichaam doen.
Luisteren naar licht om diep binnenin te zien
Zien wat er diep in deze troebele, celgevulde gels gebeurt is moeilijk voor standaardmicroscopen omdat licht wordt verstrooid en snel afneemt met de diepte. Het team loste dit op door gebruik te maken van fotoakoestische microscopie met hoge resolutie. Bij deze techniek schijnen korte laserpulsen in het weefsel en worden ze door bepaalde moleculen geabsorbeerd, wat kleine, snelle uitzettingen veroorzaakt die ultrageluidsgolven produceren. Een kleine detector vangt deze golven op en een computer reconstrueert gedetailleerde driedimensionale beelden. Om de vaten en kankercellen zichtbaar te maken, gebruikten de onderzoekers een veelgebruikt laboratoriumkleurstof (MTT) die levende cellen omzetten in donkere kristallen, die de laserstraling sterk absorberen en duidelijke signalen door het monster heen genereren.
Bloedvaten in 3D zien groeien
Met deze opstelling lieten de auteurs zien dat hun fotoakoestische systeem aanzienlijk dieper in het biogeprinte weefsel kon kijken dan een standaard confocale microscoop—ongeveer 1,6 keer dieper, bijna een millimeter bereikend. Ze volgden hoe de vaatnetwerken zich over meerdere dagen veranderden: eerst verschenen korte, spaarzame vertakkingen, daarna verlengden ze, raakten verstrengeld en vormden langere, meer complexe paden. Door elk vat digitaal in drie dimensies te traceren, kwantificeerden ze hoe gemiddelde en maximale vaatlengtes in de loop van de tijd toenamen, waarmee werd bevestigd dat het model trouw de geleidelijke opbouw van een tumorachtige bloedvoorziening vastlegt.
Kankermedicijnen testen in een miniatuur‑lab
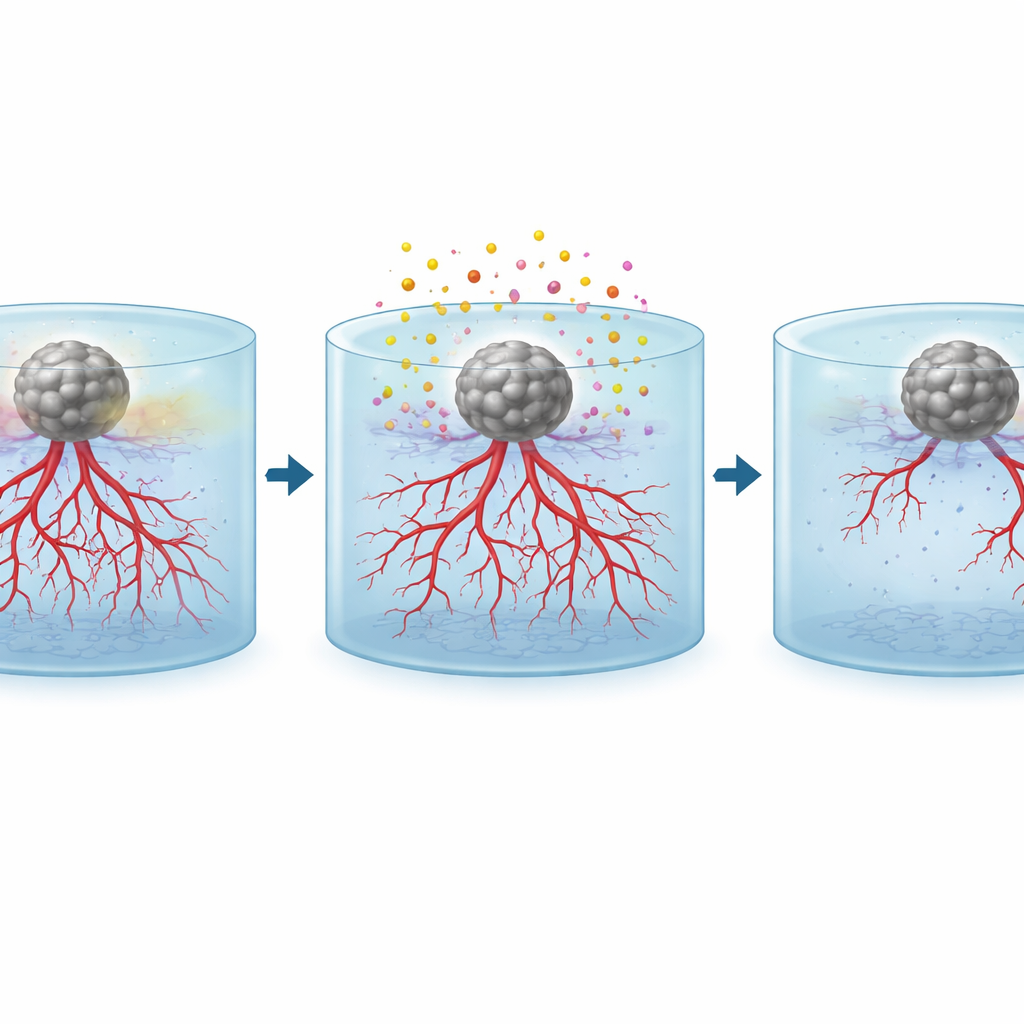
De echte kracht van het platform komt naar voren bij het testen van behandelingen. Nadat de tumorsferoïden begonnen invloed uit te oefenen op de nabije vaten, brachten de onderzoekers twee veelgebruikte anticancermiddelen aan: temozolomide, dat vooral snel delende tumorcellen schaadt, en sunitinib, dat rechtstreeks signalen voor vaatgroei blokkeert. Ze probeerden elk geneesmiddel afzonderlijk en in combinatie. Fotoakoestische beelden toonden duidelijk aan dat, vergeleken met onbehandelde monsters vol dichte, stralende vaatnetwerken, de geneesmiddelbehandelde monsters minder, kortere en meer gefragmenteerde vaten hadden, vooral in de buurt van de tumoren. De gecombineerde behandeling veroorzaakte de sterkste vermindering van vaatdichtheid op alle dieptes, wat aantoont dat deze benadering kan meten hoe verschillende therapieën door tumoren aangedreven vaatgroei in 3D veranderen.
Wat dit betekent voor toekomstige kankerzorg
Dit werk laat zien dat het mogelijk is realistische driedimensionale tumor–vaatsystemen in het laboratorium te kweken en vervolgens niet‑invasief hun interne bloedvatnetwerken te “zien” met geluid dat door licht wordt gegenereerd. Omdat de methode het gehele volume vastlegt, niet alleen het oppervlak, kan zij onthullen waar en hoe sterk een middel de bloedtoevoer van een tumor door het weefsel heen afsluit. In de toekomst zouden vergelijkbare biogeprinte constructen gemaakt van de eigen cellen van een patiënt artsen kunnen helpen behandelingsopties te vergelijken voordat ze worden toegepast, en zo de weg kunnen wijzen naar snellere, ethisch verantwoorde en meer gepersonaliseerde testen van kankertherapieën.
Bronvermelding: Jo, Y., Han, S., Kye, H. et al. Photoacoustic microscopy reveals deep angiogenic responses in 3D bioprinted tumor–vessel models. Microsyst Nanoeng 12, 129 (2026). https://doi.org/10.1038/s41378-026-01243-y
Trefwoorden: tumorangiogenese, fotoakoestische microscopie, 3D-bioprinten, kankermedicijnenscreening, vasculaire beeldvorming