Clear Sky Science · de
Photoakustische Mikroskopie zeigt tiefe angiogene Reaktionen in 3D-bioprinteten Tumor‑Gefäß‑Modellen
Warum es wichtig ist, in kleine Tumoren hineinzusehen
Krebstumoren wachsen nicht isoliert; sie bauen sich ein eigenes Versorgungsnetz aus Blutgefäßen auf, um Sauerstoff und Nährstoffe zu erhalten. Viele moderne Medikamente versuchen, diese Lebensader abzuschneiden, doch die Bewertung ihrer Wirksamkeit stützt sich meist auf Tierversuche oder zweidimensionale Zellkulturen, die jeweils erhebliche Nachteile haben. Diese Studie stellt eine Methode vor, mit der miniature drei‑dimensionale Tumor‑Gefäß‑Systeme im Labor gezüchtet und anschließend ohne Aufschneiden tief in ihr Inneres hineingesehen werden kann — mittels eines schallbasierten Bildgebungsverfahrens namens photoakustische Mikroskopie.
Mini‑Organe auf einem Chip bauen
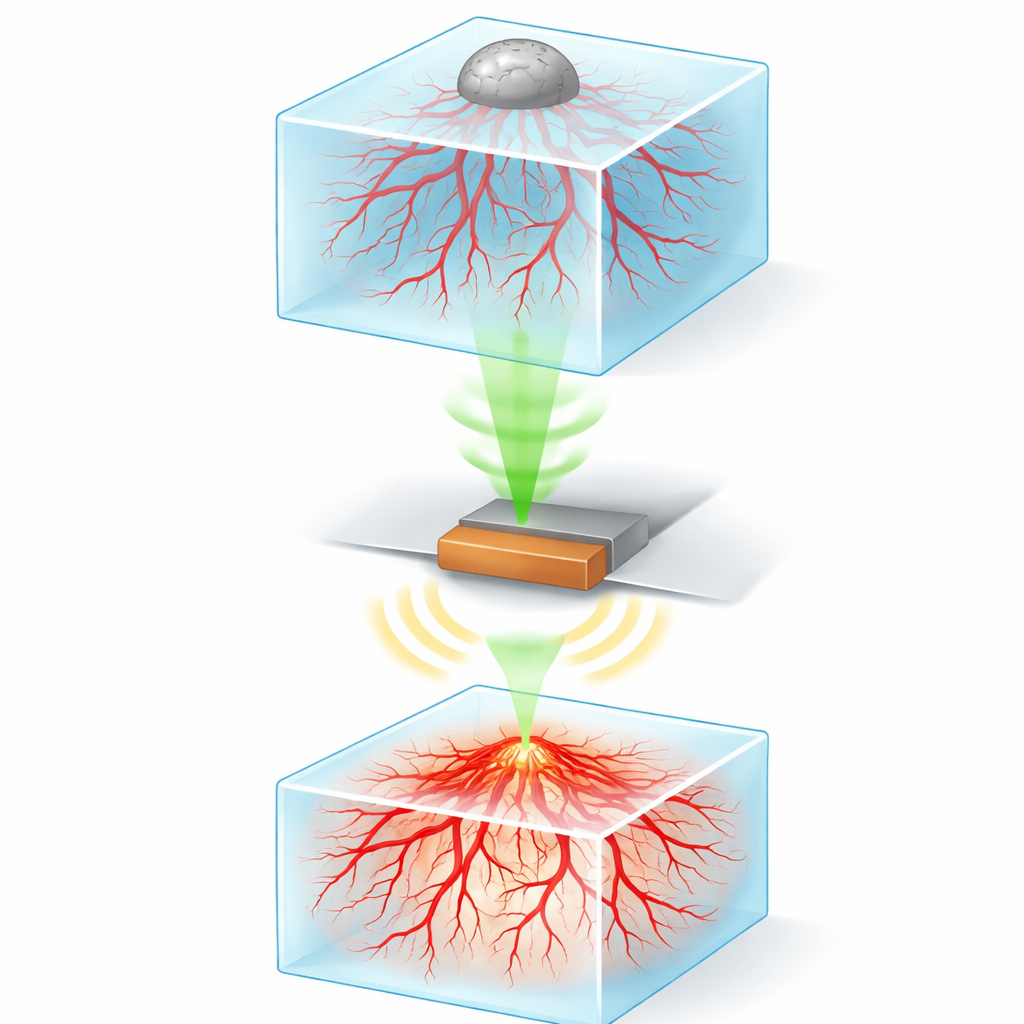
Die Forschenden erzeugten zunächst realistische, daumengroße Krebsmodelle mittels 3D‑Bioprinting. Sie druckten weiche Hydrogelblöcke, die mit menschlichen Gefäßzellen und Stütz‑Zellen beladen waren, sodass sich über mehrere Tage winzige kapillarähnliche Netzwerke im Gel von selbst ausbilden konnten. Auf diese lebenden Gefäßschichten legten sie behutsam Bündel von Hirnkrebszellen (Tumorsphäroide). Im Lauf der Zeit begannen diese Tumore mit den darunter liegenden Gefäßen zu interagieren und förderten das Wachstum neuer Sprossen in ihre Richtung, ähnlich wie Tumore es im Organismus tun.
Mit Licht hören, um tief hineinzusehen
Das, was tief im Inneren dieser trüben, zellgefüllten Gele passiert, ist für Standardmikroskope schwer sichtbar, weil Licht gestreut wird und mit der Tiefe schnell abnimmt. Das Team löste dieses Problem mit hochauflösender photoakustischer Mikroskopie. Bei dieser Technik senden kurze Laserpulse Licht in das Gewebe, das von bestimmten Molekülen absorbiert wird und so winzige, schnelle Ausdehnungen erzeugt, die Ultraschallwellen hervorrufen. Ein kleiner Detektor erfasst diese Wellen und ein Computer rekonstruiert daraus detaillierte dreidimensionale Bilder. Um Gefäße und Krebszellen sichtbar zu machen, nutzten die Forschenden einen gängigen Labofarbstoff (MTT), den lebende Zellen in dunkle Kristalle umwandeln, welche das Laserlicht stark absorbieren und im gesamten Probenvolumen klare Signale erzeugen.
Wachsendes Gefäßnetz in 3D beobachten
Mit diesem Aufbau zeigten die Autorinnen und Autoren, dass ihr photoakustisches System deutlich tiefer in das bioprintete Gewebe hineinsehen konnte als ein standardmäßiges konfokales Mikroskop — etwa 1,6‑mal tiefer und bis nahe an einen Millimeter. Sie verfolgten, wie sich die Gefäßnetzwerke über mehrere Tage veränderten: Zuerst erschienen kurze, spärliche Verzweigungen, dann verlängerten sie sich, verflochten sich und bildeten längere, komplexere Bahnen. Durch das digitale Nachzeichnen jedes Gefäßes in drei Dimensionen quantifizierten sie, wie mittlere und maximale Gefäßlängen im Zeitverlauf zunahmen, und bestätigten damit, dass das Modell den schrittweisen Aufbau einer tumorähnlichen Blutversorgung realistisch abbildet.
Krebsmedikamente in einem Mini‑Labor testen
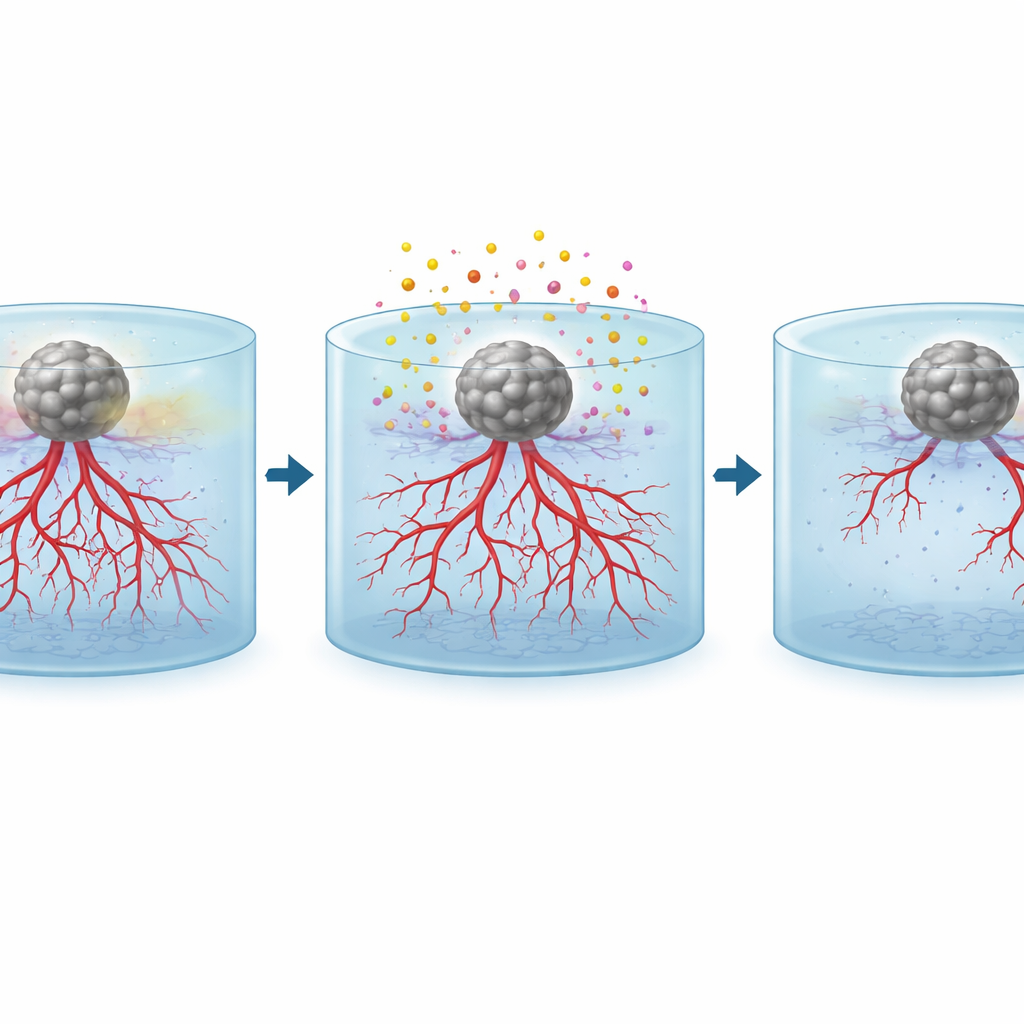
Die eigentliche Stärke der Plattform liegt in ihrer Nutzung zum Testen von Therapien. Nachdem sich die Tumorsphäroide bereits auf die umliegenden Gefäße ausgewirkt hatten, setzte das Team zwei weit verbreitete Krebsmedikamente ein: Temozolomid, das vor allem schnell teilende Tumorzellen schädigt, und Sunitinib, das gezielt Signalwege des Gefäßwachstums blockiert. Sie testeten jedes Medikament einzeln und in Kombination. Photoakustische Bilder zeigten deutlich, dass behandelte Proben im Vergleich zu unbehandelten Proben mit dichten, strahlenförmigen Gefäßnetzwerken weniger, kürzere und stärker fragmentierte Gefäße aufwiesen, besonders in Tumornähe. Die Kombinationstherapie bewirkte die stärkste Reduktion der Gefäßdichte in allen Tiefenbereichen und demonstrierte, dass dieser Ansatz messen kann, wie verschiedene Therapien das tumorgetriebene Gefäßwachstum in 3D verändern.
Was das für die zukünftige Krebsbehandlung bedeutet
Diese Arbeit zeigt, dass es möglich ist, realistische, dreidimensionale Tumor‑Gefäß‑Systeme im Labor zu züchten und ihre internen Gefäßnetzwerke nichtinvasiv mit schallgeneriertem Licht zu „sehen“. Da die Methode das gesamte Volumen erfasst und nicht nur die Oberfläche, kann sie offenlegen, wo und wie stark ein Medikament die Blutversorgung eines Tumors im Gewebe abschneidet. Künftig könnten ähnliche bioprintete Konstrukte aus den Zellen eines Patienten Ärztinnen und Ärzten helfen, Behandlungsoptionen vorab zu vergleichen — ein Schritt hin zu schnelleren, ethischeren und stärker personalisierten Tests von Krebstherapien.
Zitation: Jo, Y., Han, S., Kye, H. et al. Photoacoustic microscopy reveals deep angiogenic responses in 3D bioprinted tumor–vessel models. Microsyst Nanoeng 12, 129 (2026). https://doi.org/10.1038/s41378-026-01243-y
Schlüsselwörter: Tumorangiogenese, photoakustische Mikroskopie, 3D‑Bioprinting, Krebs‑Wirkstoffscreening, Gefäßbildgebung