Clear Sky Science · pl
Mikroskopia fotoakustyczna ujawnia głębokie angiogenne odpowiedzi w trójwymiarowych, biotłoczonych modelach nowotwór–naczynie
Dlaczego warto zaglądać do wnętrza maleńkich guzów
Guzy nowotworowe nie rosną w izolacji; tworzą własną sieć naczyń krwionośnych, by dostarczać tlen i składniki odżywcze. Wiele współczesnych terapii próbuje przeciąć tę życiodajną sieć, ale ocenianie skuteczności takich leków zwykle opiera się na modelach zwierzęcych lub na płaskich hodowlach komórkowych, z którymi wiążą się istotne ograniczenia. W tym badaniu przedstawiono sposób hodowli miniaturowych, trójwymiarowych układów guz–naczynie w laboratorium, a następnie ich nieinwazyjnego oglądania w głębi bez konieczności przecięcia, przy użyciu dźwiękowej techniki obrazowania zwanej mikroskopią fotoakustyczną.
Budowanie mini narządów na chipie
Naukowcy najpierw stworzyli realistyczne, wielkości kciuka modele nowotworowe przy użyciu biologicznego druku 3D. Wytwarzali miękkie bloki hydrożelu zawierające ludzkie komórki śródbłonka i komórki wspierające, tak aby w ciągu kilku dni w żelu naturalnie formowały się drobne sieci przypominające kapilary. Na tych żywych warstwach naczyniowych umieszczano z delikatnością skupiska komórek nowotworu mózgu (sferoidy guza). Z czasem guzy zaczynały wchodzić w interakcję z naczyńkami poniżej, pobudzając powstawanie nowych wypustek skierowanych ku nim, podobnie jak dzieje się to w organizmie.
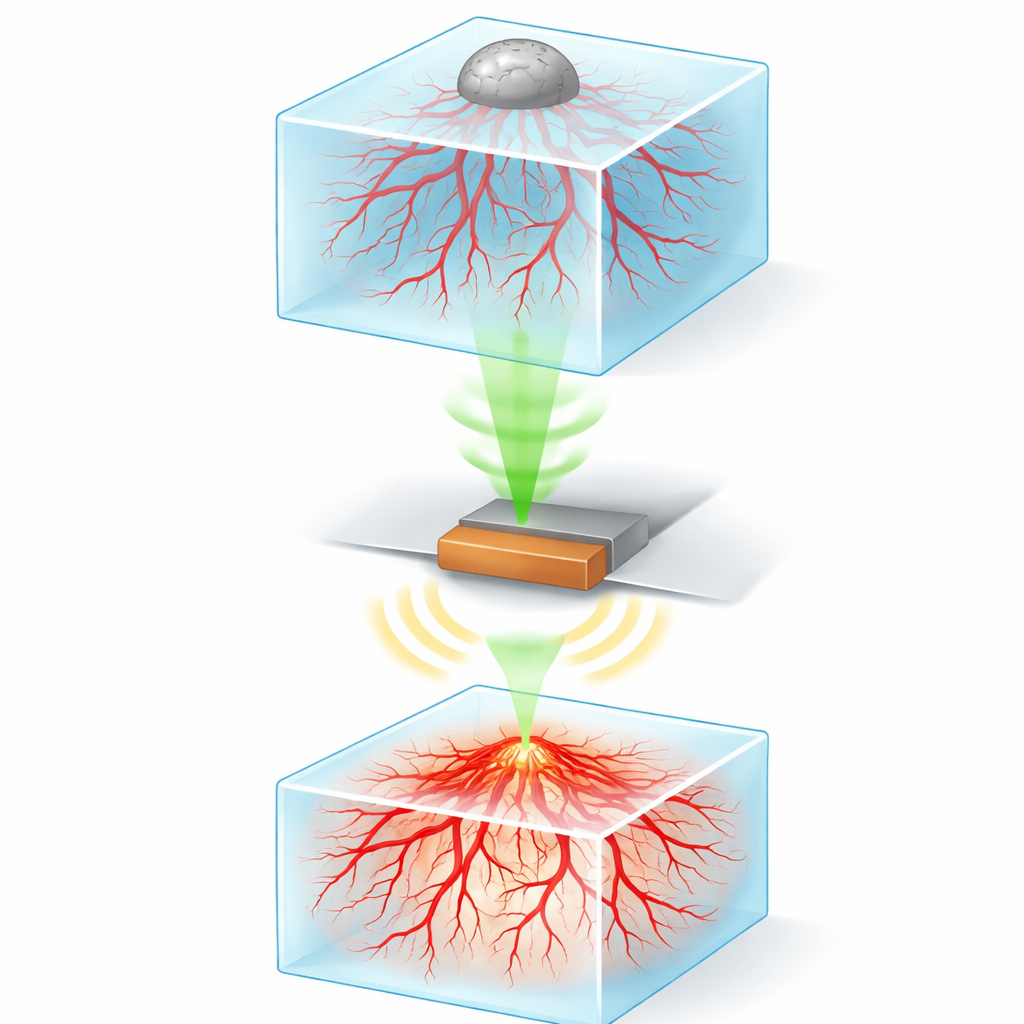
Słuchając światła, by zobaczyć w głębi
Obserwowanie tego, co dzieje się w gęstych, wypełnionych komórkami żelach, jest trudne dla standardowych mikroskopów, ponieważ światło ulega rozproszeniu i szybko traci intensywność wraz z głębokością. Zespół rozwiązał to, stosując mikroskopię fotoakustyczną o wysokiej rozdzielczości. W tej technice krótkie impulsy laserowe padają na tkankę i są pochłaniane przez określone cząsteczki, powodując drobne, szybkie rozszerzenia, które generują fale ultradźwiękowe. Mały detektor odbiera te fale, a komputer rekonstruuje szczegółowe obrazy trójwymiarowe. Aby uwidocznić naczynia i komórki nowotworowe, badacze użyli powszechnego barwnika laboratoryjnego (MTT), który żywe komórki przekształcają w ciemne kryształy, mocno absorbujące światło laserowe i generujące wyraźne sygnały w całej próbce.
Obserwowanie wzrostu naczyń w 3D
Dzięki tej konfiguracji autorzy pokazali, że ich system fotoakustyczny może widzieć znacznie głębiej w biotłoczony materiał niż standardowy mikroskop konfokalny — około 1,6 raza głębiej, sięgając niemal milimetra. Śledzili zmiany sieci naczyń przez kilka dni: początkowo pojawiały się krótkie, rzadkie odgałęzienia, potem wydłużały się, splatały i tworzyły dłuższe, bardziej złożone tory. Poprzez cyfrowe śledzenie każdej naczyniowej struktury w trzech wymiarach, ilościowo określili wzrost wartości średnich i maksymalnych długości naczyń w czasie, potwierdzając, że model wiernie odzwierciedla stopniowe budowanie się układu naczyń podobnego do guza.
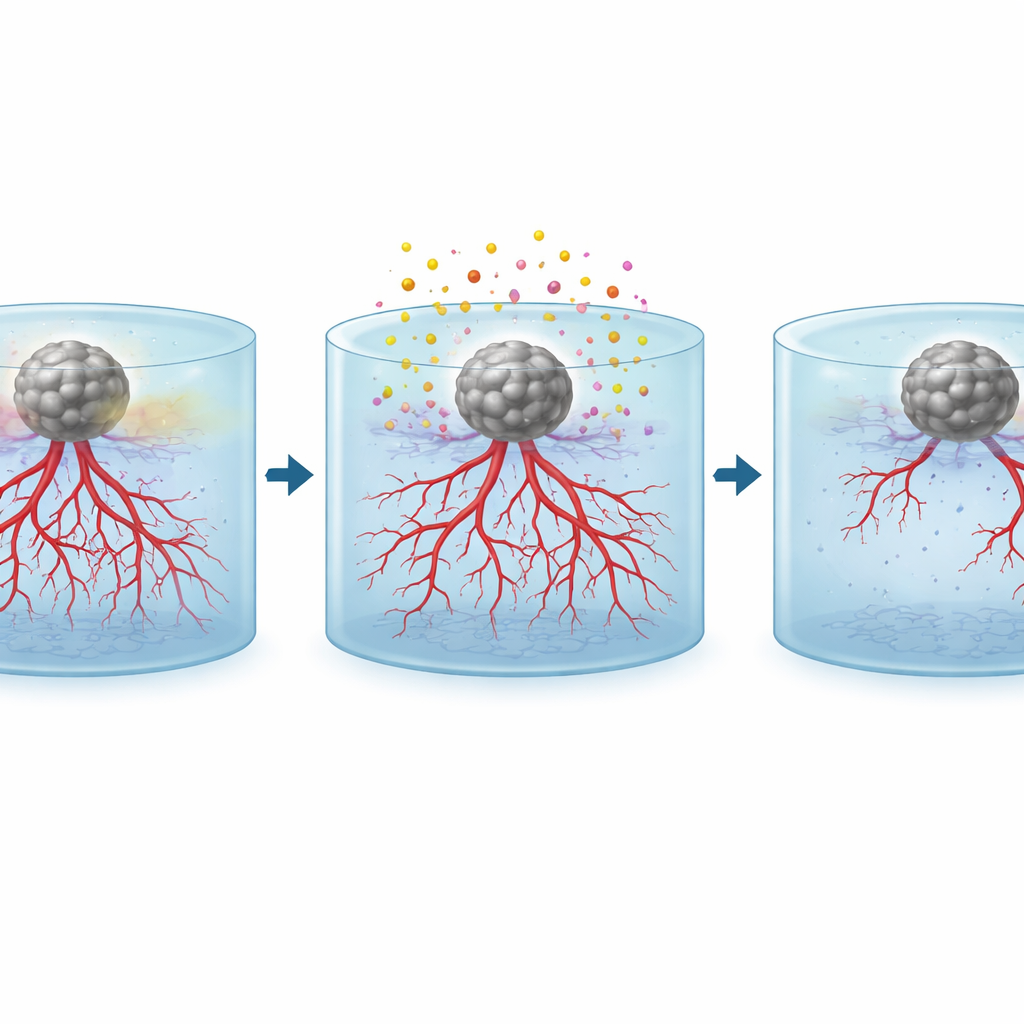
Testowanie leków przeciwnowotworowych w miniaturowym laboratorium
Rzeczywista siła platformy polega na wykorzystaniu jej do testowania terapii. Gdy sferoidy guza zaczęły wpływać na sąsiednie naczynia, zespół zastosował dwa szeroko stosowane leki przeciwnowotworowe: temozolomid, który głównie działa na szybko dzielące się komórki nowotworowe, oraz sunitynib, który bezpośrednio blokuje sygnały stymulujące wzrost naczyń. Przebadano każdy lek osobno i w połączeniu. Obrazy fotoakustyczne wyraźnie pokazały, że w porównaniu z nieleczonymi próbkami pełnymi gęstych, promieniujących sieci naczyń, próbki po leczeniu miały mniej, krótsze i bardziej fragmentaryczne naczynia, szczególnie w pobliżu guzów. Terapia skojarzona powodowała najsilniejsze zmniejszenie gęstości naczyń na wszystkich głębokościach, wykazując, że podejście to może mierzyć, jak różne terapie zmieniają napędzany przez guz wzrost naczyń w 3D.
Co to oznacza dla przyszłej opieki onkologicznej
Praca ta pokazuje, że możliwe jest hodowanie realistycznych, trójwymiarowych układów guz–naczynie w laboratorium, a następnie nieinwazyjne „zobrazowanie” ich wewnętrznych sieci naczyń przy użyciu dźwięku generowanego przez światło. Ponieważ metoda obejmuje całą objętość, nie tylko powierzchnię, może ujawniać, gdzie i jak silnie lek odcina dopływ krwi do guza w całej tkance. W przyszłości podobne biotłoczone konstrukty wykonane z komórek pacjenta mogłyby pomóc lekarzom porównywać opcje leczenia przed ich zastosowaniem, wskazując drogę ku szybszym, bardziej etycznym i bardziej spersonalizowanym testom terapii przeciwnowotworowych.
Cytowanie: Jo, Y., Han, S., Kye, H. et al. Photoacoustic microscopy reveals deep angiogenic responses in 3D bioprinted tumor–vessel models. Microsyst Nanoeng 12, 129 (2026). https://doi.org/10.1038/s41378-026-01243-y
Słowa kluczowe: angiogeneza nowotworu, mikroskopia fotoakustyczna, drukowanie 3D biologiczne, testowanie leków przeciwnowotworowych, obrazowanie naczyń