Clear Sky Science · ru
Многофункциональный волоконно-оптический тезаностический зонд для замкнутой петли фототермической терапии опухолей
Крошечное волокно, борющееся с скрытыми опухолями
Онкологи сталкиваются с упрямой задачей: как точно разрушить опухоли, спрятанные глубоко в теле, не делая больших разрезов и не повреждая соседнюю здоровую ткань. В этом исследовании представлен оптический зонд толщиной с волос, который может вводиться прямо в опухоль, нагревать её до фатальных температур и одновременно «слушать» химию и температуру опухоли в реальном времени. В результате получается инструмент замкнутой петли лечения, который находит края опухоли, применяет ровно столько тепла, сколько необходимо, и быстро оценивает, действует ли терапия.
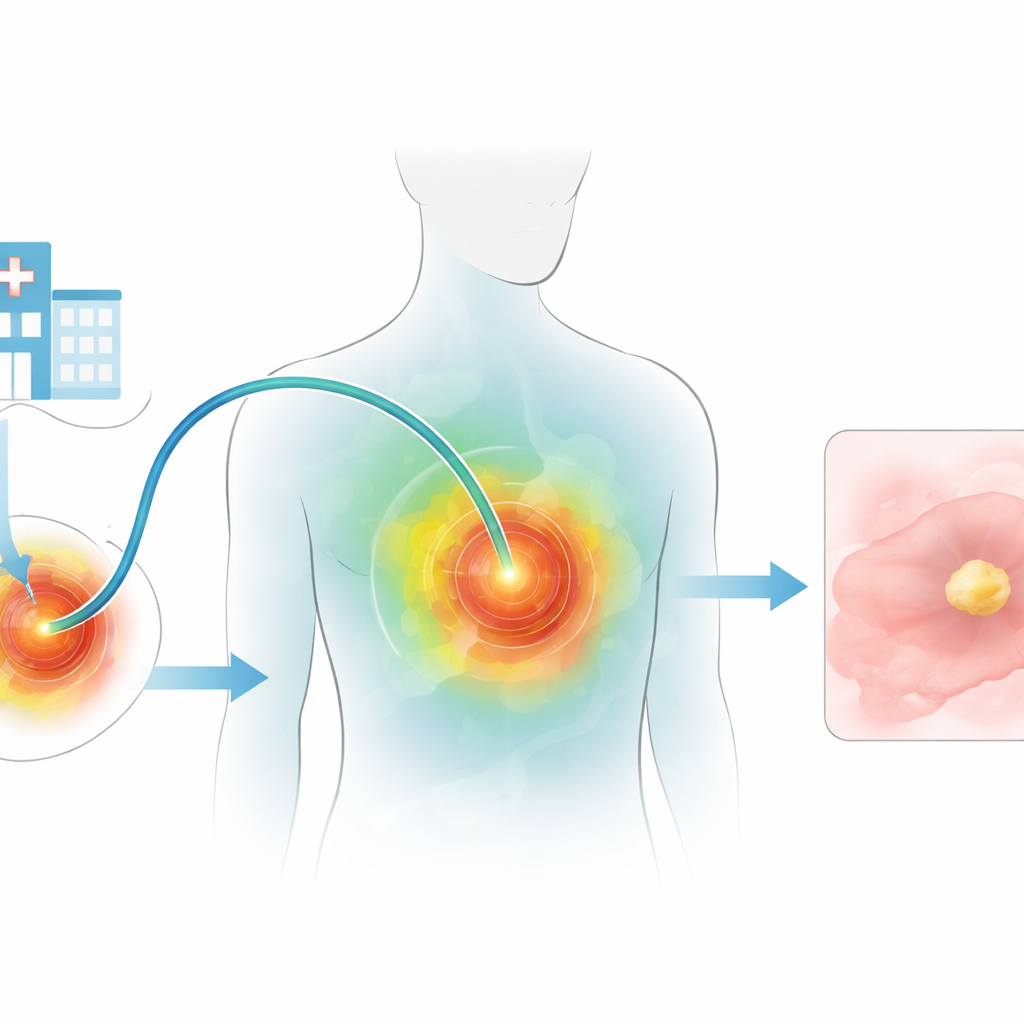
Почему нагревать опухоли сложно
Световые методы лечения рака обещают высокую локализацию повреждений опухоли, щадя остальное тело. Но свет плохо распространяется в ткани, и многие современные подходы зависят от наночастиц, циркулирующих по всему организму, что вызывает опасения по поводу долгосрочной токсичности. Существующие волоконные зонды обычно выполняют лишь одну функцию на волокно — либо лечат, либо контролируют — и часто требуют нескольких отдельных волокон, что означает большие разрезы, более жёсткие устройства и больше неудобств для пациентов. К тому же клиницисты редко получают живую обратную связь во время лечения, что затрудняет избегание недостаточного нагрева опухоли или перегрева здоровых тканей.
Одно волокно, которое видит, нагревает и проверяет
Исследователи решили эти проблемы, объединив три разных светочувствительных компонента на сужающемся кончике одного оптического волокна. Кончик, примерно толщиной с человеческий волос, покрыт тонким гидрогелевым слоем, содержащим: индикатор, чувствительный к pH, для картирования кислотности опухольного окружения; материал, чувствительный к температуре, для измерения локального нагрева; и краситель, преобразующий ближний инфракрасный свет в тепло для терапии. Важно, что каждый компонент реагирует на разный цвет света — стратегия, заимствованная из телекоммуникаций и называемая мультиплексированием по длине волны. Простым переключением входной длины волны врачи могут менять режимы волокна между измерением pH, считыванием температуры и нагревом, не создавая помех между сигналами.
«Прослушивание» химии опухоли
Многие опухоли создают вокруг себя кислую среду, и степень кислотности тесно связана с агрессивностью опухоли. pH-сенсор команды способен обнаруживать крошечные изменения кислотности — менее двух сотых единицы pH — в диапазоне, важном как для здоровой, так и для раковой ткани. У мышей с колоректальными опухолями зонд чётко различал опухолевую и нормальную ткань и даже мог определить, где опухоль кончается и начинается здоровая ткань, по изменению кислотности от центра к краю. После лечения тот же зонд отслеживал постепенный сдвиг в сторону меньшей кислотности, что указывало на более здоровое поведение ткани и служило ранним маркером эффективности терапии.
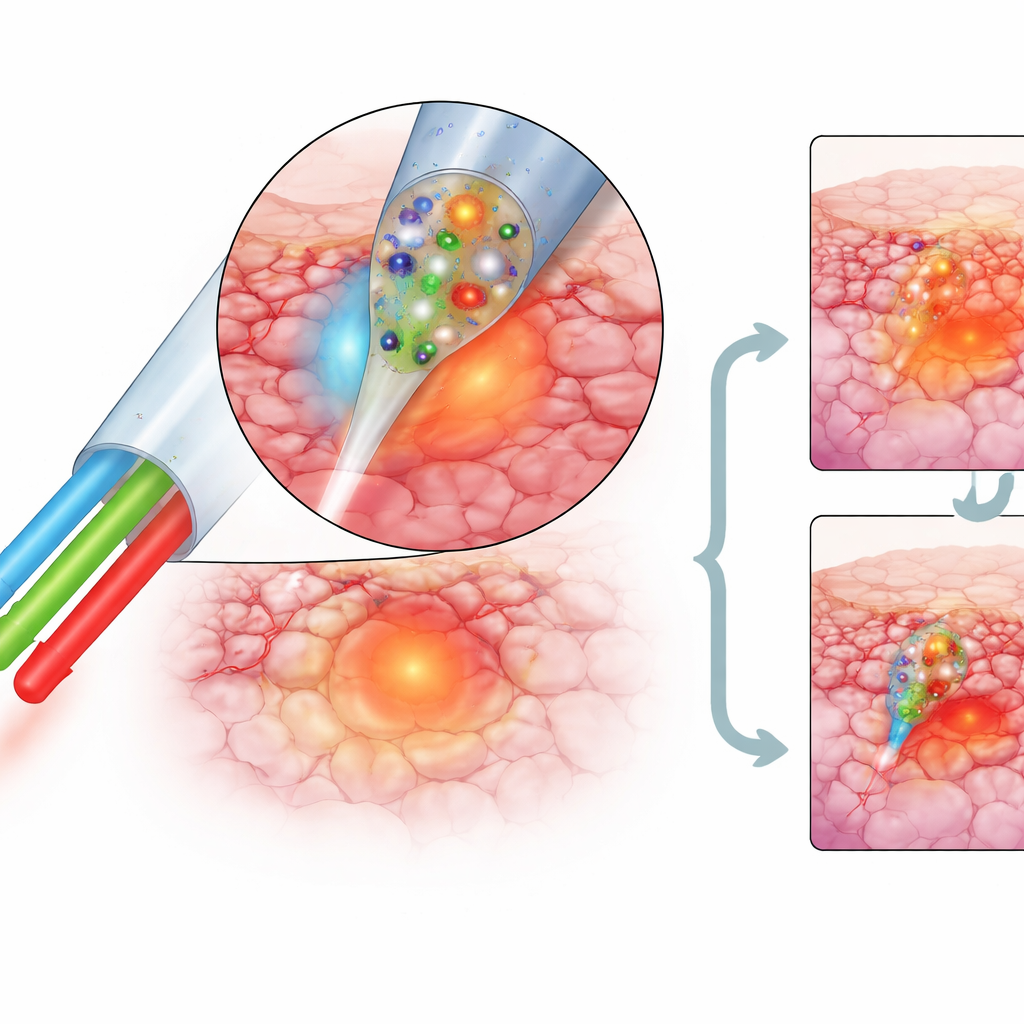
Умный нагрев с встроенным контролем температуры
Чтобы гарантировать уничтожение опухоли без повреждения соседних структур, зонд непрерывно измеряет собственную температуру. Специально разработанный светоизлучающий материал в покрытии меняет цветовой баланс по мере нагрева, что позволяет системе выводить температуру с точностью примерно до трети градуса Цельсия вблизи температуры тела и с ещё большей чувствительностью при более высоких лечебных температурах. Когда нагревательный краситель активируют инфракрасным лазером, подаваемым через то же волокно, кончик в лаборатории может достигать более 100 градусов Цельсия, затрачивая меньше энергии, чем многие системы на основе наночастиц. У живых мышей исследователи поддерживали волокно примерно на 65 градусах Цельсия в течение 15 минут — достаточно, чтобы наружные области опухоли достигли терапевтической температуры без очевидного вреда для животных.
Результаты в живых опухолях
В экспериментах на мышах этот подход замкнутой петли оказался и эффективным, и щадящим. До нагрева показания pH помогали локализовать опухоль и определить её границы. Во время лечения температурные данные зонда направляли дозирование нагрева. После лечения повторные измерения pH показали постепенное снижение кислотности, отражающее улучшение кровообращения и уменьшение числа активных раковых клеток. В последующие дни большинство обработанных опухолей уменьшились или исчезли, в то время как не леченные продолжали расти. Анализ тканей подтвердил широкое отмирание опухолевых клеток, снижение признаков гипоксии и уменьшение пролиферации клеток у обработанных животных, без серьёзных повреждений жизненно важных органов.
Что это может значить для пациентов
Проще говоря, авторы создали многофункционального «волоконного врача», который может найти опухоль, сжечь её изнутри светом и немедленно проверить, выполнена ли работа — и всё это через один очень маленький зонд. Поскольку система разделяет каждую функцию по цветам, в будущем можно будет добавить больше модулей диагностики и лечения без необходимости в дополнительных волокнах. Те же идеи конструкции можно адаптировать к более мягким, гибким волокнам для длительных имплантов. При дальнейшем развитии для клинического применения эта технология может обеспечить более точные, менее инвазивные методы лечения рака с обратной связью в реальном времени, помогая врачам подстраивать терапию под каждого пациента и минимизировать побочный ущерб.
Цитирование: Li, Z., Li, Z., Cheng, Z. et al. Multifunctional fiber-optic theranostic probe for closed-loop tumor photothermal therapy. Light Sci Appl 15, 216 (2026). https://doi.org/10.1038/s41377-026-02219-3
Ключевые слова: волоконно-оптическая терапия рака, фототермическая аблация опухолей, рН микроокружения опухоли, минимально инвазивные тезаностические подходы, измерение температуры в реальном времени