Clear Sky Science · ar
مسبار ثَرَانُوسْتِيكي ألياف بصري متعدد الوظائف للعلاج الضوئي الحراري للسرطان بنظام إغلاق الحلقة
ألياف دقيقة تقاتل الأورام الخفية
يواجه أخصائيو السرطان مشكلة صعبة: كيف يدمرون بدقة الأورام المدفونة عميقًا في الجسم من دون شقوق كبيرة أو إلحاق الضرر بالأنسجة السليمة المجاورة. تقدم هذه الدراسة مسبار ألياف بصري نحيف كالشعر يمكن إدخاله مباشرة إلى الورم، وتسخينه إلى درجات قاتلة، وفي الوقت نفسه «الاستماع» إلى كيمياء الورم وحرارته في الزمن الحقيقي. النتيجة أداة علاج بنظام إغلاق الحلقة قادرة على تحديد حواف الورم، وتطبيق قدر كافٍ من الحرارة، وتقييم بسرعة ما إذا كان العلاج ينجح.
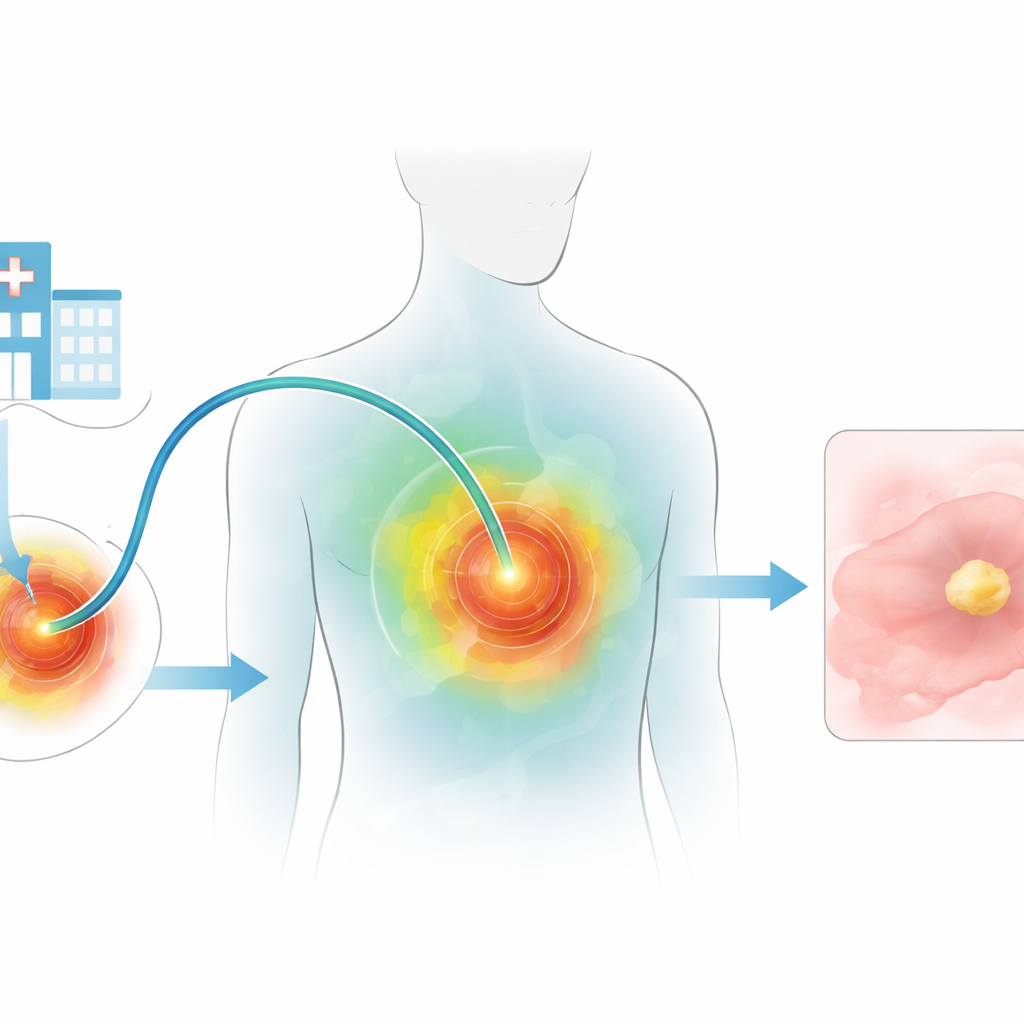
لماذا تسخين الأورام صعب
توعد العلاجات الضوئية بإحداث ضرر موضعي شديد للأورام مع الحفاظ على بقية الجسم. لكن الضوء لا ينتقل لمسافات طويلة داخل الأنسجة، وتعتمد العديد من الطرق الحالية على جزيئات نانوية تتداول في الجسم بأكمله، مما يثير مخاوف بشأن السمية طويلة الأمد. عادةً ما تقوم المجسات الليفية الحالية بمهمة واحدة فقط لكل ليف—إما علاج أو استشعار—وغالبًا ما تتطلب أليافًا متعددة منفصلة، مما يعني شقوقًا أكبر، وأجهزة أكثر صلابة، ومضايقة أكبر للمرضى. نادرًا ما يحصل الأطباء على ملاحظات مباشرة أثناء العلاج، ما يصعّب تجنب التسخين غير الكافي للورم أو التسخين المفرط للأنسجة السليمة.
ليف واحد يرى ويسخن ويتحقق
واجه الباحثون هذه التحديات بتجميع ثلاثة مكونات حساسة للضوء على طرف مخروطي لليف بصري واحد. الطرف، بعرض يقارب شعر الإنسان، مغطى بطبقة هلامية رقيقة تحتوي على: صبغة حساسة للحموضة لقياس حموضة وسط الورم، ومواد حساسة لدرجة الحرارة لقراءة الحرارة المحلية، وصبغة تحول الضوء القريب من تحت الحمراء إلى حرارة للعلاج. والأهم أن كل مكوّن يستجيب لطول موجي مختلف من الضوء، استراتيجية مقتبسة من الاتصالات تُعرف بتقسيم الموجة الطيفي. بتغيير طول الموجة الوارد ببساطة، يمكن للأطباء تبديل نفس الليف بين استشعار الحموضة، واستشعار الحرارة، والتسخين دون تداخل الإشارات.
الاستماع لكيمياء الورم
تخلق العديد من الأورام وسطًا حمضيًا حول نفسها، وترتبط درجة الحموضة ارتباطًا وثيقًا بشدة العدوانية. يستطيع مستشعر الحموضة للفريق اكتشاف تغيّرات ضئيلة في الحموضة—أصغر من اثنين من مئات وحدة pH—ضمن النطاق المهم للأنسجة السليمة والسرطانية على حد سواء. في فئران مصابة بأورام القولون والمستقيم، مكن المسبار من تمييز نسيج الورم بوضوح عن النسيج الطبيعي، وحتى تحديد نهاية الورم وبداية النسيج السليم بناءً على تغير الحموضة من المركز إلى الحافة. بعد العلاج، تعقب نفس المسبار تغيرًا تدريجيًا نحو ظروف أقل حمضية، ما يشير إلى تحسّن في سلوك النسيج ويعد علامة مبكرة على فاعلية العلاج.
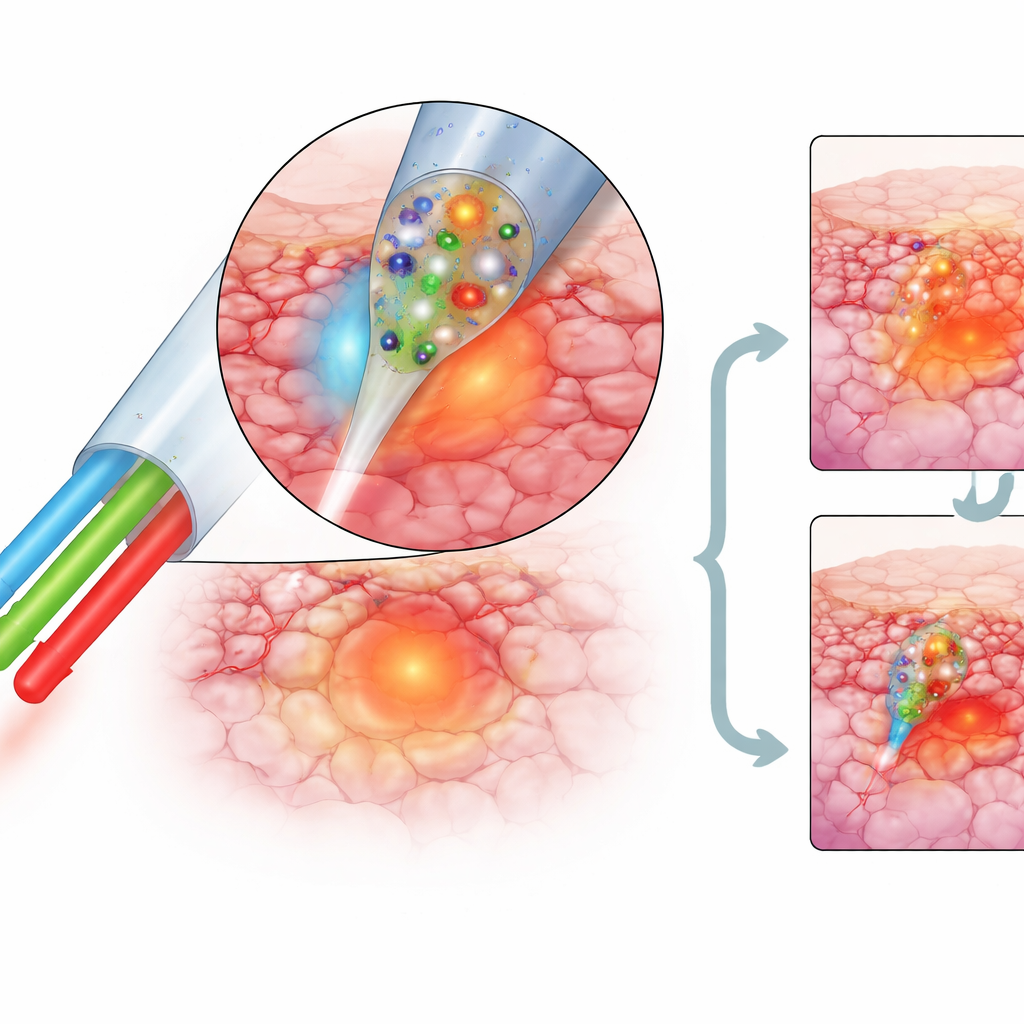
تسخين ذكي مع تحكّم حراري مدمج
لضمان تدمير الورم من دون الإضرار بالهياكل المجاورة، يقيس المسبار درجة حرارته باستمرار. مادة باعثة للضوء مصممة داخل الطلاء تغير توازن ألوانها عند الدفء، مما يسمح للنظام باستنتاج درجة الحرارة بدقة تقارب ثلث درجة مئوية قرب حرارة الجسم وبحساسية أعلى عند درجات علاجية أعلى. عندما تُشغَّل صبغة التسخين بواسطة ليزر تحت أحمر يُرسل عبر نفس الليف، يمكن للطرف الوصول إلى أكثر من 100 درجة مئوية في المختبر باستخدام طاقة أقل مما تتطلبه أنظمة الجسيمات النانوية كثيرًا. في الفئران الحية، حافظ الباحثون على الليف عند نحو 65 درجة مئوية لمدة 15 دقيقة، ما يكفي للوصول بمناطق الورم الخارجية إلى حرارة علاجية دون ضرر واضح للحيوانات.
النتائج داخل الأورام الحية
في تجارب على الفئران، أثبت النهج بنظام الإغلاق الحلقة فعاليته ولطفه معًا. قبل التسخين، ساعدت قراءات الحموضة في تحديد موقع الورم وتعريف حدوده. أثناء العلاج، وجهت قراءة درجة حرارة المسبار جرعة التسخين. بعد العلاج، أظهرت قياسات الحموضة المتكررة تقلصًا ثابتًا في الحمضية، يعكس تحسّنًا في تدفق الدم وقلة في الخلايا السرطانية النشطة. خلال الأيام التالية، انكمش معظم الأورام المعالجة أو اختفى، بينما استمرت الأورام غير المعالجة في النمو. أكدت تحليلات الأنسجة موتًا واسع النطاق للخلايا الورمية، وانخفاض مؤشرات الحرمان من الأكسجين، وتراجع تكاثر الخلايا في الحيوانات المعالجة، من دون ضرر كبير في الأعضاء الحيوية.
ماذا قد يعني هذا للمرضى
بعبارات بسيطة، بنى المؤلفون «طبيبًا أليافيًا» متعدد الوظائف يمكنه إيجاد الورم، وحرقه من الداخل بالضوء، والتحقق فورًا مما إذا تمت المهمة—كل ذلك عبر مسبار واحد صغير جدًا. وبما أن النظام يفصل كل وظيفة حسب اللون، يمكن إضافة مزيد من وحدات الاستشعار والعلاج مستقبلًا من دون الحاجة إلى ألياف إضافية. يمكن أيضًا ترجمة نفس أفكار التصميم إلى ألياف ألطف وأكثر مرونة للزرعات طويلة الأمد. إذا طُوِّرت هذه التقنية للاستخدام البشري، فقد تمكّن علاجات سرطانية أدق وأقل توغلاً مع ملاحظات في الزمن الحقيقي، مما يساعد الأطباء على تخصيص العلاج لكل مريض مع تقليل الأضرار الجانبية.
الاستشهاد: Li, Z., Li, Z., Cheng, Z. et al. Multifunctional fiber-optic theranostic probe for closed-loop tumor photothermal therapy. Light Sci Appl 15, 216 (2026). https://doi.org/10.1038/s41377-026-02219-3
الكلمات المفتاحية: علاج السرطان بالألياف الضوئية, استئصال الأورام بالحرارة الضوئية, حموضة وسط الورم, ثَرَانُوسْتيك جراحي طفيف التوغل, استشعار درجة الحرارة في الزمن الحقيقي