Clear Sky Science · de
Multifunktionale faseroptische Theranostiksonde für geschlossenes Photothermtherapie-Protokoll bei Tumoren
Eine winzige Faser gegen verborgene Tumoren
Krebsmediziner stehen vor einem hartnäckigen Problem: Wie zerstört man präzise Tumore, die tief im Körper liegen, ohne große Schnitte zu machen oder gesundes Gewebe in der Nähe zu schädigen? Diese Studie stellt eine haarfeine optische Faser vor, die direkt in einen Tumor eingeführt werden kann, ihn auf tödliche Temperaturen erhitzt und gleichzeitig in Echtzeit die Chemie und Temperatur des Tumors „abhört“. Das Ergebnis ist ein geschlossenes Behandlungswerkzeug, das Tumorgrenzen finden, genau die richtige Hitze anwenden und rasch beurteilen kann, ob die Therapie wirkt.
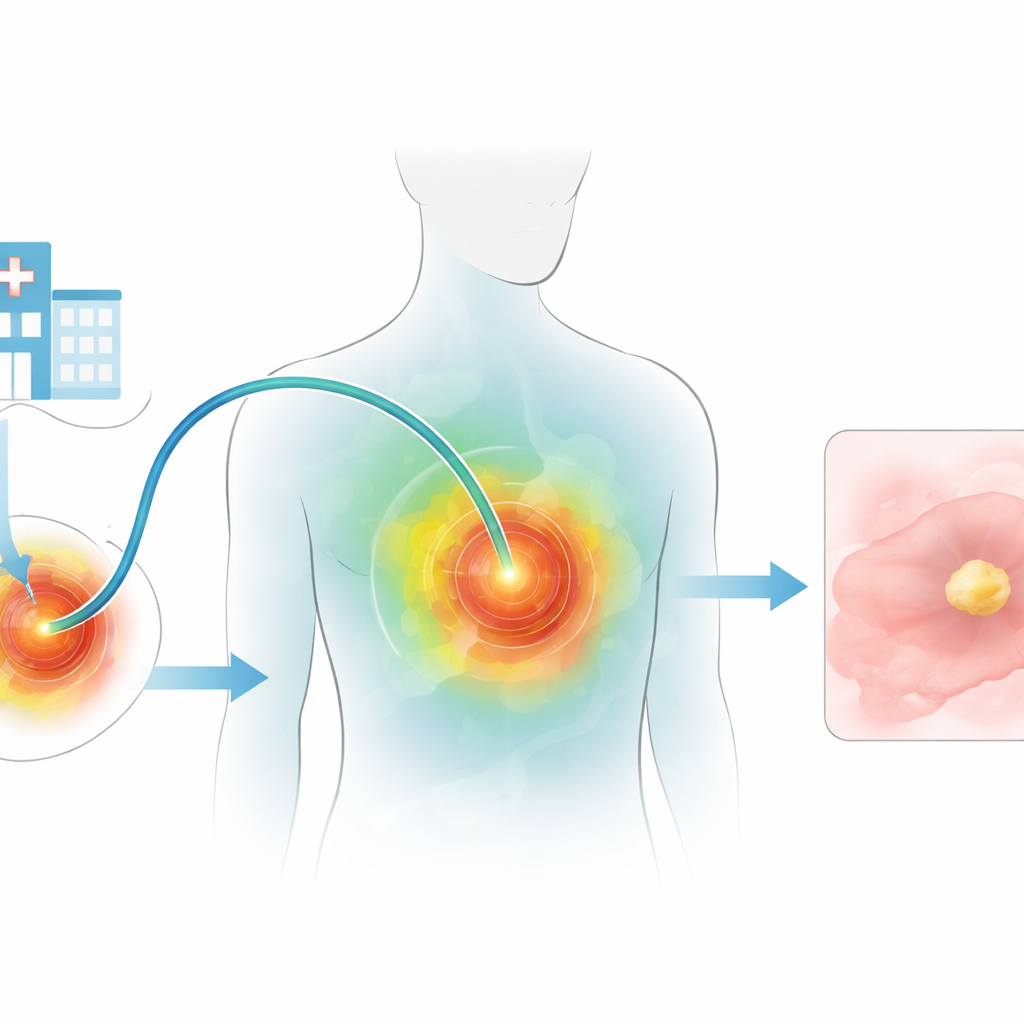
Warum das Erhitzen von Tumoren schwierig ist
Lichtbasierte Krebstherapien versprechen stark lokalisierte Schädigung von Tumoren und Schonung des übrigen Körpers. Licht dringt jedoch nicht weit durch Gewebe, und viele der aktuellen Verfahren setzen auf Nanopartikel, die im Körper zirkulieren und Bedenken bezüglich langfristiger Toxizität aufwerfen. Bestehende Fasersonden erfüllen meist nur eine Aufgabe pro Faser – entweder Behandlung oder Messung – und erfordern oft mehrere separate Fasern, was größere Einschnitte, steifere Vorrichtungen und mehr Unannehmlichkeiten für Patienten bedeutet. Kliniker erhalten zudem selten Live-Feedback während der Behandlung, was es schwer macht, Unterhitzung des Tumors oder Überhitzung von gesundem Gewebe zu vermeiden.
Eine einzige Faser, die sieht, erhitzt und prüft
Die Forscher begegneten diesen Herausforderungen, indem sie drei verschiedene lichtempfindliche Komponenten auf die verjüngte Spitze einer einzigen optischen Faser aufbrachten. Die Spitze, nur so dick wie ein menschliches Haar, ist mit einer dünnen Hydrogel-Schicht beschichtet, die enthält: einen pH-empfindlichen Farbstoff zur Kartierung der Säure im Tumormilieu, ein temperaturempfindliches Material zur lokalen Temperaturablesung und einen Farbstoff, der nahinfrarotes Licht in Wärme für die Therapie umwandelt. Entscheidend ist, dass jede Komponente auf eine andere Lichtfarbe reagiert – eine Strategie aus der Telekommunikation, bekannt als Wellenlängenmultiplex. Durch einfaches Wechseln der Eingangs-wellenlänge können Ärzte dieselbe Faser zwischen pH-Messung, Temperaturmessung und Erhitzung umschalten, ohne dass die Signale sich gegenseitig stören.
Der Chemie des Tumors zuhören
Viele Tumoren schaffen eine saure Umgebung um sich herum, und das Ausmaß der Säure ist eng mit ihrer Aggressivität verknüpft. Der pH-Sensor des Teams kann winzige Verschiebungen der Säure erkennen – kleiner als zwei Hundertstel pH-Einheiten – im Bereich, der sowohl für gesundes als auch für krebsartiges Gewebe relevant ist. In Mäusen mit kolorektalen Tumoren unterschied die Sonde klar Tumorgewebe von normalem Gewebe und konnte sogar das Ende des Tumors und den Beginn gesunden Gewebes anhand der Veränderung der Säure vom Zentrum zur Peripherie bestimmen. Nach der Behandlung verfolgte dieselbe Sonde eine allmähliche Verschiebung zu weniger sauren Bedingungen, was auf gesünderes Gewebeverhalten hindeutet und einen frühen Marker dafür liefert, dass die Therapie Wirkung zeigt.
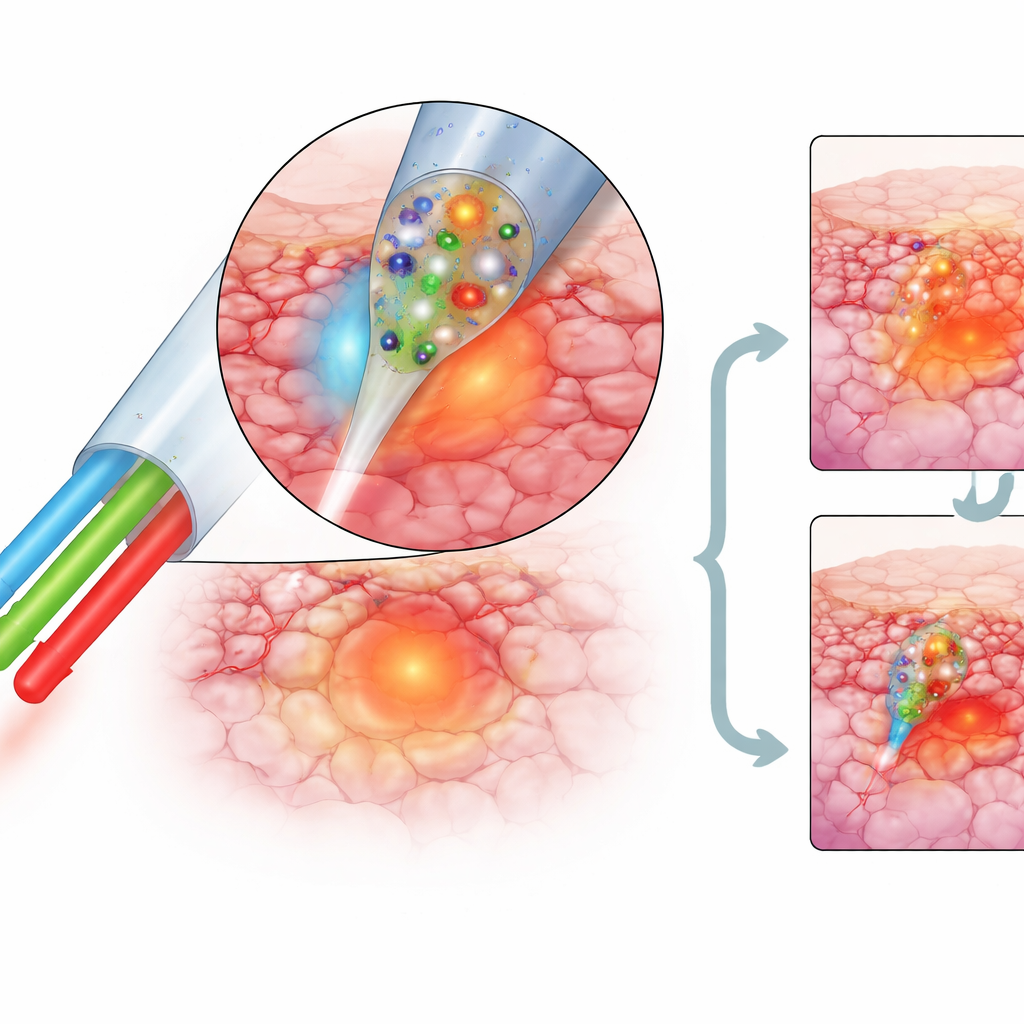
Intelligentes Erhitzen mit integrierter Temperaturkontrolle
Um sicherzustellen, dass der Tumor zerstört wird, ohne benachbarte Strukturen zu schädigen, misst die Sonde kontinuierlich ihre eigene Temperatur. Ein speziell entwickeltes lichtemittierendes Material in der Beschichtung verändert sein Farbverhältnis beim Erwärmen, sodass das System die Temperatur mit einer Genauigkeit von etwa einem Drittel Grad Celsius in Körpertemperaturbereichen ableiten kann und bei höheren Behandlungstemperaturen noch empfindlicher ist. Wenn der Heizfarbstoff durch einen infraroten Laser aktiviert wird, der durch dieselbe Faser geführt wird, kann die Spitze im Labor mit weniger Leistung als viele Nanopartikelsysteme mehr als 100 Grad Celsius erreichen. In lebenden Mäusen hielten die Forscher die Faser bei etwa 65 Grad Celsius für 15 Minuten, was ausreichte, damit die äußeren Tumorregionen therapeutische Temperaturen erreichten, ohne offensichtliche Schäden an den Tieren zu verursachen.
Ergebnisse in lebenden Tumoren
In Mausversuchen erwies sich dieser Closed-Loop-Ansatz als wirksam und schonend. Vor dem Erhitzen halfen die pH-Messungen, den Tumor zu lokalisieren und seine Grenzen zu definieren. Während der Behandlung leitete die Temperaturablesung der Sonde die Heizdosis. Danach zeigten wiederholte pH-Messungen eine stetige Verringerung der Säure, was auf verbesserte Durchblutung und weniger aktive Krebszellen hindeutete. In den folgenden Tagen schrumpften oder verschwanden die meisten behandelten Tumoren, während unbehandelte Tumoren weiter wuchsen. Gewebeanalysen bestätigten weitverbreiteten Tumorzelltod, reduzierte Anzeichen von Sauerstoffmangel und niedrigere Zellproliferation bei behandelten Tieren, ohne größere Schäden in lebenswichtigen Organen festzustellen.
Was das für Patienten bedeuten könnte
Kurz gesagt: Die Autoren haben einen multifunktionalen „Faserarzt“ entwickelt, der einen Tumor finden, ihn von innen mit Licht verbrennen und sofort prüfen kann, ob die Behandlung erfolgreich war – alles durch eine einzige, sehr kleine Sonde. Da das System jede Funktion nach Farbe trennt, könnten künftig weitere Mess- und Behandlungsmodule hinzugefügt werden, ohne zusätzliche Fasern zu benötigen. Dieselben Konstruktionsprinzipien ließen sich auf weichere, flexiblere Fasern für langfristige Implantate übertragen. Bei weiterer Entwicklung für den Menschen könnte diese Technologie präzisere, weniger invasive Krebstherapien mit Echtzeit-Feedback ermöglichen, sodass Kliniker die Therapie für jeden Patienten besser anpassen und gleichzeitig Kollateralschäden minimieren.
Zitation: Li, Z., Li, Z., Cheng, Z. et al. Multifunctional fiber-optic theranostic probe for closed-loop tumor photothermal therapy. Light Sci Appl 15, 216 (2026). https://doi.org/10.1038/s41377-026-02219-3
Schlüsselwörter: faseroptische Krebstherapie, photothermale Tumorablation, Tumormikroumgebung pH, minimalinvasive Theranostik, Echtzeit-Temperaturmessung