Clear Sky Science · pl
Wielofunkcyjna włókno-optyczna sonda theranostyczna do zamkniętej pętli fototermicznej terapii nowotworów
Małe włókno walczące z ukrytymi guzami
Specjaliści onkologii stoją przed uporczywym problemem: jak precyzyjnie zniszczyć guzy głęboko osadzone w ciele bez wykonywania dużych nacięć i uszkadzania otaczających zdrowych tkanek. W badaniu tym przedstawiono cienką jak włos sondę optyczną, która może wślizgnąć się bezpośrednio do guza, podgrzać go do śmiertelnych temperatur, a jednocześnie „nasłuchiwać” chemii i temperatury guza w czasie rzeczywistym. Efektem jest narzędzie leczenia w zamkniętej pętli, które potrafi wykryć granice guza, zastosować dokładnie tyle ciepła, ile potrzeba, i szybko ocenić, czy terapia działa.
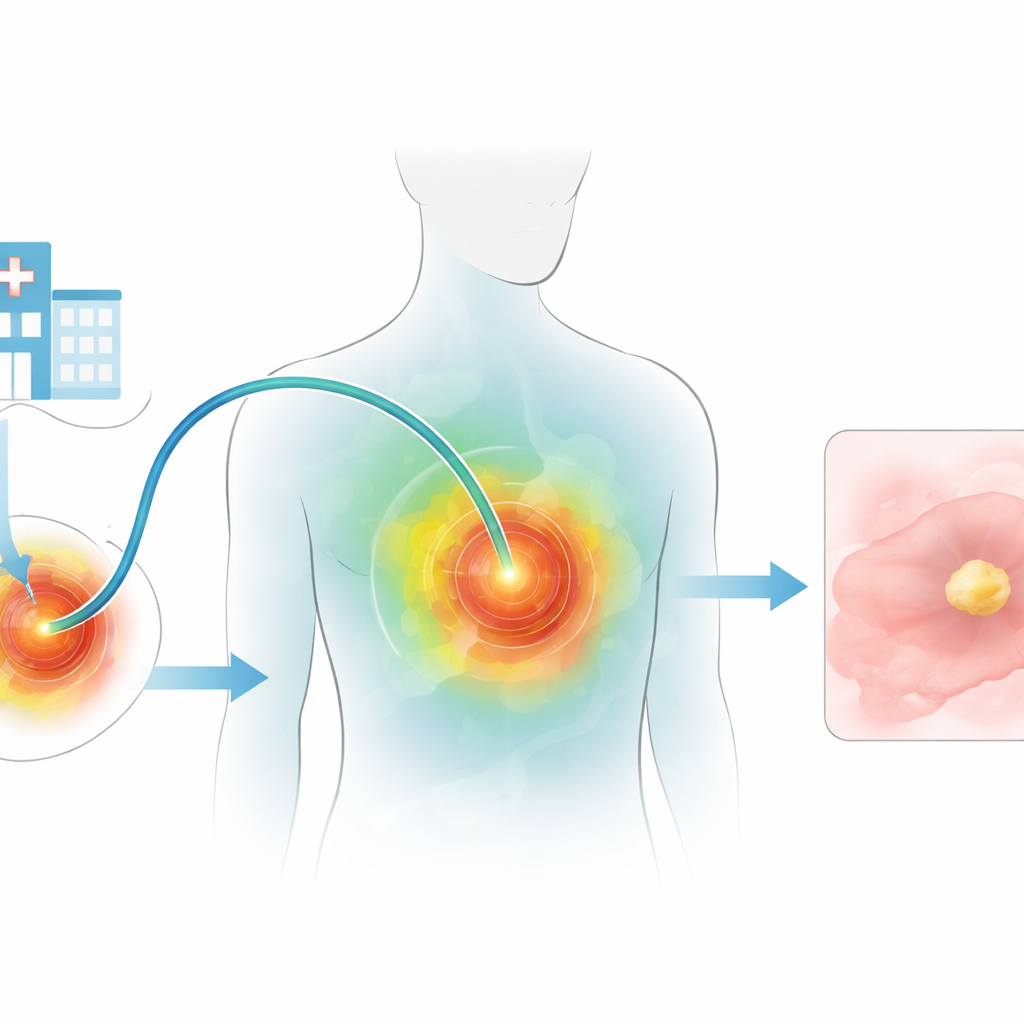
Dlaczego podgrzewanie guzów jest trudne
Terapie oparte na świetle obiecują wysoce zlokalizowane uszkodzenie guzów, oszczędzając resztę organizmu. Jednak światło nie przenika daleko przez tkanki, a wiele obecnych metod opiera się na nanocząstkach krążących po całym organizmie, co budzi obawy o długoterminową toksyczność. Istniejące sondy włókniste zwykle pełnią tylko jedną funkcję na włókno — albo leczą, albo mierzą — i często wymagają kilku oddzielnych włókien, co oznacza większe nacięcia, sztywniejsze urządzenia i większy dyskomfort dla pacjentów. Lekarze rzadko otrzymują też informacje zwrotne na żywo podczas zabiegu, co utrudnia uniknięcie niedogrzania guza lub przegrzania zdrowej tkanki.
Jedno włókno, które widzi, grzeje i sprawdza
Naukowcy rozwiązali te wyzwania, umieszczając trzy różne składniki reagujące na światło na zwężonym końcówce pojedynczego włókna optycznego. Końcówka, mająca z grubsza szerokość ludzkiego włosa, pokryta jest cienką warstwą hydrożelu zawierającą: barwnik czuły na pH do mapowania kwasowości mikrośrodowiska guza, materiał reagujący na temperaturę umożliwiający odczyt lokalnego ciepła oraz barwnik zamieniający bliską podczerwień na ciepło do terapii. Co istotne, każdy składnik reaguje na inną barwę światła — strategię zapożyczoną z telekomunikacji zwaną multipleksacją długości fali. Poprzez proste zmienianie długości fali wejściowej lekarze mogą przełączać to samo włókno między pomiarem pH, pomiarem temperatury i ogrzewaniem, bez wzajemnych zakłóceń sygnałów.
Nasłuchując chemii guza
Wiele guzów tworzy wokół siebie kwaśne środowisko, a stopień kwasowości jest ściśle powiązany z agresywnością nowotworu. Czujnik pH zespołu jest w stanie wykryć bardzo małe zmiany kwasowości — mniejsze niż dwie setne jednostki pH — w zakresie istotnym zarówno dla tkanek zdrowych, jak i nowotworowych. U myszy z rakiem jelita grubego sonda wyraźnie rozróżniała tkankę guza od tkanki prawidłowej i potrafiła nawet wskazać, gdzie guz się kończy, a zaczyna zdrowa tkanka, na podstawie zmian kwasowości od środka ku brzegom. Po leczeniu ta sama sonda śledziła stopniowy shift w kierunku mniej kwaśnych warunków, co sygnalizowało poprawę zachowania tkanek i stanowiło wczesny marker skuteczności terapii.
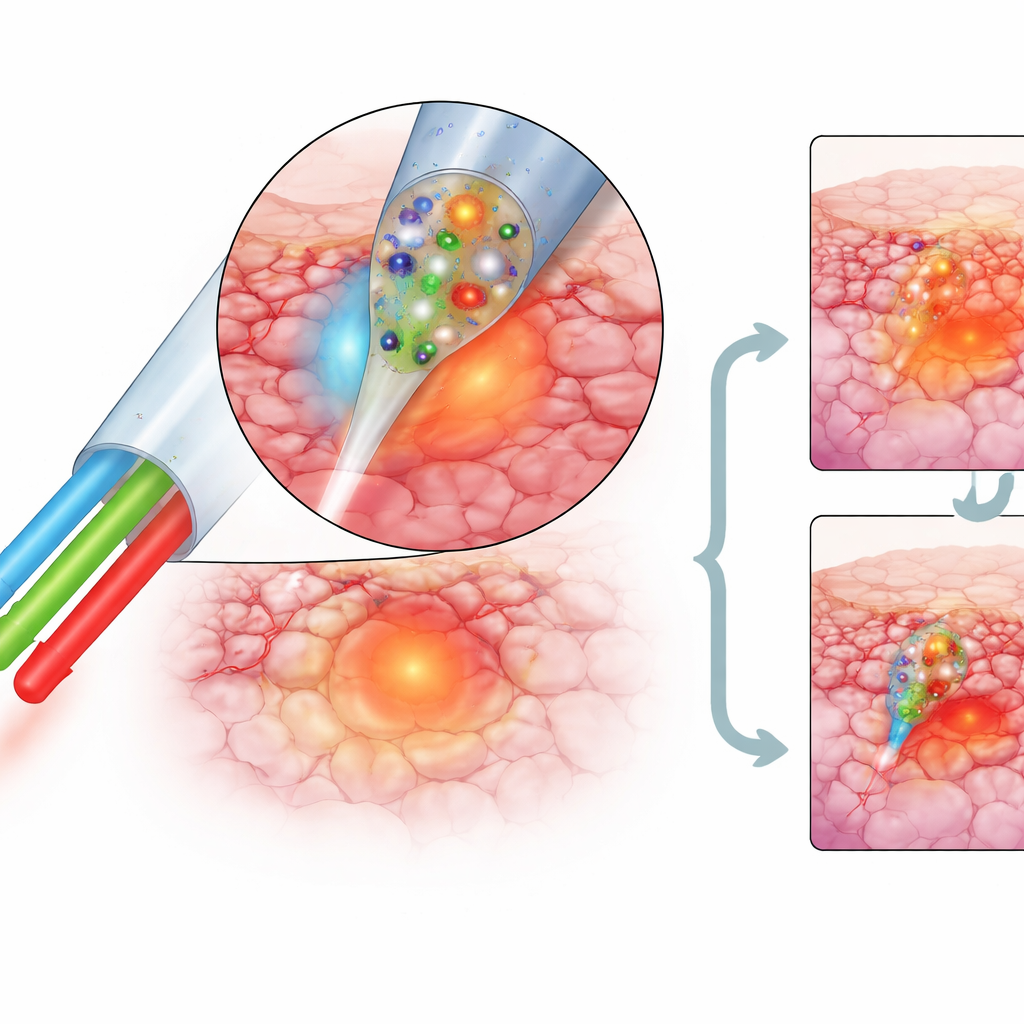
Inteligentne ogrzewanie z wbudowaną kontrolą temperatury
Aby upewnić się, że guz zostanie zniszczony bez uszkadzania pobliskich struktur, sonda nieustannie mierzy własną temperaturę. Specjalnie zaprojektowany materiał emitujący światło w powłoce zmienia bilans barw w miarę nagrzewania, co pozwala systemowi wnioskować o temperaturze z precyzją około jednej trzeciej stopnia Celsjusza w pobliżu temperatury ciała i z jeszcze większą czułością przy wyższych temperaturach zabiegowych. Gdy barwnik grzewczy jest aktywowany przez laser podczerwieni dostarczany tym samym włóknem, końcówka w warunkach laboratoryjnych może osiągnąć ponad 100 stopni Celsjusza, używając mniejszej mocy niż wymaga wiele systemów z nanocząstkami. U żywych myszy badacze utrzymywali włókno w około 65 stopniach Celsjusza przez 15 minut — wystarczająco, by zewnętrzne obszary guza osiągnęły temperaturę terapeutyczną bez zauważalnej szkody dla zwierząt.
Wyniki we wnętrzu żywych guzów
W eksperymentach na myszach podejście w zamkniętej pętli okazało się skuteczne i łagodne. Przed podgrzewaniem odczyty pH pomagały zlokalizować guz i określić jego granice. W trakcie zabiegu odczyt temperatury sondy kierował dawką ogrzewania. Po zabiegu powtarzane pomiary pH wykazały stały spadek kwasowości, odzwierciedlający poprawę przepływu krwi i mniejszą liczbę aktywnych komórek nowotworowych. W kolejnych dniach większość leczonych guzów zmniejszyła się lub zniknęła, podczas gdy nieleczone guzy nadal rosły. Analiza tkanek potwierdziła rozległą śmierć komórek nowotworowych, zmniejszone oznaki niedotlenienia i niższe tempo proliferacji komórek u leczonych zwierząt, bez wykrycia istotnych uszkodzeń narządów wewnętrznych.
Co to może znaczyć dla pacjentów
Mówiąc prościej, autorzy zbudowali wielofunkcyjnego „lekarza-włókno”, który potrafi znaleźć guz, wypalić go od środka przy pomocy światła i natychmiast sprawdzić, czy zabieg się powiódł — wszystko za pomocą jednej, bardzo małej sondy. Ponieważ system separuje każdą funkcję poprzez kolor światła, w przyszłości można dodać kolejne moduły sensoryczne i terapeutyczne bez potrzeby używania dodatkowych włókien. Te same koncepcje konstrukcyjne można przenieść na miększe, bardziej elastyczne włókna do długoterminowych implantów. Jeśli technologia zostanie dalej rozwinięta dla zastosowań u ludzi, mogłaby umożliwić dokładniejsze, mniej inwazyjne leczenie nowotworów z informacją zwrotną w czasie rzeczywistym, pomagając lekarzom dopasować terapię do każdego pacjenta przy minimalizowaniu skutków ubocznych.
Cytowanie: Li, Z., Li, Z., Cheng, Z. et al. Multifunctional fiber-optic theranostic probe for closed-loop tumor photothermal therapy. Light Sci Appl 15, 216 (2026). https://doi.org/10.1038/s41377-026-02219-3
Słowa kluczowe: optyczna terapia nowotworowa, fototermiczne wyłyżeczkowanie guza, pH mikrośrodowiska guza, minimalnie inwazyjne theranostyki, czujniki temperatury w czasie rzeczywistym