Clear Sky Science · pt
Detecção da disfunção da barreira hematoencefálica relacionada à inflamação usando PET e ressonância magnética: um estudo piloto
Por que pequenos vazamentos na proteção do cérebro importam
Muitas doenças cerebrais, da doença de Alzheimer ao traumatismo cranioencefálico, estão ligadas a uma forma de inflamação de baixo grau dentro do cérebro. Um ator-chave nessa história é a barreira hematoencefálica, uma parede protetora de células que normalmente impede a entrada de substâncias nocivas no cérebro. Quando essa barreira começa a vazar, problemas surgem — mas detectar esses vazamentos iniciais e sutis tem sido muito difícil. Este estudo testa uma nova varredura não invasiva em camundongos que pretende identificar esses pequenos defeitos da barreira bem antes de danos cerebrais óbvios ou aparecimento de sintomas.
Observando a parede protetora do cérebro
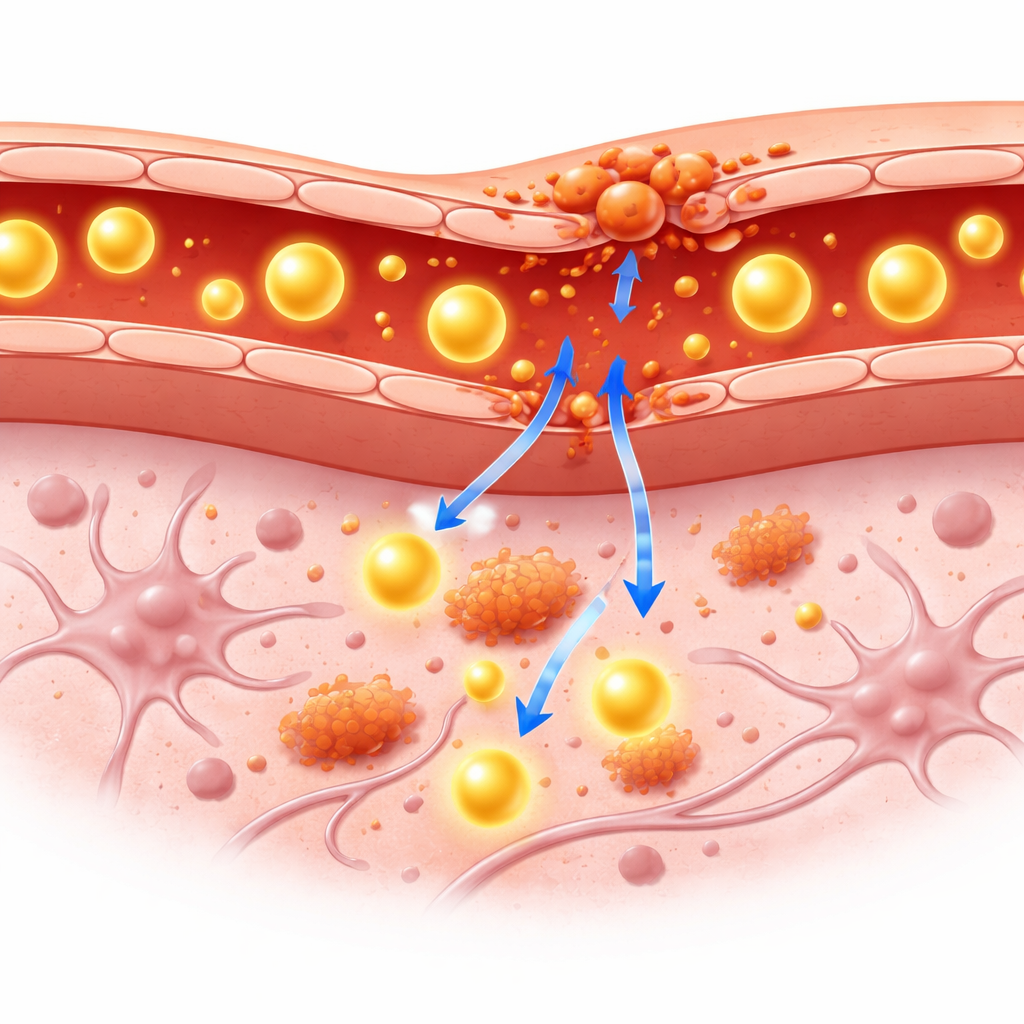
A barreira hematoencefálica age como um filtro altamente seletivo entre o sangue e o cérebro. Ela permite a passagem de nutrientes, mas bloqueia muitas moléculas grandes, inclusive a maioria das proteínas sanguíneas. Na inflamação crônica do cérebro, células do sistema imune e seus mensageiros químicos podem enfraquecer esse filtro, permitindo que moléculas grandes penetrem no tecido cerebral. Atualmente, os clínicos dependem de exames de sangue e de líquido cefalorraquidiano para inferir que a barreira está comprometida, mas esses métodos não conseguem mostrar com precisão onde no cérebro ocorre o vazamento ou quão severo ele é. Ferramentas de imagem como PET e RM podem ver dentro do cérebro vivo, mas a maioria dos traçadores PET existentes atravessa a barreira com muita facilidade, dificultando distinguir se a própria barreira está danificada.
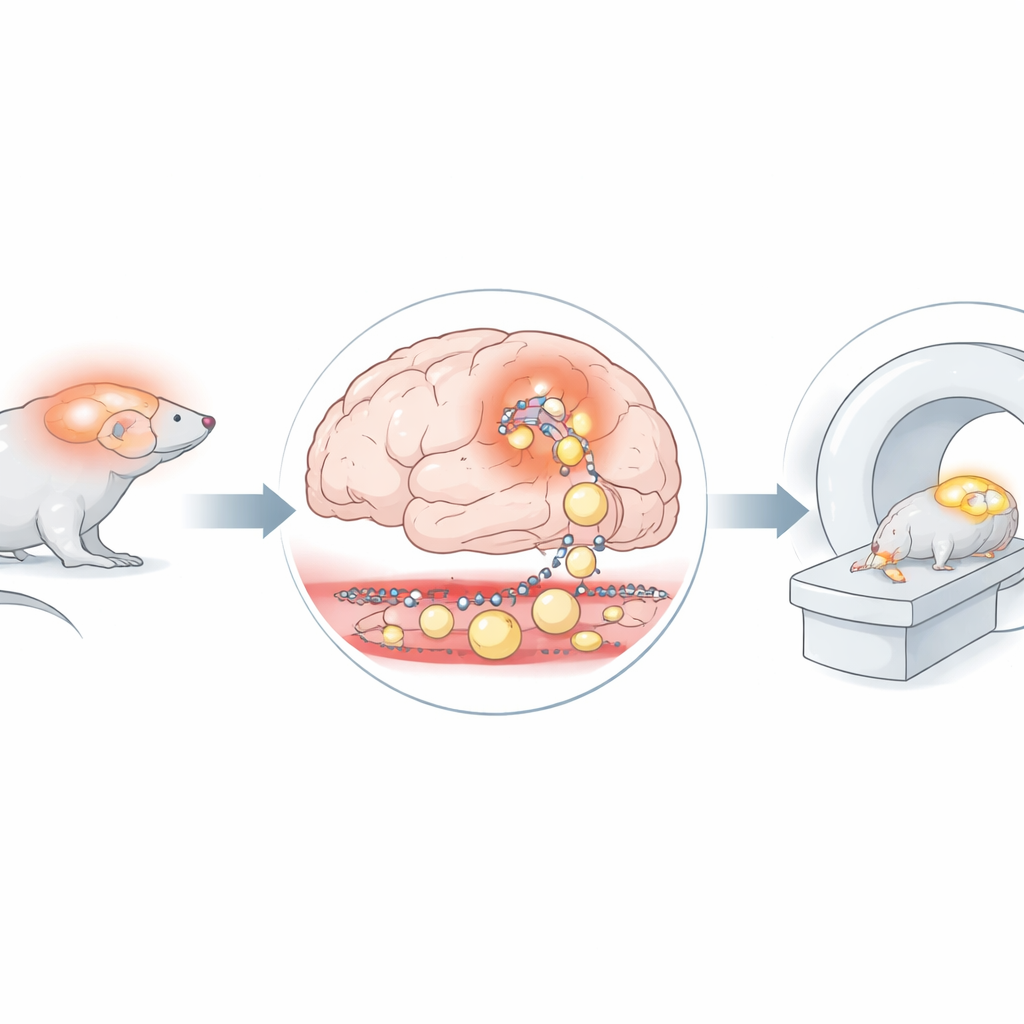
Uma proteína marcada como visitante visível
Os pesquisadores exploraram uma nova estratégia: usar albumina sérica humana — uma proteína sanguínea grande e comum que normalmente permanece na corrente sanguínea — e ligar a ela uma marca fracamente radioativa. Como a albumina é volumosa e normalmente não atravessa para o cérebro, qualquer sinal dessa proteína marcada dentro do tecido cerebral deve indicar um vazamento verdadeiro. A equipe usou um modelo murino geneticamente modificado para desenvolver inflamação cerebral crônica por meio de uma via de sinalização específica em células de suporte chamadas astrócitos. Esses camundongos, junto com camundongos controle saudáveis, foram injetados com a albumina radiomarcada e escaneados com PET/RM combinado uma hora e novamente 24 horas após a injeção. A RM forneceu imagens detalhadas da estrutura cerebral, enquanto o PET mostrou onde a albumina marcada se acumulou ao longo do tempo.
Mudanças ocultas que as imagens conseguem ver
Na RM, os cérebros dos camundongos inflamados e saudáveis pareciam essencialmente os mesmos: sem atrofia, sem lesões óbvias e sem quebra visível do tecido cerebral, mesmo em áreas conhecidas por serem vulneráveis. No entanto, o PET contou uma história diferente. Nos camundongos com neuroinflamação crônica, o sinal da albumina marcada foi consistentemente mais alto no cérebro, especialmente no cerebelo, uma região envolvida na coordenação e no equilíbrio. Ao longo de 24 horas, a quantidade de traçador no sangue caiu continuamente em ambos os grupos, mas a razão do sinal cerebral para o sinal sanguíneo aumentou mais fortemente nos camundongos inflamados. Esse padrão indica que mais da proteína grande estava atravessando a barreira e permanecendo no tecido cerebral desses animais.
Verificando o cérebro após a imagem
Para confirmar as imagens, os pesquisadores examinaram os órgãos após a sessão final de imagem. Eles mediram a radioatividade no cérebro, no sangue e nos principais órgãos e novamente encontraram níveis mais altos da albumina marcada nos cérebros dos camundongos inflamados, com níveis semelhantes nos órgãos periféricos entre os dois grupos. Fatias finas de tecido cerebral foram coradas e inspecionadas ao microscópio, revelando que a arquitetura básica do cerebelo permaneceu intacta — as camadas celulares foram preservadas e não havia sinais óbvios de perda celular. Ainda assim, a autoradiografia digital, uma técnica que mapeia a radioatividade nas lâminas de tecido, mostrou sinal mais forte no cerebelo dos camundongos inflamados, espelhando os achados do PET. Em conjunto, esses resultados sugerem que vazamentos na barreira já estavam presentes apesar das medidas estruturais padrão ainda parecerem normais.
O que isso significa para o cuidado futuro do cérebro
Este estudo piloto sugere que um traçador de albumina radiomarcada, combinado com imagem PET/RM, pode detectar de forma sensível alterações precoces na barreira protetora do cérebro durante inflamação crônica, particularmente em regiões como o cerebelo. O método captou vazamento sutil de moléculas grandes antes de qualquer dano tecidual claro aparecer na RM ou em exames microscópicos rotineiros. Embora o trabalho tenha sido realizado em um número pequeno de camundongos e enfrente alguns desafios técnicos — especialmente em vasos sanguíneos muito pequenos —, a abordagem pode eventualmente ajudar médicos a monitorar a saúde da barreira em pessoas com doenças neuroinflamatórias ou lesão cerebral. Em termos simples, oferece uma maneira de ver a barreira do cérebro começando a falhar, abrindo caminho para diagnósticos mais precoces e, potencialmente, tratamentos mais direcionados e antecipados.
Citação: Hilbrig, C.F., Baumann, B., Sievert, W. et al. Detection of inflammation-related blood–brain barrier dysfunction using PET and MR imaging: a pilot study. Sci Rep 16, 12014 (2026). https://doi.org/10.1038/s41598-026-47352-6
Palavras-chave: barreira hematoencefálica, neuroinflamação, PET MRI, traçador de albumina, imagem cerebral