Clear Sky Science · nl
Detectie van ontstekingsgerelateerde bloed-hersenbarrièredisfunctie met PET- en MR-beelden: een pilotstudie
Waarom kleine lekkages in het beschermschild van de hersenen ertoe doen
Veel hersenaandoeningen, van Alzheimer tot traumatisch hersenletsel, houden verband met een sluimerende vorm van ontsteking in de hersenen. Een sleutelrol in dit verhaal is weggelegd voor de bloed-hersenbarrière, een beschermende wand van cellen die normaal gesproken schadelijke stoffen buiten de hersenen houdt. Als deze barrière begint te lekken, volgen er problemen — maar het vroegtijdig opsporen van die subtiele lekkages is erg moeilijk geweest. Deze studie test een nieuwe, niet-invasieve scan bij muizen die gericht is op het opsporen van zulke kleine barrièredefecten lang voordat duidelijk hersenletsel of symptomen optreden.
Het beschermende muurtje van de hersenen in beeld
De bloed-hersenbarrière werkt als een zeer selectief filter tussen het bloed en de hersenen. Het laat voedingsstoffen binnen maar blokkeert veel grote moleculen, waaronder de meeste bloedproteïnen. Bij chronische hersenontsteking kunnen immuuncellen en hun signaalstoffen dit filter verzwakken, waardoor grote moleculen in het hersenweefsel kunnen sijpelen. Klinisch vertrouwen artsen momenteel op bloedtesten en ruggenmergvochtanalyses om af te leiden dat de barrière beschadigd is, maar deze methoden kunnen niet nauwkeurig laten zien waar in de hersenen het lek zit of hoe ernstig het is. Beeldvormende technieken zoals PET en MRI kunnen in levende hersenen kijken, maar de meeste bestaande PET-tracers passeren de barrière te gemakkelijk, waardoor het lastig is vast te stellen of de barrière zelf beschadigd is.
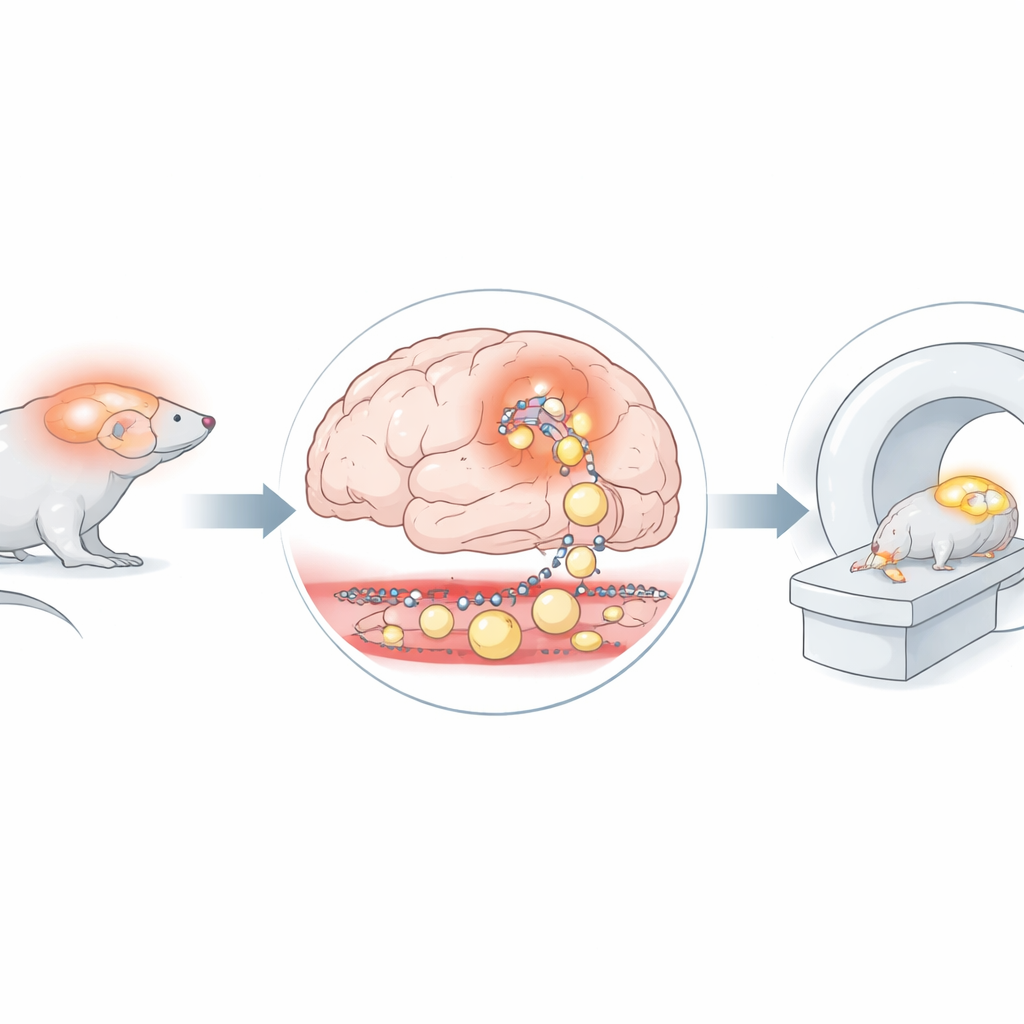
Een gemerkt eiwit als zichtbare gast
De onderzoekers onderzochten een nieuwe strategie: menselijk serumalbumine — een veelvoorkomend, groot bloedproteïne dat normaal in de bloedbaan blijft — markeren met een zwak radioactief label. Omdat albumine omvangrijk is en gewoonlijk niet in de hersenen terechtkomt, zou elk signaal van dit gemarkeerde eiwit in het hersenweefsel duiden op een daadwerkelijk lek. Het team gebruikte een muismodel dat genetisch zo was aangepast dat het chronische hersenontsteking ontwikkelt via een specifiek signaalpad in ondersteunende cellen die astrocyten worden genoemd. Deze muizen, samen met gezonde controlemuizen, kregen het geradiomerkte albumine geïnjecteerd en werden gescand met gecombineerde PET en MRI één uur en opnieuw 24 uur na injectie. MRI leverde gedetailleerde beelden van de hersenstructuur, terwijl PET liet zien waar het gemarkeerde albumine in de loop van de tijd ophoopte.
Verborgen veranderingen die scans kunnen tonen
Op MRI zagen de hersenen van de ontstoken en gezonde muizen er in wezen hetzelfde uit: geen krimp, geen duidelijke laesies en geen zichtbare afbraak van hersenweefsel, zelfs niet in gebieden waarvan bekend is dat ze kwetsbaar zijn. PET vertelde echter een ander verhaal. Bij de muizen met chronische neuro-inflammatie was het signaal van het gemarkeerde albumine consequent hoger in de hersenen, en vooral in het cerebellum, een regio die betrokken is bij coördinatie en evenwicht. Over 24 uur daalde de hoeveelheid tracer in het bloed gestaag in beide groepen, maar de verhouding van hersensignaal tot bloed signaal steeg sterker bij de ontstoken muizen. Dit patroon wijst erop dat er meer van het grote proteïne door de barrière sijpelde en in het hersenweefsel bleef hangen bij deze dieren.
De hersenen nakijken na de scan
Om de scans te bevestigen onderzochten de onderzoekers de organen na de laatste beeldvorming. Ze maten radioactiviteit in de hersenen, het bloed en de grote organen en vonden opnieuw hogere niveaus van het gemarkeerde albumine in de hersenen van ontstoken muizen, met vergelijkbare niveaus in perifere organen tussen beide groepen. Dunne plakjes hersenweefsel werden gekleurd en onder de microscoop bekeken, waarbij bleek dat de basale architectuur van het cerebellum intact bleef — cel-lagen waren behouden en er waren geen duidelijke tekenen van celdood. Digitale autoradiografie, een techniek die radioactiviteit in weefselplakjes in kaart brengt, toonde echter een sterker signaal in het cerebellum van de ontstoken muizen, overeenkomstig de PET-resultaten. Gezamenlijk suggereren deze resultaten dat barrièrelekkages al aanwezig waren, hoewel standaard structurele maten nog normaal leken.
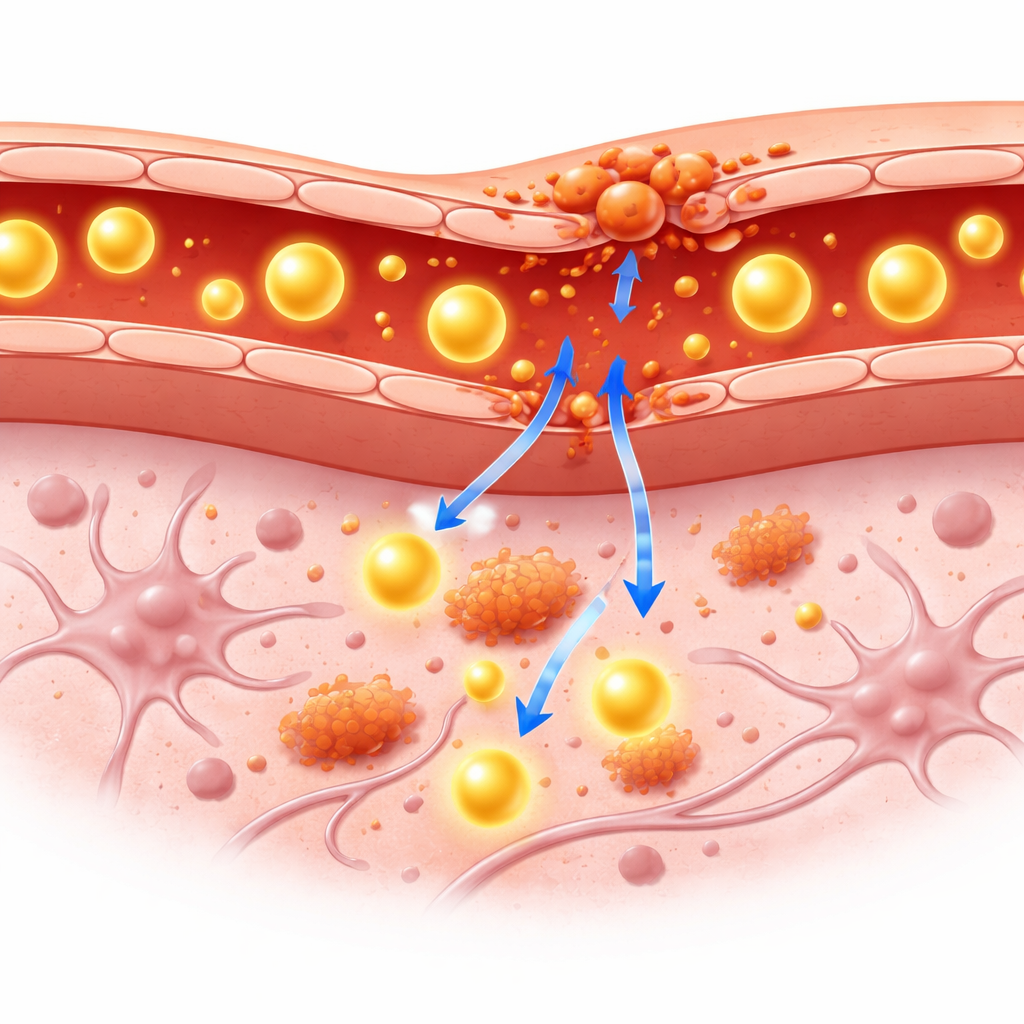
Wat dit betekent voor toekomstige zorg voor de hersenen
Deze pilotstudie suggereert dat een geradiomerkte albumine-tracer, gecombineerd met PET/MR-beeldvorming, vroegtijdige veranderingen in de beschermende barrière van de hersenen tijdens chronische ontsteking gevoelig kan detecteren, met name in regio’s zoals het cerebellum. De methode signaleerde subtiele lekkage van grote moleculen voordat er duidelijke weefselschade zichtbaar werd op MRI of in routinematig microscopisch onderzoek. Hoewel het werk in een klein aantal muizen is uitgevoerd en enkele technische uitdagingen kent — vooral in zeer kleine bloedvaten — kan de aanpak mogelijk artsen helpen bij het monitoren van barrièregezondheid bij mensen met neuro-inflammatoire ziekten of hersenletsel. Simpel gezegd biedt het een manier om te zien dat het beschermschild van de hersenen begint te falen, wat de deur opent naar vroegere diagnose en mogelijk eerder, meer gerichte behandeling.
Bronvermelding: Hilbrig, C.F., Baumann, B., Sievert, W. et al. Detection of inflammation-related blood–brain barrier dysfunction using PET and MR imaging: a pilot study. Sci Rep 16, 12014 (2026). https://doi.org/10.1038/s41598-026-47352-6
Trefwoorden: bloed-hersenbarrière, neuro-inflammatie, PET MRI, albumine tracer, hersenbeeldvorming