Clear Sky Science · de
Nachweis entzündungsbedingter Blut-Hirn-Schranken-Dysfunktion mittels PET- und MR-Bildgebung: eine Pilotstudie
Warum kleine Lecks in der Gehirnschutzhülle wichtig sind
Viele Erkrankungen des Gehirns, von Alzheimer bis hin zu traumatischen Hirnverletzungen, stehen im Zusammenhang mit einer langsam verlaufenden Form der Entzündung im Gehirn. Ein zentraler Akteur in diesem Prozess ist die Blut-Hirn-Schranke, eine schützende Zellbarriere, die normalerweise schädliche Substanzen vom Gehirn fernhält. Wenn diese Schranke zu lecken beginnt, entstehen Probleme – doch frühe, subtile Lecks zu erkennen, war bislang sehr schwierig. Diese Studie prüft bei Mäusen einen neuen, nicht-invasiven Scan, der darauf abzielt, solche kleinen Barrieredefekte lange vor offensichtlichen Hirnschäden oder Symptomen zu entdecken.
Die Schutzwand des Gehirns beobachten
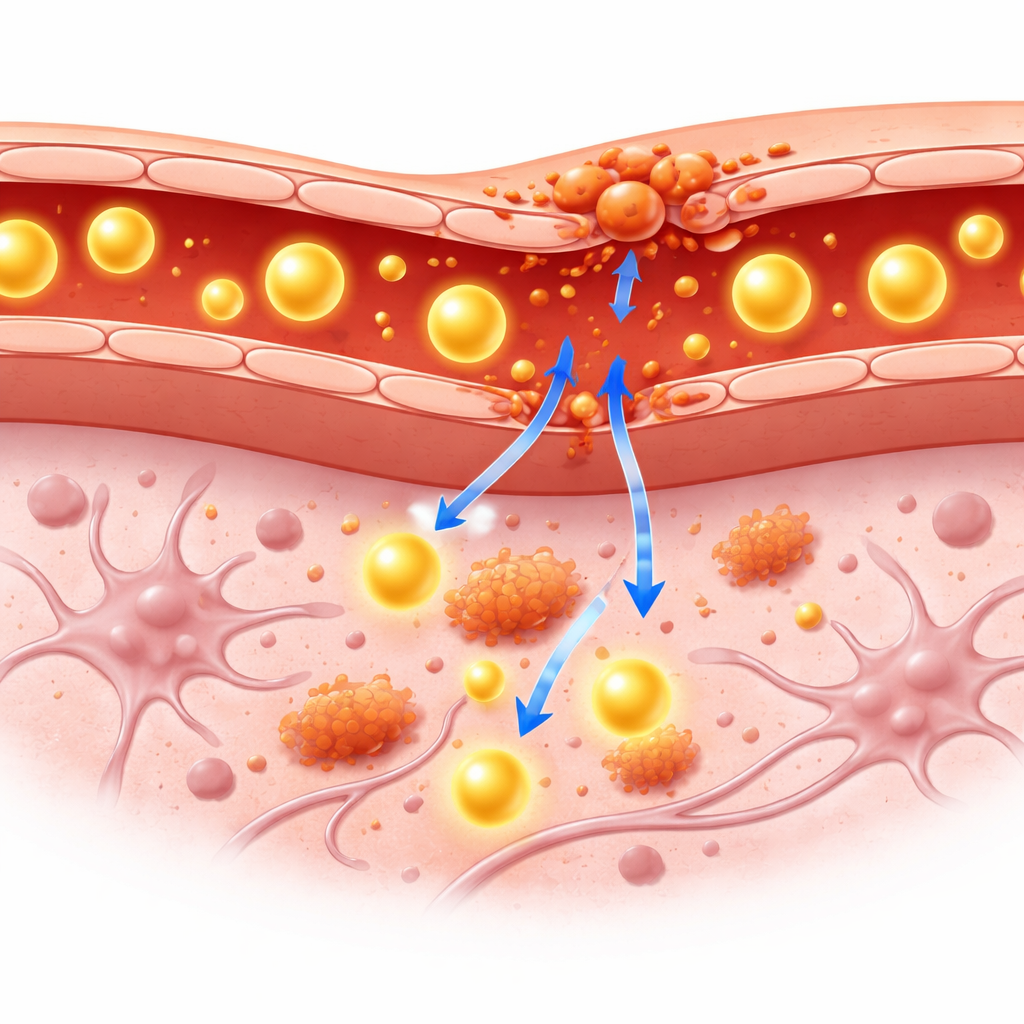
Die Blut-Hirn-Schranke wirkt wie ein hochselektiver Filter zwischen Blut und Gehirn. Sie lässt Nährstoffe hinein, blockiert aber viele große Moleküle, einschließlich der meisten Blutproteine. Bei chronischen Gehirnentzündungen können Immunzellen und ihre Botenstoffe diesen Filter schwächen, sodass größere Moleküle ins Gewebe eindringen. Kliniker stützen sich derzeit auf Bluttests und Liquorproben, um Rückschlüsse auf eine gestörte Schranke zu ziehen, doch diese Methoden zeigen nicht genau, wo im Gehirn das Leck auftritt oder wie schwerwiegend es ist. Bildgebende Verfahren wie PET und MRI erlauben einen Blick ins lebende Gehirn, doch die meisten vorhandenen PET-Tracer passieren die Schranke zu leicht, sodass es schwerfällt zu unterscheiden, ob die Schranke selbst beschädigt ist.
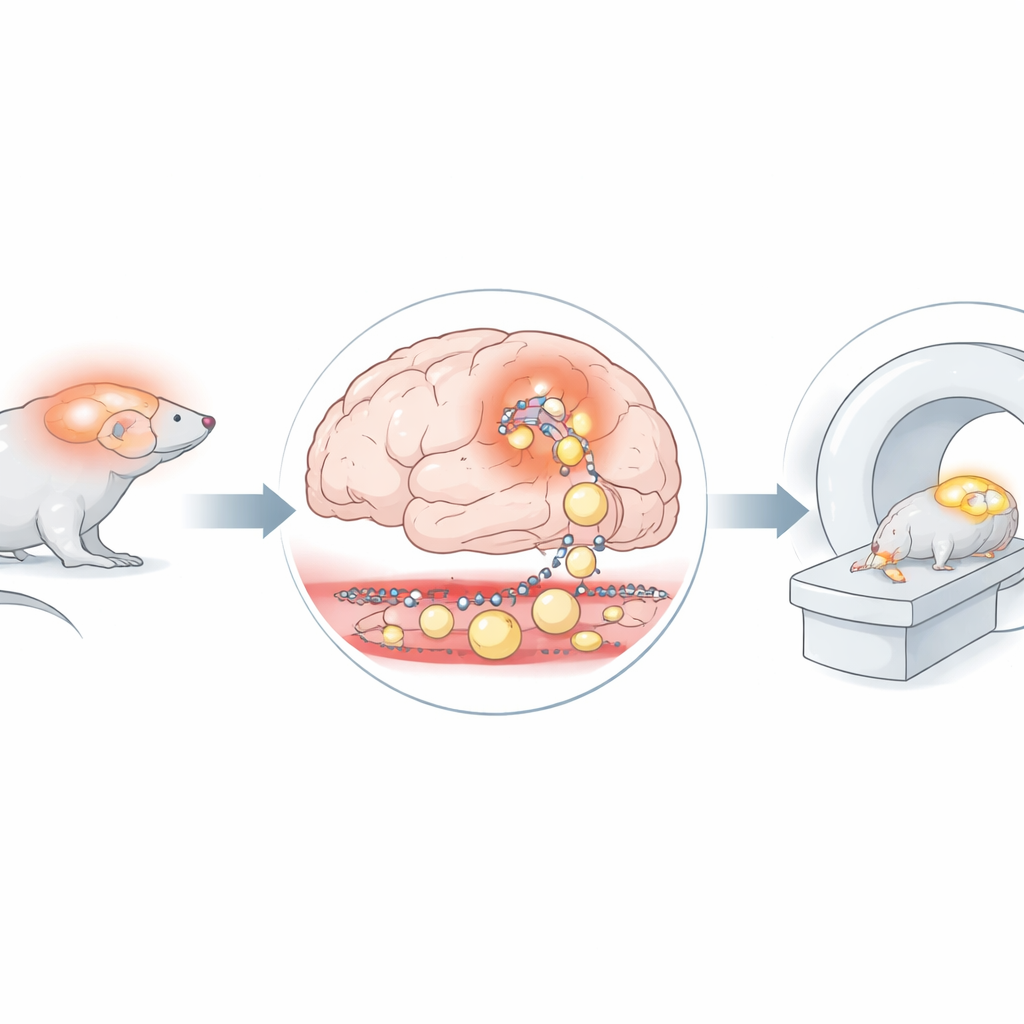
Ein markiertes Protein als sichtbarer Gast
Die Forschenden verfolgten eine neue Strategie: Sie nahmen humanes Serumalbumin – ein häufiges, großes Blutprotein, das normalerweise im Blutkreislauf verbleibt – und versehen es mit einem schwach radioaktiven Marker. Da Albumin sperrig ist und normalerweise nicht ins Gehirn übertritt, sollte jedes Signal dieses markierten Proteins im Gehirngewebe auf ein echtes Leck hinweisen. Das Team verwendete ein Mausmodell, das so gezüchtet wurde, dass es durch einen bestimmten Signalweg in den Stütz- und Versorgungszellen, den Astrozyten, eine chronische Gehirnentzündung entwickelt. Diese Mäuse sowie gesunde Kontrolltiere wurden mit dem radioaktiv markierten Albumin injiziert und eine Stunde sowie 24 Stunden nach der Injektion mit kombinierter PET- und MRI-Bildgebung gescannt. Das MRI lieferte detaillierte Bilder der Hirnstruktur, während PET zeigte, wo sich das markierte Albumin im Laufe der Zeit ansammelte.
Verborgene Veränderungen, die Scans sichtbar machen
Im MRI sahen die Gehirne der entzündeten und der gesunden Mäuse im Wesentlichen gleich aus: keine Schrumpfung, keine offensichtlichen Läsionen und kein sichtbarer Zerfall von Hirngewebe, selbst in als anfällig bekannten Regionen. PET erzählte jedoch eine andere Geschichte. Bei den Mäusen mit chronischer Neuroinflammation war das Signal des markierten Albumins im Gehirn durchweg erhöht, insbesondere im Kleinhirn, einer Region, die an Koordination und Gleichgewicht beteiligt ist. Über 24 Stunden nahm die Tracer-Menge im Blut in beiden Gruppen stetig ab, doch das Verhältnis von Hirnsignal zu Blutsignal stieg bei den entzündeten Mäusen stärker an. Dieses Muster deutet darauf hin, dass mehr des großen Proteins durch die Schranke sickerte und im Hirngewebe dieser Tiere verblieb.
Prüfung des Gehirns nach dem Scan
Zur Bestätigung der Bildgebung untersuchten die Forschenden die Organe nach der letzten Bildgebungssitzung. Sie maßen die Radioaktivität im Gehirn, Blut und in den wichtigsten Organen und fanden erneut höhere Werte des markierten Albumins im Gehirn der entzündeten Mäuse, während die Werte in peripheren Organen in beiden Gruppen ähnlich waren. Dünne Schnittpräparate des Gehirns wurden gefärbt und mikroskopisch untersucht; dabei zeigte sich, dass die Grundarchitektur des Kleinhirns intakt blieb – Zellschichten waren erhalten und es gab keine offensichtlichen Hinweise auf Zellverlust. Digitale Autoradiographie, eine Technik zur Kartierung von Radioaktivität in Gewebeschnitten, zeigte jedoch ein stärkeres Signal im Kleinhirn der entzündeten Mäuse, was die PET-Befunde widerspiegelte. Gemeinsam deuten diese Ergebnisse darauf hin, dass Barrierelecks bereits vorhanden waren, auch wenn standardmäßige strukturelle Messungen noch normal wirkten.
Was das für die künftige Versorgung des Gehirns bedeutet
Diese Pilotstudie legt nahe, dass ein radioaktiv markierter Albumin-Tracer in Kombination mit PET/MR-Bildgebung frühzeitige Veränderungen der Schutzbarriere des Gehirns bei chronischer Entzündung empfindlich nachweisen kann, insbesondere in Regionen wie dem Kleinhirn. Die Methode erfasste subtile Lecks großer Moleküle, bevor auf MRI oder in routinemäßigen mikroskopischen Untersuchungen klare Gewebeschäden erkennbar waren. Obwohl die Arbeit an einer kleinen Anzahl von Mäusen durchgeführt wurde und technischen Herausforderungen gegenübersteht – vor allem bei sehr kleinen Blutgefäßen – könnte der Ansatz letztlich Ärzten helfen, den Zustand der Schranke bei Menschen mit neuroinflammatorischen Erkrankungen oder Hirnverletzungen zu überwachen. Einfach gesagt bietet er eine Möglichkeit, zu sehen, wie die Schutzhülle des Gehirns zu versagen beginnt, und eröffnet damit Perspektiven für frühere Diagnosen und möglicherweise frühere, gezieltere Behandlungen.
Zitation: Hilbrig, C.F., Baumann, B., Sievert, W. et al. Detection of inflammation-related blood–brain barrier dysfunction using PET and MR imaging: a pilot study. Sci Rep 16, 12014 (2026). https://doi.org/10.1038/s41598-026-47352-6
Schlüsselwörter: Blut-Hirn-Schranke, Neuroinflammation, PET MRI, Albumin-Tracer, Gehirnbildgebung