Clear Sky Science · fr
Détection des dysfonctionnements de la barrière hémato‑encéphalique liés à l’inflammation par PET et IRM : une étude pilote
Pourquoi de petites fuites de la barrière cérébrale ont de l’importance
De nombreuses maladies cérébrales, de la maladie d’Alzheimer aux traumatismes crâniens, sont associées à une inflammation chronique et de faible intensité à l’intérieur du cerveau. Un acteur clé de ce processus est la barrière hémato‑encéphalique, une paroi protectrice de cellules qui empêche normalement les substances nocives d’entrer dans le cerveau. Lorsque cette barrière commence à fuir, des problèmes surgissent — mais détecter ces fuites précoces et subtiles a été très difficile. Cette étude teste un nouveau type de scan non invasif chez la souris visant à repérer ces petits défauts de la barrière bien avant l’apparition de lésions cérébrales évidentes ou de symptômes.
Observer la paroi protectrice du cerveau
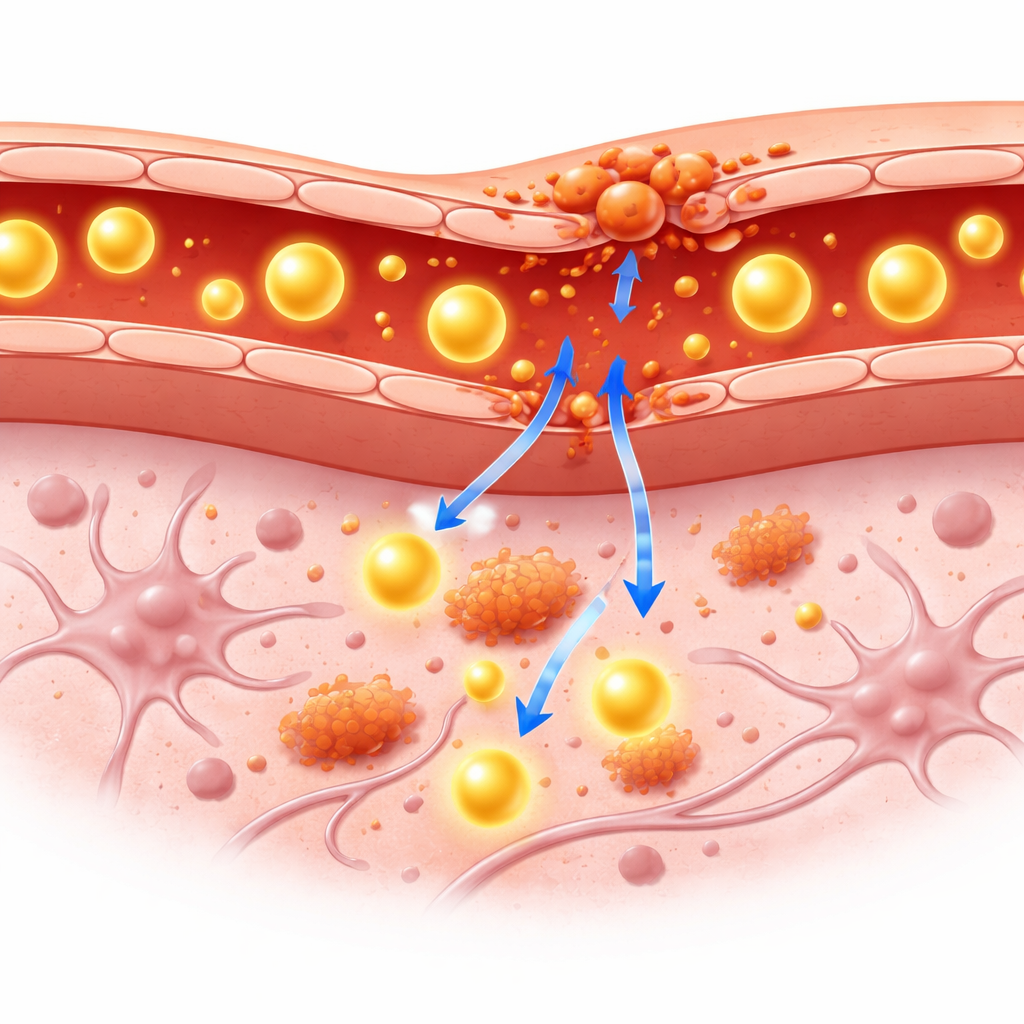
La barrière hémato‑encéphalique fonctionne comme un filtre très sélectif entre le sang et le cerveau. Elle laisse passer les nutriments mais bloque de nombreuses grosses molécules, y compris la plupart des protéines sanguines. Lors d’une inflammation cérébrale chronique, les cellules immunitaires et leurs messagers chimiques peuvent affaiblir ce filtre, permettant à de grosses molécules de s’infiltrer dans le tissu cérébral. Les cliniciens s’appuient aujourd’hui sur des analyses sanguines et des prélèvements de liquide cérébro‑spinal pour inférer une altération de la barrière, mais ces méthodes ne montrent pas précisément où la fuite se produit ni son degré de gravité. Des outils d’imagerie tels que le PET et l’IRM permettent de voir à l’intérieur du cerveau vivant, toutefois la plupart des traceurs PET existants traversent la barrière trop facilement, rendant difficile de déterminer si la barrière elle‑même est endommagée.
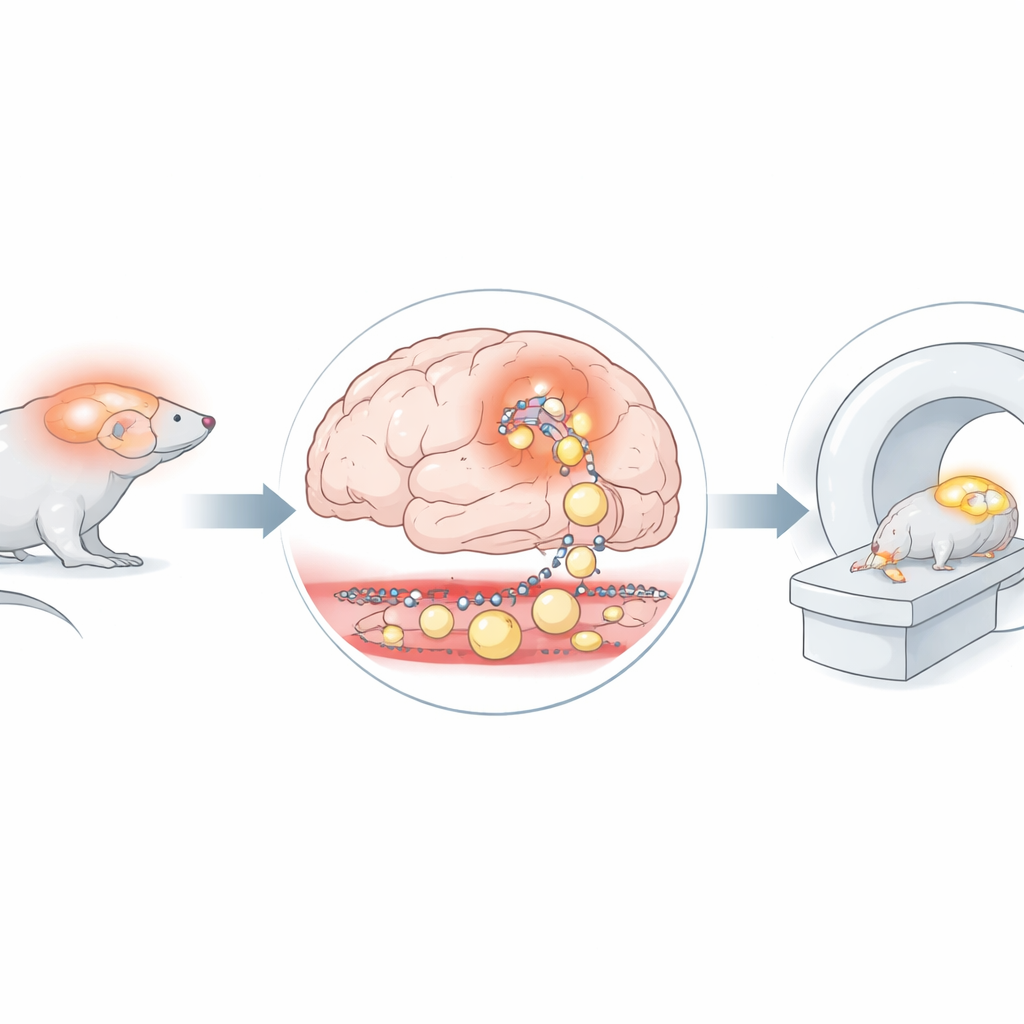
Une protéine marquée comme invité visible
Les chercheurs ont exploré une nouvelle stratégie : utiliser l’albumine sérique humaine — une protéine sanguine volumineuse qui reste normalement dans la circulation — et lui attacher un marqueur faiblement radioactif. Comme l’albumine est volumineuse et ne traverse habituellement pas la barrière, tout signal provenant de cette protéine marquée à l’intérieur du tissu cérébral devrait indiquer une fuite réelle. L’équipe a utilisé un modèle murin génétiquement modifié pour développer une inflammation cérébrale chronique via une voie de signalisation spécifique dans les cellules de soutien appelées astrocytes. Ces souris, et des souris témoins saines, ont été injectées avec l’albumine radiomarquée et scannées par PET/IRM combinés une heure puis 24 heures après l’injection. L’IRM a fourni des images détaillées de la structure cérébrale, tandis que le PET a montré où l’albumine marquée s’accumulait au fil du temps.
Des changements cachés que les scans révèlent
À l’IRM, les cerveaux des souris enflammées et des souris saines semblaient essentiellement identiques : pas d’atrophie, pas de lésions évidentes et pas de dégradation visible du tissu cérébral, même dans des zones connues pour être vulnérables. Cependant, le PET a raconté une autre histoire. Chez les souris présentant une neuroinflammation chronique, le signal de l’albumine marquée était systématiquement plus élevé dans le cerveau, et en particulier dans le cervelet, une région impliquée dans la coordination et l’équilibre. Sur 24 heures, la quantité de traceur dans le sang diminuait régulièrement dans les deux groupes, mais le rapport signal cérébral / signal sanguin augmentait davantage chez les souris enflammées. Ce schéma indique qu’une plus grande quantité de la grosse protéine traversait la barrière et restait dans le tissu cérébral de ces animaux.
Vérifier le cerveau après le scan
Pour confirmer les images, les chercheurs ont examiné les organes après la dernière séance d’imagerie. Ils ont mesuré la radioactivité dans le cerveau, le sang et les principaux organes et ont de nouveau constaté des niveaux plus élevés d’albumine marquée dans les cerveaux des souris enflammées, avec des niveaux similaires dans les organes périphériques pour les deux groupes. Des coupes fines de tissu cérébral ont été colorées et inspectées au microscope, révélant que l’architecture de base du cervelet restait intacte — les couches cellulaires étaient préservées et il n’y avait pas de signes évidents de perte cellulaire. Pour autant, l’autoradiographie numérique, une technique qui cartographie la radioactivité dans les coupes de tissu, montrait un signal plus marqué dans le cervelet des souris enflammées, reflétant les résultats du PET. Ensemble, ces résultats suggèrent que des fuites de la barrière étaient déjà présentes même si les mesures structurelles standard semblaient normales.
Ce que cela signifie pour la prise en charge future du cerveau
Cette étude pilote suggère qu’un traceur d’albumine radiomarquée, combiné à l’imagerie PET/IRM, peut détecter avec sensibilité des changements précoces dans la barrière protectrice du cerveau lors d’une inflammation chronique, en particulier dans des régions comme le cervelet. La méthode a détecté des fuites subtiles de grosses molécules avant qu’un dommage tissulaire clair n’apparaisse à l’IRM ou à l’examen microscopique de routine. Bien que l’étude ait été réalisée sur un petit nombre de souris et présente certaines contraintes techniques — notamment pour les très petits vaisseaux sanguins — l’approche pourrait à terme aider les médecins à surveiller l’état de la barrière chez les personnes atteintes de maladies neuroinflammatoires ou suite à un traumatisme cérébral. En termes simples, elle offre un moyen de voir la barrière du cerveau commencer à céder, ouvrant la voie à un diagnostic plus précoce et potentiellement à des traitements plus précoces et mieux ciblés.
Citation: Hilbrig, C.F., Baumann, B., Sievert, W. et al. Detection of inflammation-related blood–brain barrier dysfunction using PET and MR imaging: a pilot study. Sci Rep 16, 12014 (2026). https://doi.org/10.1038/s41598-026-47352-6
Mots-clés: barrière hémato‑encéphalique, neuroinflammation, PET IRM, traceur d’albumine, imagerie cérébrale