Clear Sky Science · pt
Correlações processo-propriedade em microfluídica de formulações de nanopartículas lipídicas com dsRNA
Novas ferramentas para proteção de culturas mais segura
Agricultores ao redor do mundo lutam para proteger as plantações de insetos sem prejudicar abelhas, borboletas e outras espécies benéficas. Este estudo explora uma nova forma de proteger plantas usando um sinal natural de silenciamento génico, envolto em partículas minúsculas à base de gordura para que possa sobreviver tempo suficiente para atuar no campo. O objetivo é um pulverizador que vise apenas insetos nocivos, reduza a dependência de venenos de largo espectro e possa ser produzido a baixo custo em escala industrial.
Por que um sussurro genético pode substituir um ataque químico
Muitos inseticidas modernos matam uma ampla gama de espécies e podem persistir no solo, na água e nas cadeias alimentares. Em contraste, a interferência por RNA (RNAi) age como um sussurro genético: moléculas de RNA de fita dupla (dsRNA) são desenhadas para corresponder a um gene vital apenas no inseto-praga. Quando ingeridas, elas acionam a degradação do mensageiro desse gene, eventualmente matando a praga enquanto preservam a maior parte das outras espécies. Porém, essas fitas de dsRNA são frágeis. Luz solar, enzimas na superfície das folhas e condições agressivas no intestino do inseto podem destruí‑las em poucas horas. Para transformar a RNAi em um spray prático para o campo, o dsRNA precisa ser protegido tempo suficiente para ser ingerido e liberado dentro das células do inseto.
Casulos protetores minúsculos feitos de ingredientes acessíveis
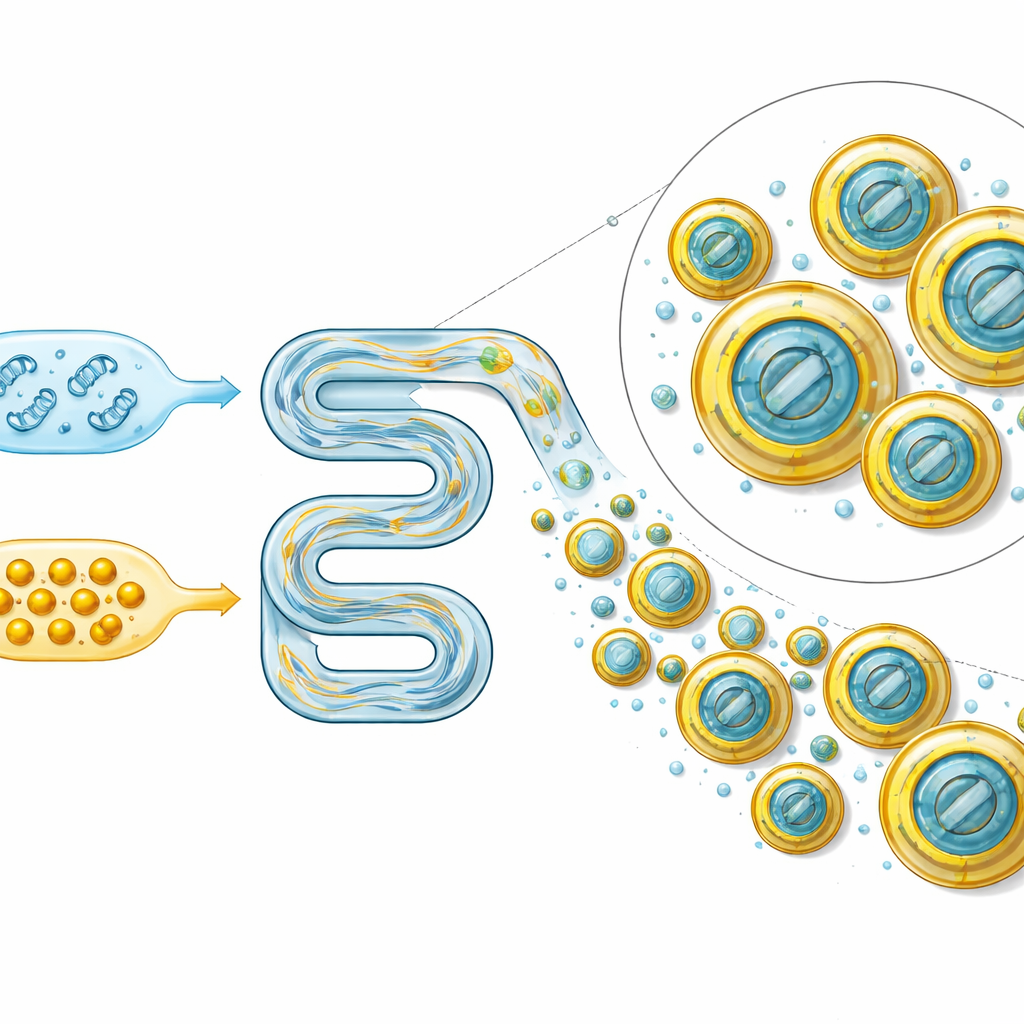
Empresas farmacêuticas já protegem RNA médico com nanopartículas lipídicas — esferas em escala nanométrica feitas de moléculas gordurosas. Mas os lipídios especiais usados em vacinas são caros demais para aplicação em grandes áreas agrícolas. Os autores, portanto, montaram uma “caixa de ferramentas” com três lipídios de grau técnico já produzidos em escala de toneladas: uma amina gordurosa carregada positivamente para atrair o dsRNA carregado negativamente, um estabilizador contendo PEG para manter as partículas dispersas, e uma mistura de lecitina similar aos emulsificantes alimentares. Usando mistura controlada em canais microfluídicos estreitos, eles ajustaram quanto lipídio adicionar e quão rápido misturar, e então mediram tamanho das partículas, carga superficial e uniformidade por métodos de espalhamento de luz e microscopia eletrônica. Misturas mais rápidas e maior quantidade de lipídio geralmente produziram partículas menores e mais esféricas — em sua maioria abaixo de 100 nanômetros — enquanto lipídio insuficiente levou a aglomerados e formas irregulares.
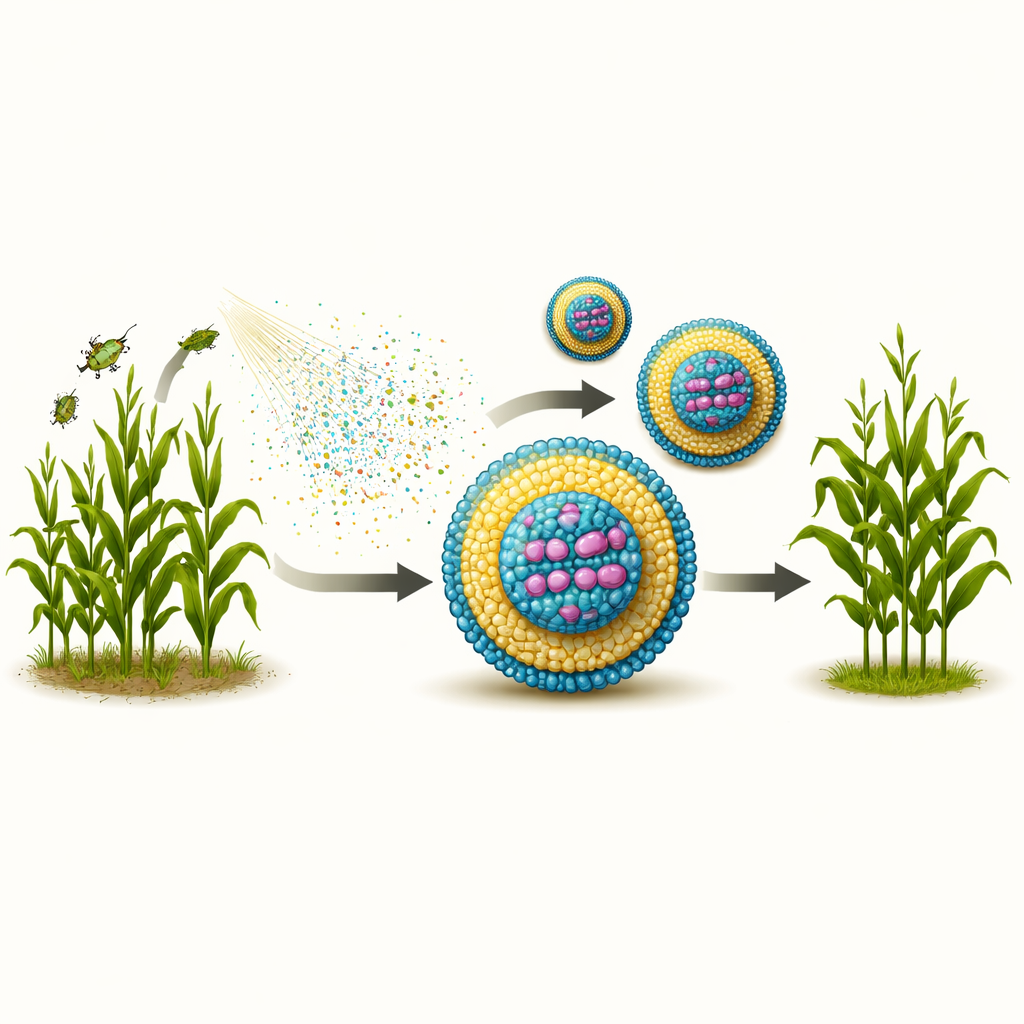
Manter a mensagem genética intacta em condições adversas
Para testar se essas partículas realmente protegem seu conteúdo, a equipe expôs tanto dsRNA nu quanto dsRNA encapsulado em nanopartículas lipídicas a uma enzima degradante (RNase III) e a uma ampla gama de acidez e alcalinidade. Em géis, o dsRNA não protegido praticamente desapareceu após 24 horas com a enzima ou em pH muito baixo e muito alto. Em contraste, todas as receitas de nanopartículas mantiveram o dsRNA intacto por pelo menos um dia sob ataque enzimático, e as fitas genéticas puderam ser recuperadas adicionando um detergente que desmonta as partículas. As formulações também melhoraram muito a sobrevivência do dsRNA em condições ácidas, semelhantes às encontradas nos tratos digestivos de besouros praga importantes. Em condições extremamente alcalinas, as partículas perderam sua carga estabilizadora e precipitaram, de modo que a proteção ficou limitada, mas esses extremos são menos relevantes para o uso típico em campo e para a digestão por insetos.
Do gotejamento no banco de laboratório ao fluxo em escala agrícola
Proteção por si só não é suficiente; qualquer solução prática precisa ser fabricada em grandes volumes a baixo custo. Os pesquisadores, portanto, adaptaram seu processo microfluídico para operar em taxas de fluxo muito mais altas, produzindo centenas de mililitros de formulação em uma única execução — um passo importante rumo a lotes em escala piloto. Variando sistematicamente as proporções dos três lipídios enquanto mantinham constante a razão lipídio-dsRNA geral, eles mapearam como mudanças na receita afetavam o tamanho das partículas e a carga superficial. Em seguida, usaram uma técnica calorimétrica para examinar quão facilmente um detergente poderia extrair o dsRNA de volta das partículas. As medições de energia mostraram que a liberação foi moderada e impulsionada principalmente pelo desordenamento do sistema lipídio–água, sugerindo que o dsRNA pode ser firmemente protegido e, ainda assim, liberado sob as condições adequadas.
Rumo a um controle de pragas mais inteligente e direcionado
Em termos simples, este trabalho demonstra que é possível construir pequenas cascas protetoras bem comportadas ao redor de sinais de silenciamento genético usando ingredientes baratos e escaláveis e métodos de mistura de alto rendimento. Essas partículas mantêm a mensagem do dsRNA protegida de enzimas e acidez agressiva tempo suficiente para alcançar insetos praga, ao mesmo tempo em que permitem sua liberação quando acionadas. Embora sejam necessários refinamentos adicionais para reduzir o aglomeramento das partículas e testar o desempenho em culturas e insetos reais, o estudo estabelece a base essencial para sprays de RNA prontos para o campo que um dia poderiam substituir muitos inseticidas de amplo espectro por uma ferramenta mais precisa e ambientalmente amigável.
Citação: Geisler, P., Knorr, E., Steiniger, F. et al. Microfluidic process-property correlations of dsRNA lipid nanoparticle formulations. Sci Rep 16, 9653 (2026). https://doi.org/10.1038/s41598-026-44095-2
Palavras-chave: Interferência por RNA, nanopartículas lipídicas, biopesticida, microfluídica, agricultura sustentável