Clear Sky Science · pl
Korelacje procesu i właściwości mikroprzepływowych formulacji LNP z dsRNA
Nowe narzędzia dla bezpieczniejszej ochrony upraw
Rolnicy na całym świecie borykają się z ochroną upraw przed owadami, nie szkodząc przy tym pszczołom, motylom i innym pożytecznym organizmom. Badanie to analizuje nowe podejście do ochrony roślin za pomocą naturalnego sygnału wyciszającego geny, opakowanego w mikroskopijne cząstki lipidowe, dzięki czemu może przetrwać wystarczająco długo, by zadziałać w warunkach polowych. Celem jest oprysk celujący wyłącznie w szkodniki, ograniczający zależność od szeroko działających trucizn i możliwy do taniej produkcji w skali przemysłowej.
Dlaczego genetyczny szept może zastąpić chemiczny szturm
Wiele współczesnych insektycydów zabija szerokie spektrum gatunków i może utrzymywać się w glebie, wodzie i łańcuchach pokarmowych. W przeciwieństwie do tego interferencja RNA (RNAi) działa jak genetyczny szept: dwuniciowe RNA (dsRNA) są projektowane tak, by odpowiadać istotnemu genowi jedynie u danego szkodnika. Po spożyciu wywołują rozkład odpowiedniego informacyjnego RNA (mRNA), co ostatecznie prowadzi do śmierci szkodnika przy oszczędzeniu większości innych gatunków. Jednak dsRNA są kruche — światło słoneczne, enzymy na powierzchni liści i surowe warunki w przewodzie pokarmowym owadów mogą je zniszczyć w ciągu kilku godzin. Aby RNAi stała się praktycznym opryskiem polowym, dsRNA musi być osłonięte wystarczająco długo, by zostało zjedzone i uwolnione w komórkach owada.
Maleńkie ochronne osłonki z tanich składników
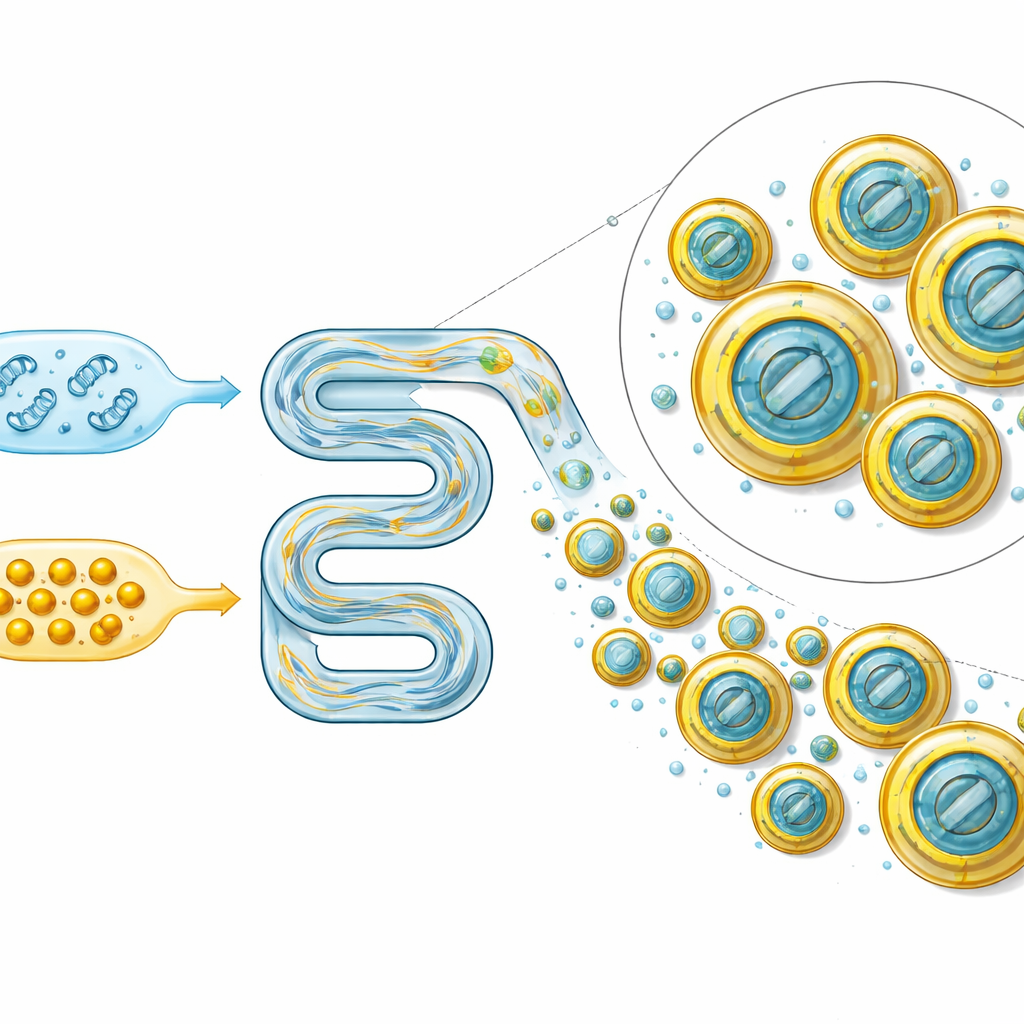
Firmy farmaceutyczne już zabezpieczają medyczne RNA za pomocą lipidowych nanocząstek — nanometrowych sfer zbudowanych z cząsteczek tłuszczowych. Specjalistyczne lipidy stosowane w szczepionkach są jednak zbyt kosztowne do zastosowania na dużych polach. Autorzy zbudowali więc „skrzynkę narzędziową” z trzech technicznych lipidów produkowanych już na skalę tonową: dodatnio naładowanego aminu tłuszczowego, który wiąże ujemnie naładowane dsRNA; stabilizatora zawierającego PEG, który zapobiega zlepianiu cząstek; oraz mieszanki lecytyny podobnej do emulgatorów spożywczych. Stosując kontrolowane mieszanie w wąskich kanałach mikroprzepływowych, dostrajali ilość dodawanego lipidu i prędkość mieszania, a następnie mierzyli rozmiar cząstek, ładunek powierzchniowy i jednorodność metodami rozpraszania światła oraz mikroskopią elektronową. Szybsze mieszanie i większa ilość lipidów zwykle dawały mniejsze, bardziej kuliste cząstki — przeważnie poniżej 100 nanometrów — podczas gdy zbyt mała zawartość lipidu prowadziła do grudek i nieregularnych kształtów.
Utrzymanie integralności informacji genetycznej w trudnych warunkach
Aby sprawdzić, czy te cząstki rzeczywiście chronią ładunek, zespół wystawił zarówno nieosłonięte dsRNA, jak i dsRNA zamknięte w lipidowych nanocząstkach na działanie degradującego enzymu (RNazy III) oraz na szeroki zakres kwaśności i zasadowości. Na żelach niechronione dsRNA praktycznie znikało po 24 godzinach w obecności enzymu lub w bardzo niskim i bardzo wysokim pH. W przeciwieństwie do tego wszystkie receptury nanocząstek utrzymywały dsRNA nienaruszone przez co najmniej dobę pod atakiem enzymatycznym, a nici genetyczne można było odzyskać przez dodanie detergentu rozbijającego cząstki. Formuły znacznie poprawiały też przeżywalność dsRNA w warunkach kwaśnych, podobnych do występujących w układach pokarmowych ważnych chrząszczy szkodników. W ekstremalnie zasadowych warunkach cząstki traciły stabilizujący ładunek i wytrącały się, więc ochrona była ograniczona, ale takie skrajności są mniej istotne dla typowego użytku polowego i trawienia przez owady.
Z kropli zlewu laboratoryjnego do przepływu w skali farmy
Sama ochrona to za mało; praktyczne rozwiązanie musi być produkowane w dużych ilościach niskim kosztem. Badacze przystosowali zatem proces mikroprzepływowy do pracy przy znacznie wyższych przepływach, produkując setki mililitrów formulacji w jednym cyklu — ważny krok w kierunku partii pilotażowych. Systematycznie zmieniając proporcje trzech lipidów przy zachowaniu stałego stosunku całkowitego lipidu do dsRNA, odwzorowali, jak zmiany receptury wpływają na rozmiar cząstek i ładunek powierzchniowy. Następnie użyli techniki kalorymetrii, by zbadać, jak łatwo detergent może wydobyć dsRNA z cząstek. Pomiary energii wykazały, że uwolnienie jest umiarkowane i w dużej mierze napędzane zaburzeniem uporządkowania układu lipid–woda, co sugeruje, że dsRNA może być solidnie chronione, a jednocześnie uwalniane w odpowiednich warunkach.
W kierunku mądrzejszej, celowanej ochrony przed szkodnikami
Mówiąc prosto, praca ta pokazuje, że możliwe jest zbudowanie małych, dobrze zachowujących się osłonek ochronnych wokół sygnałów wyciszających geny, używając tanich, skalowalnych składników i metod szybkiego mieszania. Te cząstki chronią wiadomość dsRNA przed enzymami i silną kwasowością na tyle długo, by dotrzeć do owadów-szkodników, a jednocześnie pozwalają na jej uwolnienie po spełnieniu właściwych warunków. Choć potrzebne są dalsze udoskonalenia w celu zmniejszenia zlepiania cząstek i przetestowania skuteczności na rzeczywistych uprawach i owadach, badanie to stanowi istotne podstawy dla oprysków RNA gotowych do użycia w terenie, które mogą kiedyś zastąpić wiele szerokozakresowych insektycydów bardziej precyzyjnym i przyjaźniejszym dla środowiska narzędziem.
Cytowanie: Geisler, P., Knorr, E., Steiniger, F. et al. Microfluidic process-property correlations of dsRNA lipid nanoparticle formulations. Sci Rep 16, 9653 (2026). https://doi.org/10.1038/s41598-026-44095-2
Słowa kluczowe: Interferencja RNA, lipidowe nanocząstki, biopestycyd, mikroprzepływy, rolnictwo zrównoważone