Clear Sky Science · it
Correlazioni fra procedimento e proprietà nelle formulazioni di nanoparticelle lipidiche per dsRNA
Nuovi strumenti per una protezione delle colture più sicura
Agricoltori di tutto il mondo affrontano la sfida di proteggere le colture dagli insetti senza danneggiare api, farfalle e altri organismi utili. Questo studio esplora un nuovo modo di salvaguardare le piante usando un segnale naturale di silenziamento genico, racchiuso in piccolissime particelle lipidiche in modo che possa sopravvivere abbastanza a lungo da agire sul campo. L’obiettivo è uno spray che colpisca solo gli insetti dannosi, riduca la dipendenza da veleni ad ampio spettro e possa essere prodotto a basso costo su scala industriale.
Perché un sussurro genetico può sostituire un’esplosione chimica
Molti insetticidi moderni uccidono un’ampia gamma di specie e possono persistere nel suolo, nell’acqua e nelle catene alimentari. Al contrario, l’interferenza a RNA (RNAi) funziona come un sussurro genetico: molecole di RNA a doppio filamento (dsRNA) sono progettate per corrispondere a un gene vitale solo nell’insetto bersaglio. Quando ingerite, attivano la degradazione dell’mRNA di quel gene, portando infine alla morte del parassita mentre la maggior parte delle altre specie rimane risparmiata. Tuttavia, questi filamenti di dsRNA sono fragili. Luce solare, enzimi presenti sulle superfici fogliari e le condizioni aggressive nell’intestino degli insetti possono distruggerli in poche ore. Per rendere l’RNAi un prodotto pratico per uso in campo, il dsRNA deve essere protetto abbastanza a lungo da essere ingerito e rilasciato all’interno delle cellule dell’insetto.
Piccole corazze protettive fatte con ingredienti economici
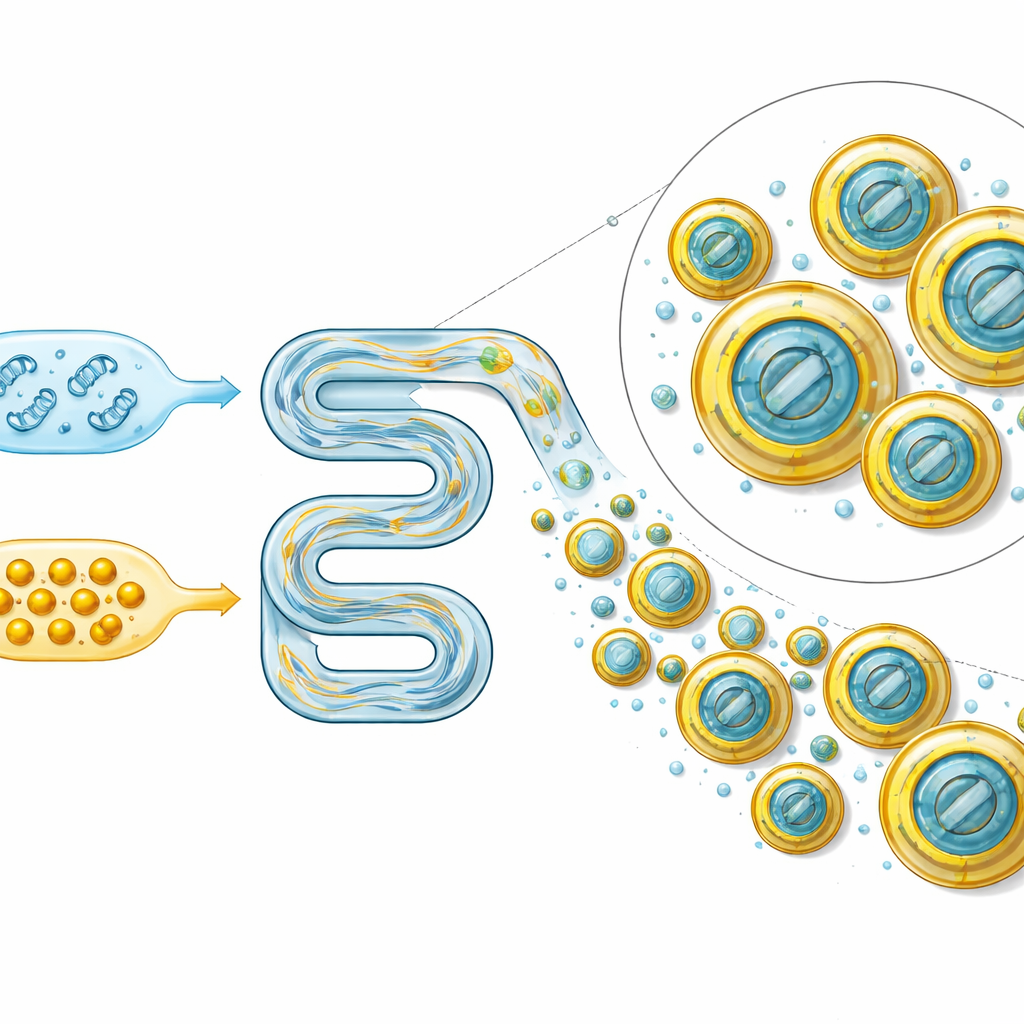
Le aziende farmaceutiche proteggono già l’RNA medico con nanoparticelle lipidiche—sfere a scala nanometrica composte da molecole grasse. Ma i lipidi specialistici usati nei vaccini sono troppo costosi per l’impiego su ampie superfici agricole. Gli autori hanno quindi costruito una “cassetta degli attrezzi” di tre lipidi tecnici prodotti già su scala di tonnellate: un ammina grassa carica positivamente per legare il dsRNA carico negativamente, uno stabilizzante contenente PEG per mantenere le particelle disperse, e una miscela di lecitine simile agli emulsionanti alimentari. Usando miscelazione controllata in canali microfluidici stretti, hanno regolato la quantità di lipide aggiunta e la velocità di miscelazione, quindi hanno misurato dimensione delle particelle, carica superficiale e uniformità con metodi di diffusione della luce e microscopia elettronica. Miscele più veloci e maggior contenuto di lipidi hanno generalmente prodotto particelle più piccole e sferiche—per lo più sotto i 100 nanometri—mentre troppo poco lipide ha portato a aggregati e forme irregolari.
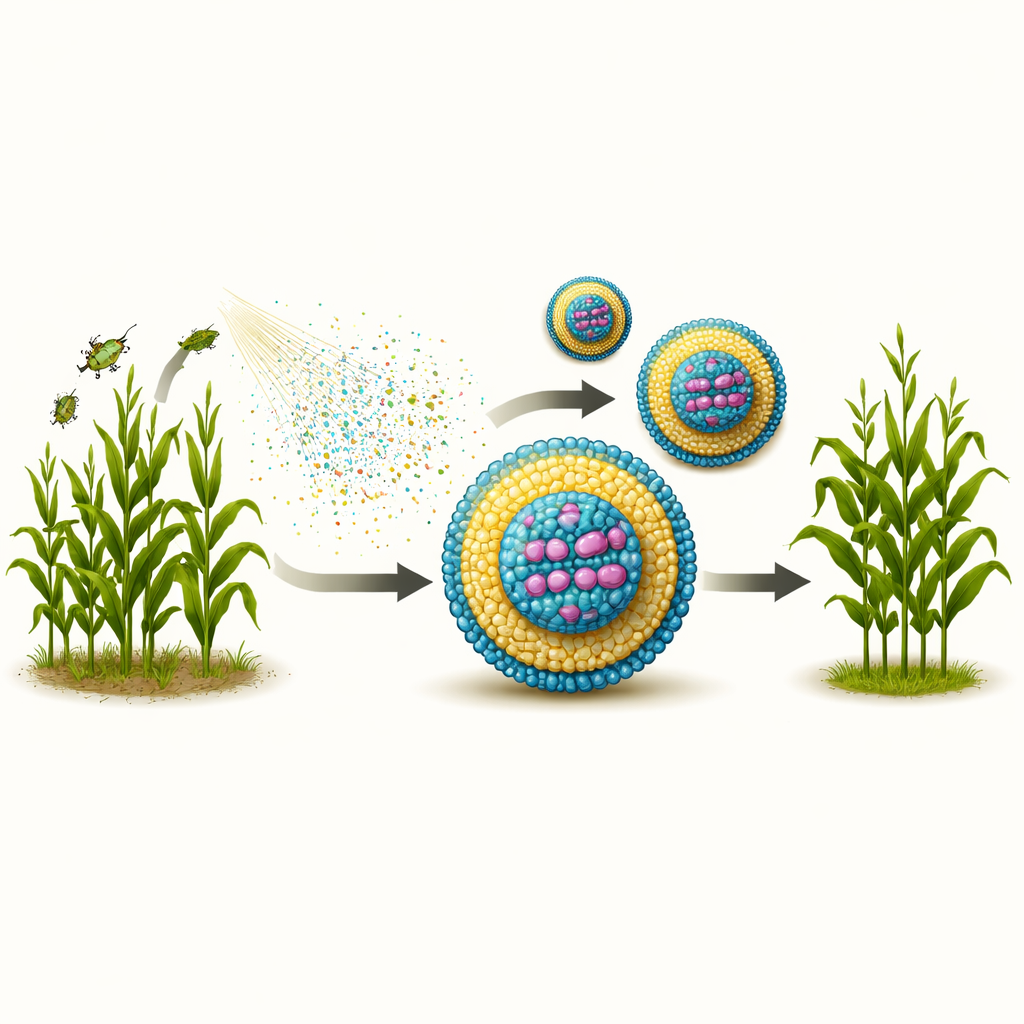
Mantenere intatto il messaggio genetico in condizioni ostili
Per verificare se queste particelle proteggessero davvero il carico, il team ha esposto sia il dsRNA nudo sia il dsRNA racchiuso in nanoparticelle lipidiche a un enzima degradante (RNase III) e a un ampio spettro di acidità e alcalinità. Su gel, il dsRNA non protetto scompariva sostanzialmente dopo 24 ore con l’enzima o a pH molto acidi e molto alcalini. Al contrario, tutte le ricette di nanoparticelle hanno mantenuto il dsRNA integro per almeno un giorno sotto attacco enzimatico, e i filamenti genetici sono stati recuperabili aggiungendo un detergente che disfa le particelle. Le formulazioni hanno inoltre migliorato notevolmente la sopravvivenza del dsRNA in condizioni acide, simili a quelle presenti nell’intestino di coleotteri dannosi. In condizioni estremamente alcaline le particelle perdevano la carica stabilizzante e precipitavano, quindi la protezione era limitata, ma tali estremi sono meno rilevanti per l’uso tipico in campo e per la digestione degli insetti.
Dalla goccia in laboratorio al flusso su scala agricola
La protezione da sola non basta; qualsiasi soluzione pratica deve poter essere prodotta in grandi volumi a basso costo. I ricercatori hanno quindi adattato il loro processo microfluidico per operare a flussi molto più elevati, producendo centinaia di millilitri di formulazione in una singola corsa—un passo importante verso lotti su scala pilota. Variando sistematicamente le proporzioni dei tre lipidi mantenendo costante il rapporto complessivo lipidi/dsRNA, hanno mappato come le modifiche della ricetta influenzassero dimensione delle particelle e carica superficiale. Hanno poi usato una tecnica calorimetrica per esaminare quanto facilmente un detergente poteva estrarre il dsRNA dalle particelle. Le misure energetiche hanno mostrato che il rilascio era moderato e guidato in gran parte dal disordine del sistema lipidi-acqua, suggerendo che il dsRNA può essere saldamente protetto ma comunque liberabile nelle giuste condizioni.
Verso un controllo dei parassiti più intelligente e mirato
In termini concreti, questo lavoro dimostra che è possibile costruire piccole corazze protettive ben comportate attorno a segnali di silenziamento genico usando ingredienti economici e scalabili e metodi di miscelazione ad alto rendimento. Queste particelle mantengono il messaggio dsRNA al sicuro dagli enzimi e dall’acidità aggressiva abbastanza a lungo da raggiungere gli insetti nocivi, pur permettendone il rilascio se opportunamente innescato. Sebbene siano necessari ulteriori perfezionamenti per ridurre l’aggregazione delle particelle e per testare le prestazioni su colture e insetti reali, lo studio pone le basi essenziali per spray a base di RNA pronti per il campo che un giorno potrebbero sostituire molti insetticidi ad ampio spettro con uno strumento più preciso e rispettoso dell’ambiente.
Citazione: Geisler, P., Knorr, E., Steiniger, F. et al. Microfluidic process-property correlations of dsRNA lipid nanoparticle formulations. Sci Rep 16, 9653 (2026). https://doi.org/10.1038/s41598-026-44095-2
Parole chiave: Interferenza a RNA, nanoparticelle lipidiche, biopesticida, microfluidica, agricoltura sostenibile