Clear Sky Science · de
Prozess-Eigenschafts-Korrelationen mikrofluidischer dsRNA-Lipid-Nanopartikel-Formulierungen
Neue Werkzeuge für sichereren Pflanzenschutz
Bäuerinnen und Bauern weltweit kämpfen damit, Pflanzen vor Insekten zu schützen, ohne Bienen, Schmetterlinge und andere nützliche Organismen zu schädigen. Diese Studie untersucht einen neuen Ansatz, Pflanzen mit einem natürlichen, Gen-stilllegenden Signal zu schützen, das in winzigen, fettbasierten Partikeln verpackt ist, damit es im Feld lange genug überlebt, um zu wirken. Ziel ist eine Sprühlösung, die nur schädliche Insekten anspricht, die Abhängigkeit von breit wirkenden Giften reduziert und sich kostengünstig im Industriemaßstab herstellen lässt.
Warum ein genetisches Flüstern einen chemischen Sprengstoß ersetzen kann
Viele moderne Insektizide töten eine breite Palette von Arten und können im Boden, Wasser und in Nahrungsketten verweilen. Im Gegensatz dazu wirkt RNA-Interferenz (RNAi) wie ein genetisches Flüstern: Doppelsträngige RNA (dsRNA)-Moleküle werden so entworfen, dass sie mit einem lebenswichtigen Gen eines Schadinsekts übereinstimmen. Beim Verschlucken lösen sie den Abbau der entsprechenden Boten-RNA aus und töten schließlich den Schädling, während die meisten anderen Arten verschont bleiben. Diese dsRNA-Stränge sind jedoch sehr empfindlich. Sonnenlicht, Enzyme auf Blattoberflächen und harte Bedingungen im Insektenmagen können sie innerhalb weniger Stunden zerstören. Damit RNAi als praktische Feldspritze funktioniert, muss die dsRNA gerade lange genug geschützt werden, um aufgenommen und innerhalb der Insektenzellen freigesetzt zu werden.
Winzige Schutzhüllen aus preiswerten Zutaten
Pharmafirmen schützen medizinische RNA bereits mit Lipidnanopartikeln—Nanoskalen-Kugeln aus fettähnlichen Molekülen. Die spezialisierten Lipide, die in Impfstoffen verwendet werden, sind jedoch zu teuer für den Einsatz auf großen Feldern. Die Autoren bauten daher eine „Werkzeugkiste“ aus drei technisch-hergestellten Lipiden, die bereits in Tonnenmengen produziert werden: ein positiv geladenes Fettamin, das die negativ geladene dsRNA fängt, ein PEG-haltiger Stabilisator, der die Partikel dispergiert hält, und eine Lecithin-Mischung ähnlich den Lebensmittelemulgatoren. Durch kontrolliertes Mischen in engen mikrofluidischen Kanälen variierten sie die zugefügte Lipidmenge und die Mischgeschwindigkeit und bestimmten dann Partikelgröße, Oberflächenladung und Gleichmäßigkeit mit lichtstreuenden Methoden und Elektronenmikroskopie. Schnelleres Mischen und mehr Lipid führten im Allgemeinen zu kleineren, sphärischeren Partikeln—zumeist unter 100 Nanometern—während zu wenig Lipid zu Klumpen und unregelmäßigen Formen führte.
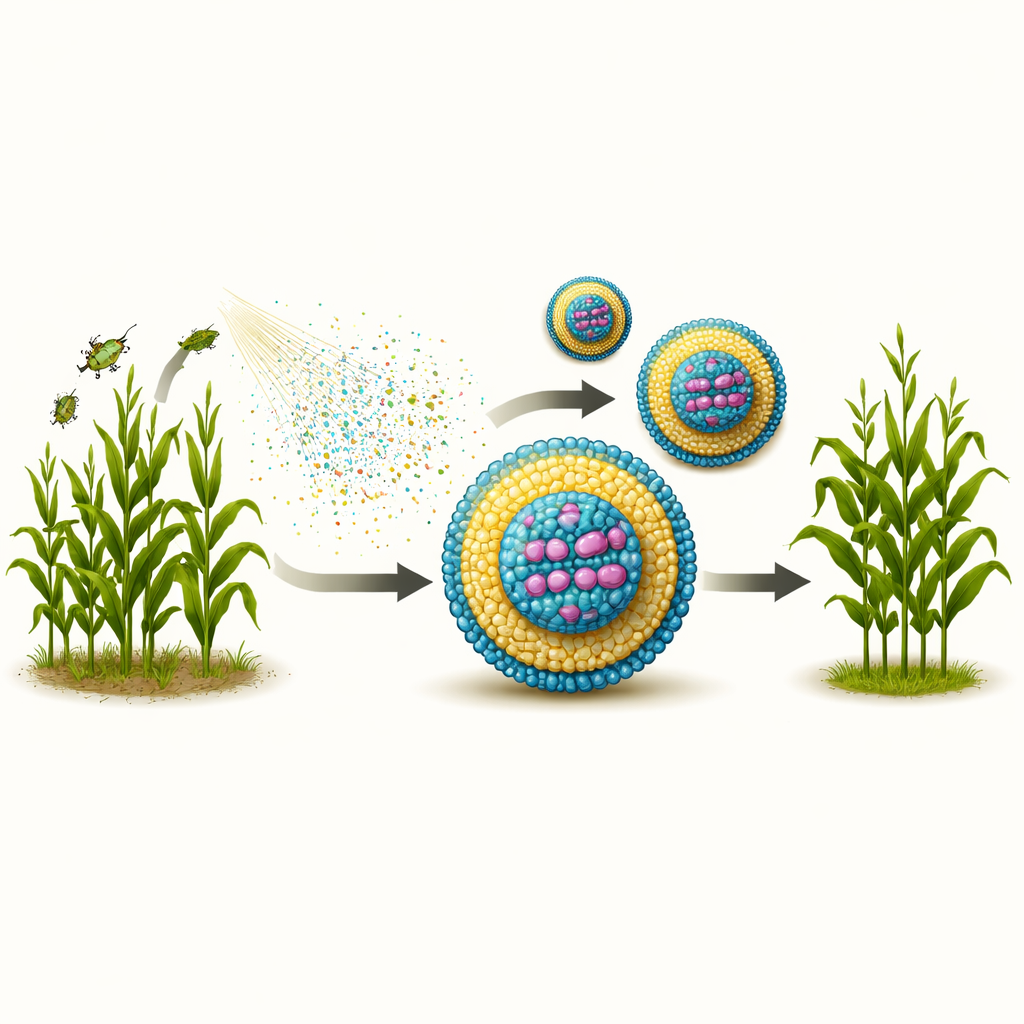
Die genetische Botschaft unter rauen Bedingungen intakt halten
Um zu prüfen, ob diese Partikel ihren Frachtstoff wirklich schützen, setzte das Team sowohl ungeschützte dsRNA als auch dsRNA innerhalb von Lipidnanopartikeln einem abbauenden Enzym (RNase III) und einem breiten pH-Spektrum aus. Auf Gelen verschwand die ungeschützte dsRNA nach 24 Stunden beim Enzymangriff oder bei sehr niedrigem bzw. sehr hohem pH-Wert praktisch vollständig. Im Gegensatz dazu hielten alle Nanopartikel-Rezepturen die dsRNA bei Enzymexposition mindestens einen Tag lang intakt, und die genetischen Stränge konnten durch Zugabe eines Detergens, das die Partikel auseinanderzieht, wiedergewonnen werden. Die Formulierungen verbesserten zudem das Überleben der dsRNA unter sauren Bedingungen erheblich, ähnlich denen im Verdauungstrakt wichtiger Käfer-Schädlinge. Bei extrem alkalischen Bedingungen verloren die Partikel jedoch ihre stabilisierende Ladung und fielen aus, sodass der Schutz begrenzt war—diese Extreme sind für typischen Feldeinsatz und Insektenverdau aber weniger relevant.
Vom Laborfluss zum landwirtschaftlichen Maßstab
Schutz allein reicht nicht aus; eine praktikable Lösung muss in großen Mengen zu niedrigen Kosten herstellbar sein. Die Forschenden passten daher ihren mikrofluidischen Prozess an, um mit deutlich höheren Flussraten zu arbeiten und Hunderte Milliliter Formulierung in einem Durchlauf zu produzieren—ein wichtiger Schritt in Richtung Pilotmaßstab. Durch systematisches Variieren der Anteile der drei Lipide bei gleichzeitig konstantem Gesamt-Lipid-zu-dsRNA-Verhältnis kartierten sie, wie Rezeptänderungen Partikelgröße und Oberflächenladung beeinflussen. Anschließend nutzten sie eine kalorimetrische Technik, um zu untersuchen, wie leicht ein Detergens die dsRNA wieder aus den Partikeln lösen kann. Die Energiemessungen zeigten, dass die Freisetzung moderat ist und weitgehend durch die Entordnung des Lipid-Wasser-Systems angetrieben wird, was darauf hindeutet, dass dsRNA fest geschützt sein kann, aber unter den richtigen Bedingungen dennoch freigesetzt werden kann.
Auf dem Weg zu intelligenterem, zielgerichtetem Schädlingsschutz
Einfach gesagt zeigt diese Arbeit, dass es möglich ist, kleine, gut kontrollierte Schutzhüllen um Gen-stilllegende Signale zu bauen, und zwar mit kostengünstigen, skalierbaren Zutaten und Hochdurchsatz-Mischverfahren. Diese Partikel bewahren die dsRNA-Botschaft vor Enzymen und starker Säure lange genug, um Insekten-Schädlinge zu erreichen, und erlauben dennoch deren Freisetzung bei Auslösung. Obwohl weitere Verbesserungen nötig sind, um Partikelverklebungen zu reduzieren und die Leistung an echten Feldkulturen und Insekten zu testen, schafft die Studie die wesentlichen Grundlagen für feldtaugliche RNA-Sprays, die eines Tages viele Breitband-Insektizide durch ein präziseres und umweltfreundlicheres Werkzeug ersetzen könnten.
Zitation: Geisler, P., Knorr, E., Steiniger, F. et al. Microfluidic process-property correlations of dsRNA lipid nanoparticle formulations. Sci Rep 16, 9653 (2026). https://doi.org/10.1038/s41598-026-44095-2
Schlüsselwörter: RNA-Interferenz, Lipidnanopartikel, Biopestizid, Mikrofluidik, nachhaltige Landwirtschaft