Clear Sky Science · pt
Compreendendo a química de inserção de CO2 em baixa pressão na catálise de copolimerização epóxido–CO2
Transformando gás residual em materiais do dia a dia
O dióxido de carbono (CO2) é geralmente visto como um gás residual que aquece nosso planeta, mas químicos estão aprendendo a transformá‑lo em plásticos úteis. O problema é que a maioria dos processos atuais exige que o CO2 seja comprimido a altas pressões, o que custa dinheiro e energia. Este artigo investiga como produzir plásticos à base de CO2 de forma eficiente em pressões muito mais baixas, apontando caminhos para uma fabricação mais sustentável de materiais usados em adesivos, baterias e plásticos flexíveis.
Por que a pressão importa na química verde
Para reciclar CO2 em plásticos, os químicos usam catalisadores—moléculas especiais que ajudam a ligar o CO2 a pequenos blocos de construção chamados epóxidos para formar longas cadeias de policarbonato. Indústrias costumam conduzir essas reações em altas pressões de CO2 para obter boas velocidades e qualidade do produto, mas comprimir gás consome muita energia e é caro. Os autores usam simulações de processo para mostrar que aumentar a pressão de CO2 de níveis modestos para altos pode elevar o consumo de energia para um plástico chave, o poli(propileno carbonato), em mais de 200%. Isso torna a operação em baixa pressão crucial se os plásticos à base de CO2 devem ser ao mesmo tempo favoráveis ao clima e atraentes comercialmente.
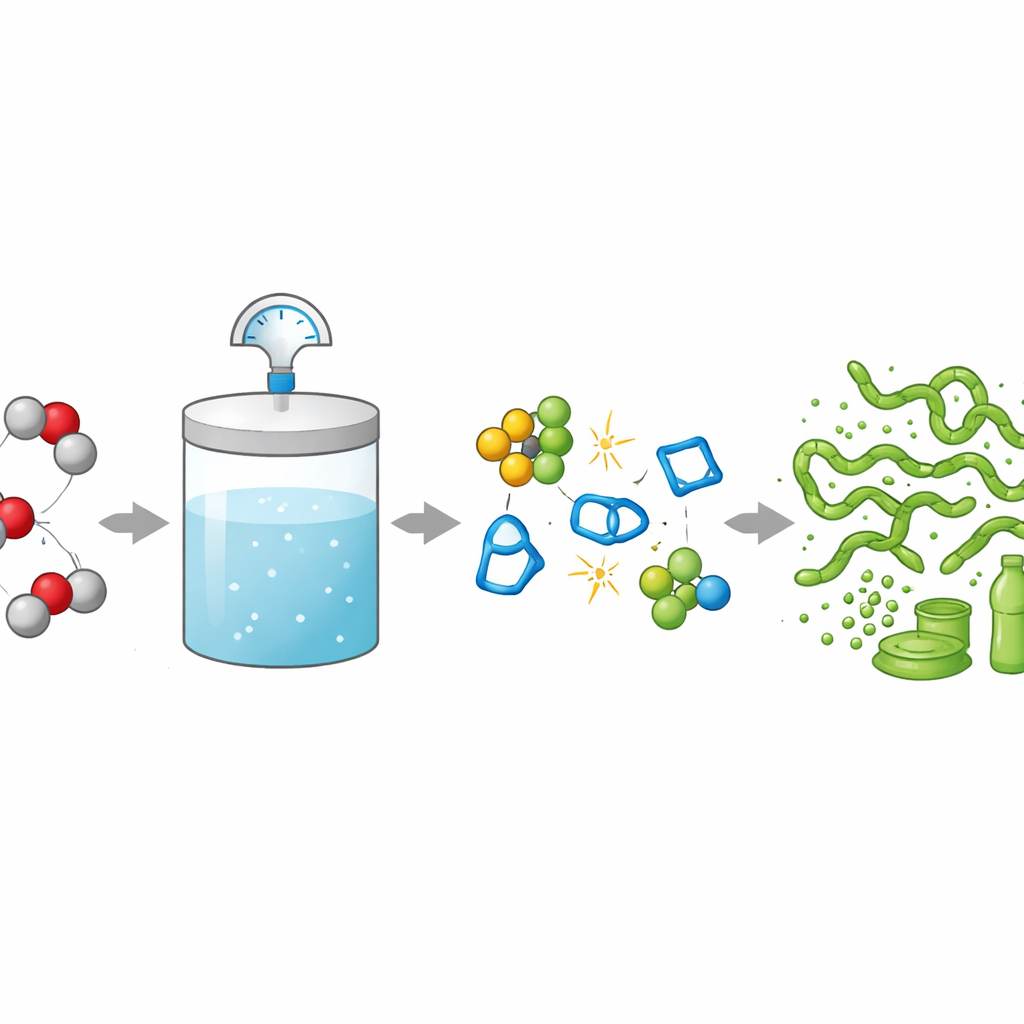
Investigando a etapa oculta na reação
Uma etapa crítica, porém pouco compreendida, em muitos processos à base de CO2 é a “inserção” do CO2: o CO2 reage com uma ligação metal–oxigênio dentro do catalisador para formar uma nova espécie metal–carbonato. Essa etapa costuma ser presumida rápida e irrelevante para a velocidade global, por isso raramente foi examinada em condições reais de produção. A equipe escolheu uma reação amplamente estudada—copolimerização por abertura de anel do CO2 com epóxidos como óxido de propeno e óxido de ciclohexeno—para estudar essa etapa de inserção. Selecionaram cinco dos catalisadores à base de cobalto mais conhecidos, que já funcionam em pressões relativamente baixas e temperaturas moderadas, e então realizaram testes sistemáticos entre 2 e 30 bar de CO2 acompanhando cuidadosamente a velocidade de formação do polímero.
Descobrindo um equilíbrio dependente da pressão
Em todos os cinco catalisadores, as velocidades de reação mostraram dois regimes claros. Em baixa pressão de CO2, a velocidade aumentava de forma constante com a pressão: mais CO2 deslocava o equilíbrio dentro do catalisador de uma forma metal–alóxido para uma forma metal–carbonato que efetivamente realiza a etapa chave de formação de ligações. Acima de uma pressão “limiar” específica para cada catalisador, adicionar mais CO2 deixou de ajudar—a velocidade se estabilizou porque quase todas as moléculas do catalisador já estavam na forma carbonato ativa. A partir dessas medições, os autores extraíram dois números práticos para cada catalisador: uma constante de equilíbrio, que mede a força com que o CO2 é inserido no catalisador, e uma pressão limiar, a pressão mínima de CO2 necessária para atingir a velocidade máxima.
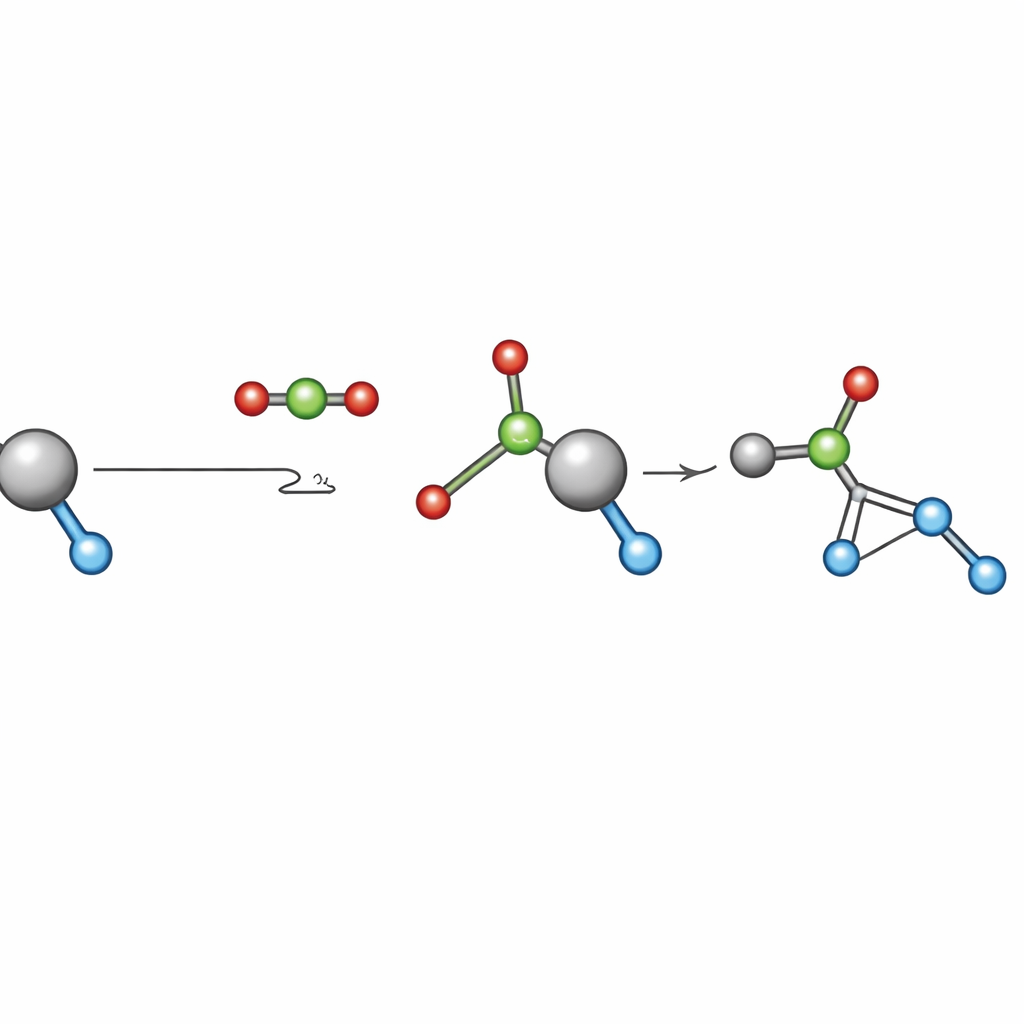
De números fundamentais a regras de projeto
Quando os pesquisadores compararam os catalisadores, surgiu um padrão simples. Catalisadores com maiores constantes de equilíbrio de inserção de CO2 reagiam mais rápido e atingiam suas velocidades máximas em pressões menores. Desempenhos piores apresentavam inserção mais fraca e precisavam de pressões de CO2 mais altas para trabalhar melhor. Essas correlações se mantiveram não apenas entre diferentes complexos de cobalto, mas também ao trocar o epóxido usado como monômero. A equipe demonstrou que, medindo a velocidade de reação em apenas uma pressão moderada (5 bar), era possível prever tanto a constante de equilíbrio quanto a pressão limiar para aquele par catalisador–monômero. Eles confirmaram essas previsões experimentalmente com catalisadores adicionais, incluindo um sistema de metais mistos, e descobriram que um catalisador de destaque já podia operar eficientemente abaixo de 5 bar para certos monômeros.
Orientando futuras tecnologias de reciclagem de CO2
Para um leitor não especialista, a conclusão chave é que os autores transformaram uma etapa microscópica complexa—o CO2 se inserindo numa ligação metal–oxigênio—em dois números simples e mensuráveis que dizem aos engenheiros como operar um processo com energia mínima. Ao vincular a estrutura do catalisador à força de inserção do CO2 e à pressão operacional necessária, o trabalho oferece um roteiro para projetar catalisadores de próxima geração que funcionem de forma rápida, limpa e em baixa pressão. Essa abordagem pode acelerar o desenvolvimento de tecnologias escaláveis de conversão de CO2 em plásticos, ajudando a transformar um importante gás de efeito estufa em produtos úteis com custos energéticos e climáticos muito menores.
Citação: Thorogood, R., Eisenhardt, K.H.S., Smith, M.L. et al. Understanding low-pressure CO2 insertion chemistry in epoxide–CO2 copolymerization catalysis. Nat. Chem. 18, 931–938 (2026). https://doi.org/10.1038/s41557-026-02098-6
Palavras-chave: utilização de dióxido de carbono, catálise em baixa pressão, plásticos de policarbonato, copolimerização de epóxidos, química verde