Clear Sky Science · fr
Comprendre la chimie d’insertion du CO2 à basse pression dans la catalyse de copolymérisation époxyde–CO2
Transformer un gaz résiduel en matériaux du quotidien
Le dioxyde de carbone (CO2) est généralement perçu comme un gaz résiduel qui réchauffe notre planète, mais les chimistes apprennent à en faire des plastiques utiles. Le problème, c’est que la plupart des procédés actuels exigent de comprimer le CO2 à de fortes pressions, ce qui coûte de l’argent et de l’énergie. Cet article explore comment fabriquer des plastiques à base de CO2 de manière efficace à des pressions bien plus basses, ouvrant la voie à une production plus verte de matériaux utilisés dans les adhésifs, les batteries et les plastiques flexibles.
Pourquoi la pression compte en chimie durable
Pour recycler le CO2 en plastiques, les chimistes utilisent des catalyseurs — des molécules spéciales qui aident à lier le CO2 à de petits blocs de construction appelés époxydes pour former de longues chaînes de polycarbonate. Les usines industrielles font souvent fonctionner ces réactions à des pressions élevées de CO2 pour obtenir des vitesses et une qualité de produit satisfaisantes, mais comprimer un gaz consomme beaucoup d’énergie et coûte cher. Les auteurs montrent, par des simulations de procédé, qu’augmenter la pression de CO2 de niveaux modestes à élevés peut accroître la consommation d’énergie pour un plastique clé, le poly(propylène carbonate), de plus de 200 %. Cela rend l’exploitation à basse pression cruciale si les plastiques à base de CO2 doivent être à la fois favorables au climat et commercialement attractifs.
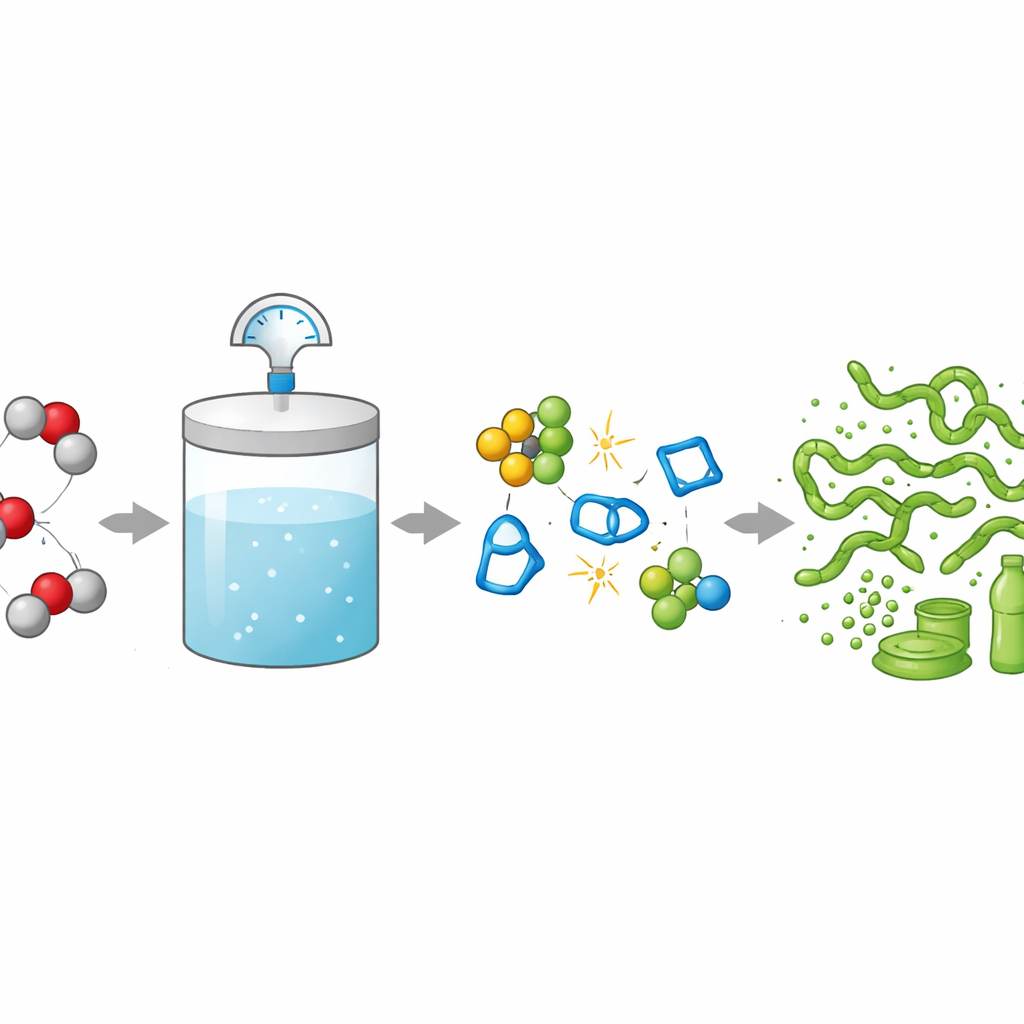
Explorer l’étape cachée de la réaction
Une étape critique mais mal comprise dans de nombreux procédés à base de CO2 est l’« insertion » du CO2 : le CO2 réagit avec une liaison métal–oxygène à l’intérieur du catalyseur pour former une nouvelle espèce métal–carbonate. Cette étape est souvent supposée rapide et peu importante pour la vitesse globale, et a donc rarement été étudiée dans des conditions proches de la production réelle. L’équipe a choisi une réaction largement étudiée — la copolymérisation par ouverture de cycle du CO2 avec des époxydes tels que l’oxyde de propylène et l’oxyde de cyclohexène — pour étudier cette étape d’insertion. Ils ont sélectionné cinq des catalyseurs à base de cobalt les plus connus, qui fonctionnent déjà à des pressions relativement basses et des températures modestes, puis ont réalisé des tests systématiques entre 2 et 30 bars de CO2 tout en suivant attentivement la vitesse de formation du polymère.
Découverte d’un équilibre dépendant de la pression
Pour les cinq catalyseurs, les vitesses de réaction ont montré deux régimes distincts. À basse pression de CO2, la vitesse augmentait régulièrement avec la pression : davantage de CO2 faisait basculer l’équilibre à l’intérieur du catalyseur d’une forme métal–alkoxyde vers une forme métal–carbonate qui réalise effectivement l’étape clé de formation de liaison. Au‑delà d’une pression « seuil » spécifique à chaque catalyseur, ajouter plus de CO2 n’apportait plus d’amélioration — la vitesse plafonnait parce que presque toutes les molécules de catalyseur étaient déjà sous la forme active carbonate. À partir de ces mesures, les auteurs ont extrait deux nombres pratiques pour chaque catalyseur : une constante d’équilibre, qui quantifie la propension à insérer le CO2 dans le catalyseur, et une pression seuil, la pression minimale de CO2 nécessaire pour atteindre la vitesse maximale.
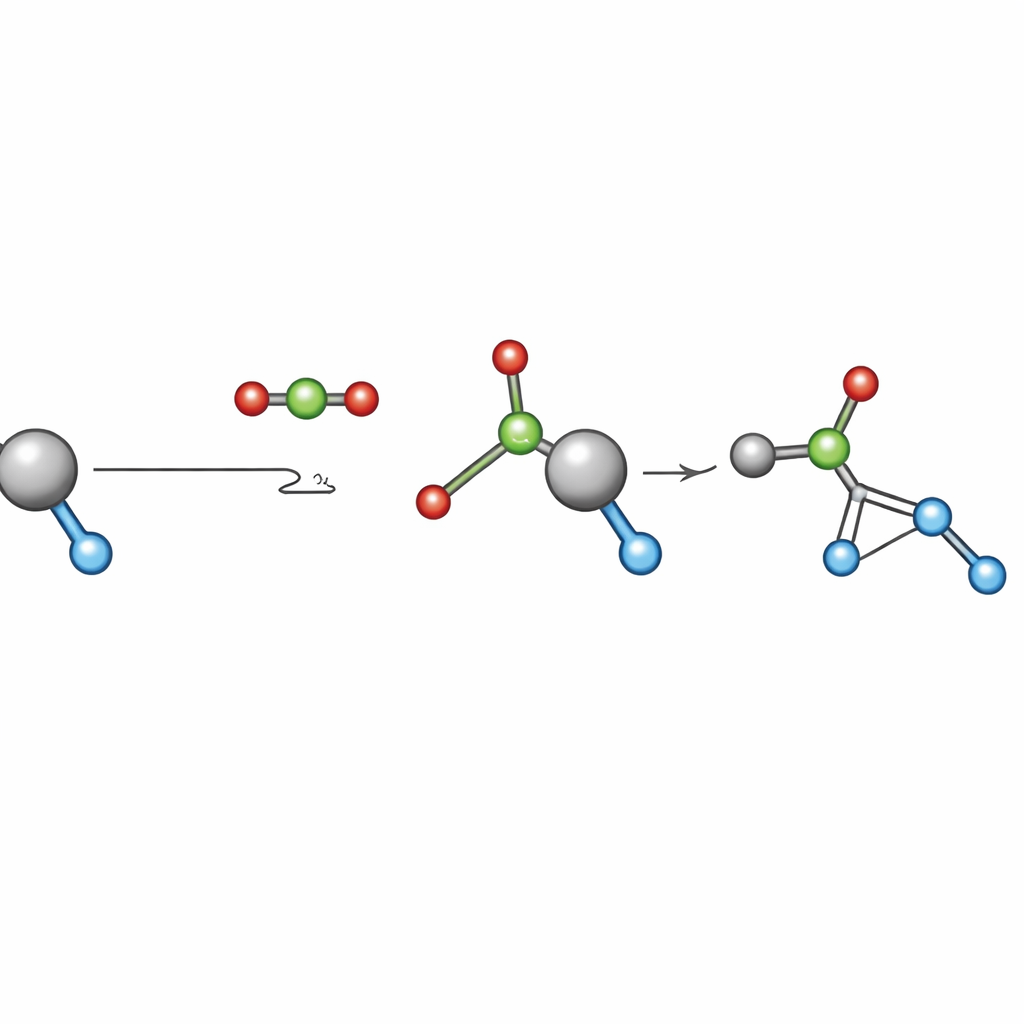
Des nombres fondamentaux aux règles de conception
Lorsque les chercheurs ont comparé les catalyseurs, un schéma simple est apparu. Les catalyseurs ayant des constantes d’insertion du CO2 plus élevées réagissaient plus vite et atteignaient leurs vitesses maximales à des pressions plus faibles. Les performeurs moins bons avaient une insertion plus faible et nécessitaient des pressions de CO2 plus élevées pour donner le meilleur d’eux‑mêmes. Ces corrélations étaient valables non seulement pour différents complexes de cobalt, mais aussi lors du changement du monomère époxyde. L’équipe a montré qu’en mesurant la vitesse de réaction à une seule pression modérée (5 bar), ils pouvaient prédire à la fois la constante d’équilibre et la pression seuil pour la paire catalyseur–monomère considérée. Ils ont confirmé ces prédictions expérimentalement avec des catalyseurs supplémentaires, y compris un système à métaux mixtes, et ont trouvé qu’un catalyseur remarquable pouvait déjà fonctionner efficacement en dessous de 5 bars pour certains monomères.
Orienter les technologies futures de recyclage du CO2
Pour un non‑spécialiste, le résultat clé est que les auteurs ont transformé une étape microscopique complexe — l’insertion du CO2 dans une liaison métal–oxygène — en deux nombres simples et mesurables qui indiquent aux ingénieurs comment piloter un procédé avec une consommation d’énergie minimale. En reliant la structure des catalyseurs à la force d’insertion du CO2 et à la pression de fonctionnement requise, ce travail offre une feuille de route pour concevoir des catalyseurs de nouvelle génération qui fonctionnent rapidement, proprement et à basse pression. Cette approche pourrait accélérer le développement de technologies évolutives de conversion du CO2 en plastiques, aidant à transformer un gaz à effet de serre majeur en produits utiles avec des coûts énergétiques et climatiques bien moindres.
Citation: Thorogood, R., Eisenhardt, K.H.S., Smith, M.L. et al. Understanding low-pressure CO2 insertion chemistry in epoxide–CO2 copolymerization catalysis. Nat. Chem. 18, 931–938 (2026). https://doi.org/10.1038/s41557-026-02098-6
Mots-clés: valorisation du dioxyde de carbone, catalyse à basse pression, plastiques polycarbonate, copolymérisation d’époxydes, chimie verte