Clear Sky Science · es
Comprender la química de inserción de CO2 a baja presión en la catálisis de copolimerización epóxido–CO2
Convertir un gas residual en materiales cotidianos
El dióxido de carbono (CO2) suele verse como un gas residual que calienta el planeta, pero los químicos están aprendiendo a transformarlo en plásticos útiles. El inconveniente es que la mayoría de los procesos actuales requieren comprimir el CO2 a altas presiones, lo que consume dinero y energía. Este artículo explora cómo fabricar plásticos a base de CO2 de forma eficiente a presiones mucho más bajas, marcando el camino hacia una fabricación más ecológica de materiales utilizados en adhesivos, baterías y plásticos flexibles.
Por qué la presión importa en la química verde
Para reciclar CO2 en plásticos, los químicos usan catalizadores—moléculas especiales que ayudan a enlazar el CO2 con pequeños bloques de construcción llamados epóxidos para formar largas cadenas de policarbonato. Las plantas industriales suelen realizar estas reacciones a altas presiones de CO2 para obtener buenas velocidades y calidad del producto, pero comprimir gas requiere mucha energía y resulta caro. Los autores usan simulaciones de proceso para mostrar que aumentar la presión de CO2 de niveles modestos a altos puede incrementar el uso energético para un plástico clave, el poli(propileno carbonato), en más de un 200%. Eso hace que operar a baja presión sea crucial si los plásticos a base de CO2 han de ser tanto climáticamente responsables como atractivos comercialmente.
Investigando el paso oculto de la reacción
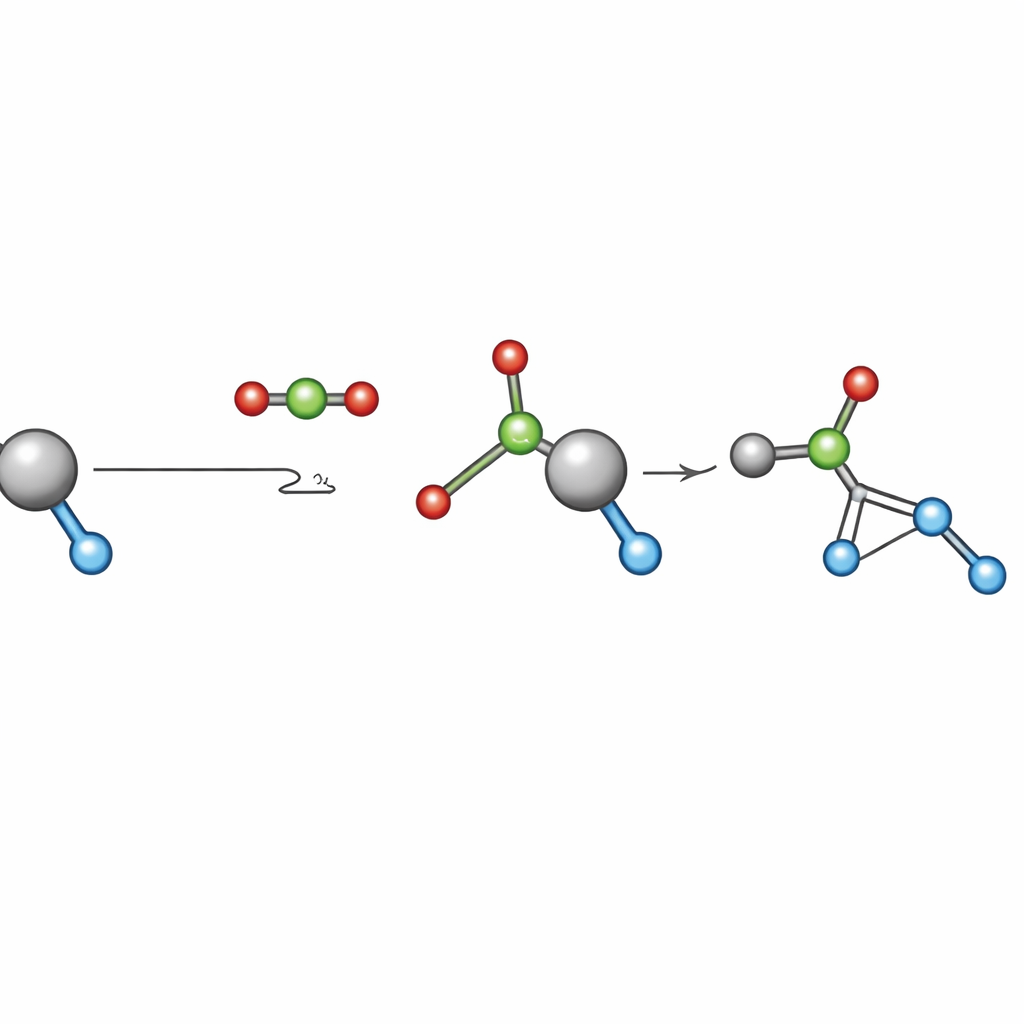
Un paso crítico pero poco entendido en muchos procesos basados en CO2 es la «inserción» del CO2: el CO2 reacciona con un enlace metal–oxígeno dentro del catalizador para formar una nueva especie metal–carbonato. A menudo se asume que este paso es rápido y no relevante para la velocidad global, por lo que rara vez se ha examinado en condiciones reales de producción. El equipo eligió una reacción muy estudiada—la copolimerización por apertura de anillo del CO2 con epóxidos como el óxido de propileno y el óxido de ciclohexeno—para estudiar este paso de inserción. Seleccionaron cinco de los catalizadores a base de cobalto más conocidos que ya funcionan a presiones relativamente bajas y temperaturas moderadas, y realizaron pruebas sistemáticas entre 2 y 30 bar de CO2 mientras monitorizaban cuidadosamente la rapidez con la que se formaba el polímero.
Descubriendo un equilibrio dependiente de la presión
En los cinco catalizadores, las velocidades de reacción mostraron dos regímenes claros. A baja presión de CO2, la velocidad aumentaba de forma constante con la presión: más CO2 desplazaba el equilibrio dentro del catalizador desde una forma metal–alcoxido hacia una forma metal–carbonato que en realidad lleva a cabo el paso clave de formación de enlace. Por encima de una «presión umbral» específica para cada catalizador, añadir más CO2 ya no ayudaba: la velocidad se estabilizaba porque casi todas las moléculas de catalizador ya estaban en la forma carbonato activa. A partir de estas mediciones, los autores extrajeron dos números prácticos para cada catalizador: una constante de equilibrio, que mide cuán fuertemente se inserta el CO2 en el catalizador, y una presión umbral, la presión mínima de CO2 necesaria para alcanzar la velocidad máxima.
De números fundamentales a reglas de diseño
Al comparar los catalizadores, surgió un patrón simple. Los catalizadores con constantes de equilibrio de inserción de CO2 mayores reaccionaban más rápido y alcanzaban su velocidad máxima a presiones más bajas. Los de peor rendimiento tenían una inserción más débil y necesitaban presiones de CO2 más altas para rendir al máximo. Estas correlaciones se mantuvieron no solo entre distintos complejos de cobalto, sino también al cambiar el monómero epóxido. El equipo demostró que midiendo la velocidad de reacción a una sola presión moderada (5 bar) podían predecir tanto la constante de equilibrio como la presión umbral para ese par catalizador–monómero. Confirmaron estas predicciones experimentalmente con catalizadores adicionales, incluido un sistema mixto de metales, y encontraron que un catalizador destacado ya podía operar de forma eficiente por debajo de 5 bar para ciertos monómeros.
Guiando futuras tecnologías de reciclaje de CO2
Para un público no especializado, el resultado clave es que los autores han convertido un paso microscópico complejo—el deslizamiento del CO2 en un enlace metal–oxígeno—en dos números simples y medibles que indican a los ingenieros cómo operar un proceso con la mínima energía. Al vincular la estructura del catalizador con la fuerza de inserción del CO2 y la presión de operación requerida, el trabajo ofrece una hoja de ruta para diseñar catalizadores de próxima generación que funcionen de forma rápida, limpia y a baja presión. Este enfoque podría acelerar el desarrollo de tecnologías escalables de conversión de CO2 en plásticos, ayudando a transformar un importante gas de efecto invernadero en productos útiles con costes energéticos y climáticos mucho menores.
Cita: Thorogood, R., Eisenhardt, K.H.S., Smith, M.L. et al. Understanding low-pressure CO2 insertion chemistry in epoxide–CO2 copolymerization catalysis. Nat. Chem. 18, 931–938 (2026). https://doi.org/10.1038/s41557-026-02098-6
Palabras clave: utilización de dióxido de carbono, catálisis a baja presión, plásticos de policarbonato, copolimerización de epóxidos, química verde