Clear Sky Science · pl
Zrozumienie chemii wstawiania CO2 przy niskim ciśnieniu w katalizie kopolimeryzacji epoksydu z CO2
Przekształcanie gazu odpadowego w codzienne materiały
Dwutlenek węgla (CO2) zwykle postrzegany jest jako gaz odpadowy ocieplający naszą planetę, ale chemicy uczą się, jak przekształcać go w użyteczne tworzywa. Problem w tym, że większość obecnych procesów wymaga sprężenia CO2 do wysokich ciśnień, co generuje koszty i zużycie energii. Artykuł bada, jak wytwarzać tworzywa oparte na CO2 efektywnie przy znacznie niższych ciśnieniach, wskazując drogę do bardziej ekologicznej produkcji materiałów stosowanych w klejach, bateriach i elastycznych tworzywach.
Dlaczego ciśnienie ma znaczenie w zielonej chemii
Aby „recyklingować” CO2 w tworzywa, chemicy używają katalizatorów — specjalnych związków, które pomagają łączyć CO2 z małymi blokami budulcowymi zwanymi epoksydami, tworząc długie łańcuchy poli(węglanów). Zakłady przemysłowe często prowadzą te reakcje przy wysokim ciśnieniu CO2, żeby uzyskać odpowiednie szybkości i jakość produktu, ale sprężanie gazu pochłania dużo energii i jest kosztowne. Autorzy wykorzystują symulacje procesowe, aby pokazać, że zwiększenie ciśnienia CO2 z umiarkowanego do wysokiego może podnieść zużycie energii dla kluczowego tworzywa, poli(propenokarbonianu), o ponad 200 procent. To sprawia, że praca przy niskim ciśnieniu jest kluczowa, jeśli tworzywa na bazie CO2 mają być jednocześnie przyjazne dla klimatu i atrakcyjne komercyjnie.
Badanie ukrytego etapu reakcji
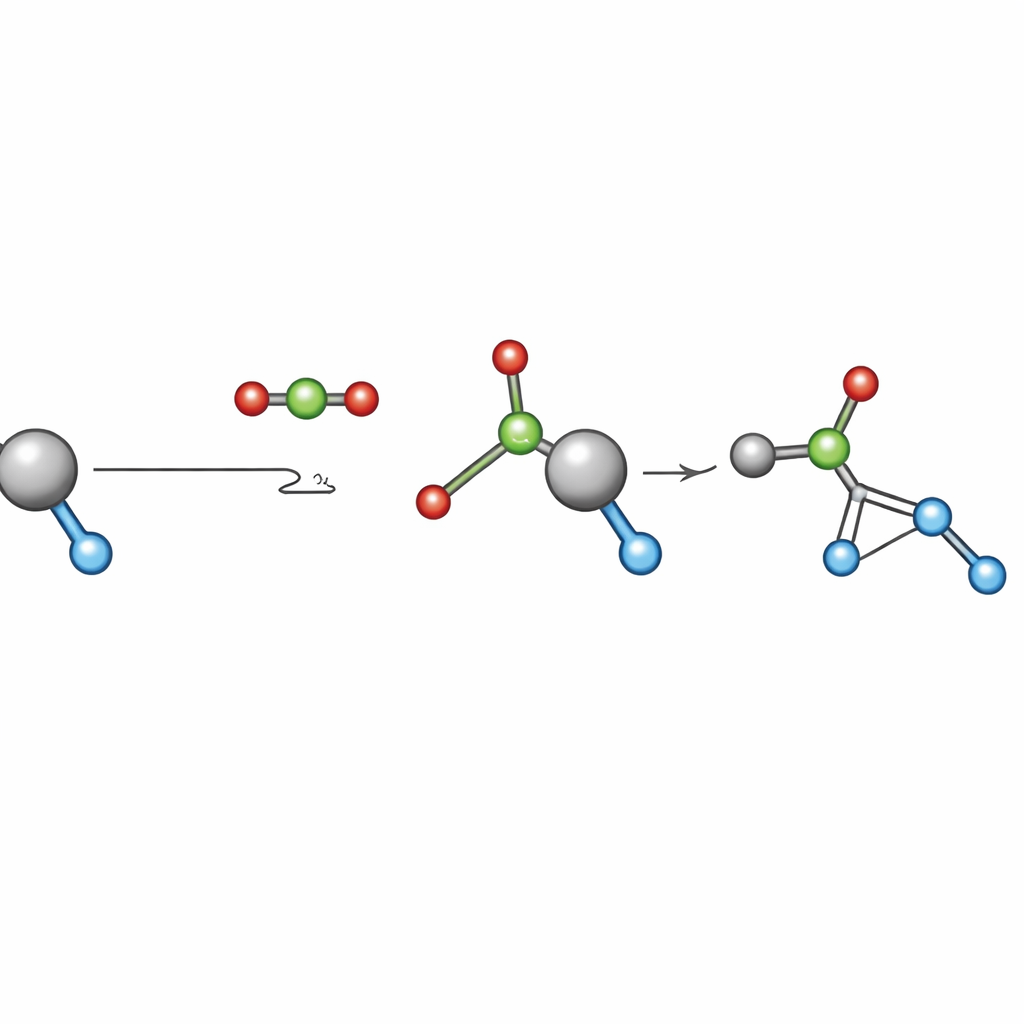
Krytyczny, lecz słabo poznany etap w wielu procesach z CO2 to tzw. „wstawianie” CO2: CO2 reaguje z wiązaniem metal–tlen w katalizatorze, tworząc nowy gatunek metal–węglanowy. Często zakłada się, że ten etap jest szybki i nie wpływa na ogólną szybkość reakcji, więc rzadko badano go w warunkach zbliżonych do produkcyjnych. Zespół wybrał szeroko badany proces — kopolimeryzację otwarcia pierścienia CO2 z epoksydami, takimi jak tlenek propylenowy i tlenek cykloheksylu — żeby przeanalizować ten krok wstawiania. Wybrali pięć najlepiej poznanych katalizatorów na bazie kobaltu, które już działają przy stosunkowo niskich ciśnieniach i umiarkowanych temperaturach, a następnie przeprowadzili systematyczne testy przy ciśnieniach CO2 od 2 do 30 bar, uważnie śledząc tempo powstawania polimeru.
Odkrycie zależnej od ciśnienia równowagi
We wszystkich pięciu katalizatorach szybkości reakcji wykazały dwa wyraźne rejony. Przy niskim ciśnieniu CO2 szybkość rosła stopniowo wraz ze wzrostem ciśnienia: większa ilość CO2 przesuwała równowagę w katalizatorze z formy metal–alkoksydowej w kierunku formy metal–węglanowej, która faktycznie przeprowadza kluczowy etap tworzenia wiązań. Powyżej określonego „progu” ciśnienia dla każdego katalizatora dodawanie kolejnego CO2 przestało pomagać — szybkość się ustabilizowała, ponieważ niemal wszystkie cząsteczki katalizatora były już w aktywnej formie węglanowej. Z tych pomiarów autorzy wydestylowali dwie praktyczne wielkości dla każdego katalizatora: stałą równowagi, mierzącą, jak silnie CO2 wstawia się do katalizatora, oraz ciśnienie progowe, czyli minimalne ciśnienie CO2 potrzebne do osiągnięcia maksymalnej szybkości.
Od liczb podstawowych do zasad projektowania
Gdy badacze porównali katalizatory, wyłonił się prosty wzorzec. Katalizatory o większych stałych równowagi wstawiania CO2 działały szybciej i osiągały maksymalne prędkości przy niższych ciśnieniach. Słabiej działające miały słabsze wstawianie i potrzebowały wyższego ciśnienia CO2, aby działać optymalnie. Korelacje te zachodziły nie tylko między różnymi kompleksami kobaltu, lecz także przy zmianie epoksydowego monomeru. Zespół wykazał, że mierząc szybkość reakcji przy jednym umiarkowanym ciśnieniu (5 bar), można przewidzieć zarówno stałą równowagi, jak i ciśnienie progowe dla danej pary katalizator–monomer. Potwierdzili te przewidywania doświadczalnie dodatkowymi katalizatorami, w tym układem mieszanym metalowym, i stwierdzili, że jeden wyróżniający się katalizator potrafił już pracować efektywnie poniżej 5 bar dla niektórych monomerów.
Wskazówki dla przyszłych technologii recyklingu CO2
Dla czytelnika niebędącego specjalistą kluczowy wniosek jest taki, że autorzy sprowadzili skomplikowany mikroskopowy etap — wślizgiwanie się CO2 do wiązania metal–tlen — do dwóch prostych, mierzalnych liczb, które informują inżynierów, jak prowadzić proces przy minimalnym zużyciu energii. Łącząc strukturę katalizatora z siłą wstawiania CO2 i wymaganym ciśnieniem roboczym, praca oferuje mapę drogową do projektowania następnej generacji katalizatorów, które działają szybko, czysto i przy niskim ciśnieniu. Takie podejście może przyspieszyć rozwój skalowalnych technologii przetwarzania CO2 na tworzywa, pomagając przekształcić znaczący gaz cieplarniany w użyteczne produkty przy znacznie mniejszych kosztach energetycznych i klimatycznych.
Cytowanie: Thorogood, R., Eisenhardt, K.H.S., Smith, M.L. et al. Understanding low-pressure CO2 insertion chemistry in epoxide–CO2 copolymerization catalysis. Nat. Chem. 18, 931–938 (2026). https://doi.org/10.1038/s41557-026-02098-6
Słowa kluczowe: wykorzystanie dwutlenku węgla, kataliza przy niskim ciśnieniu, poliwęglanowe tworzywa sztuczne, kopolimeryzacja epoksydów, zielona chemia