Clear Sky Science · pt
Modelagem da deformação epitelial e reorganização celular em resposta a forças externas durante a epibolia de Zebrafish
Como um embrião precoce forma uma pele protetora
Antes que um embrião de zebrafish se pareça com um peixe, ele precisa realizar um feito notável: uma lâmina fina de células se espalha sobre um enorme vitelo e o sela. Esse movimento, chamado epibolia, é uma das primeiras grandes mudanças de forma em muitos embriões de peixes. Entender como essa camada frágil consegue esticar tanto, permanecer íntegra e mover-se de modo coordenado ajuda os cientistas a compreender como os embriões constroem organismos — e por que tecidos às vezes falham, rompem ou cicatrizam mal em doença e lesão.

Uma lâmina celular que precisa esticar sem romper
No início da epibolia, o zebrafish jovem é em grande parte uma única célula de vitelo enorme coberta por milhares de células bem menores. A mais externa dessas é uma lâmina muito fina, “semelhante a uma pele”, chamada camada envolvente (EVL). Durante a epibolia, a EVL precisa se espalhar de um pequeno capuz no topo do vitelo até envolver toda sua circunferência, mais que dobrando sua área. Ela deve fazer isso mantendo-se selada para o exterior e firmemente ligada às células vizinhas, apesar de ser puxada por forças geradas nas profundezas do vitelo. Experimentos mostraram que a borda da EVL começa irregular e depois se alisa em um anel suave conforme avança, mas as regras mecânicas que possibilitam isso não estavam claras.
Construindo um embrião virtual
Para investigar essas regras, os autores desenvolveram um modelo computacional da EVL usando uma estratégia “baseada em agentes”. Em vez de simular cada detalhe das formas celulares, representaram cada célula da EVL por um ponto — seu centro de massa — sobre a superfície de uma esfera que representa o vitelo. Esses pontos estão ligados por molas virtuais que imitam tanto a resistência das células à compressão quanto a adesão nas junções célula–célula. O modelo puxa apenas as células na borda exposta da lâmina, refletindo como embriões reais transmitem força do vitelo através das junções marginais. À medida que o tempo simulado avança, as molas se esticam ou comprimem e os pontos se movem, permitindo que a camada deslize sobre o vitelo esférico.
Perguntando como células trocam vizinhos sem risco
Quando os vínculos célula–célula no modelo eram fixos, a EVL comportava-se como um elástico: esticava, tornava-se irregular e recuava fortemente quando o puxão cessava. A EVL real faz algo mais sutil — ela se remodela internamente e não volta a seu estado anterior. Para capturar isso, os pesquisadores permitiram que vínculos entre células vizinhas fossem aleatoriamente quebrados e reconstituídos com células próximas, representando uma versão grosseira de como epitélios trocam vizinhos. Eles adicionaram uma regra simples de “energia” que favorece arranjos locais nos quais cada célula apresenta um empacotamento aproximadamente hexagonal. Isso evitou que a lâmina desenvolvesse falhas enquanto ainda permitia extensa reorganização. Com esse remodelamento, a EVL virtual pôde se espalhar ao redor do vitelo, afinar e sofrer cisalhamento, e então permanecer estável quando a força de tração foi removida. O comportamento do tecido não foi puramente elástico nem puramente plástico, mas “viscoelastoplástico”: deformou-se, relaxou e em parte travou em sua nova forma.
Manter a borda em movimento sincronizada
Um enigma em embriões vivos é que todas as partes da borda da EVL alcançam o polo vegetal quase ao mesmo tempo. Na primeira versão do modelo, entretanto, pequenas diferenças aleatórias eram ampliadas: uma região da borda avançava mais rápido, formando uma protuberância, enquanto outras ficavam para trás. Simplesmente tensionar o anel de células marginais não resolveu o problema. A equipe então acrescentou uma forma simples de feedback: células da borda que estavam mais distantes do polo vegetal eram puxadas ligeiramente com mais força do que as já mais próximas. Esse feedback negativo sincronizou o movimento da borda sem alterar a taxa global de expansão. Curiosamente, ambas as versões do modelo — com ou sem esse feedback — alisaram espontaneamente a borda inicialmente irregular à medida que as células trocavam continuamente de vizinhos, sugerindo que rearranjos locais rápidos e o aumento da tensão suavizam naturalmente a fronteira.
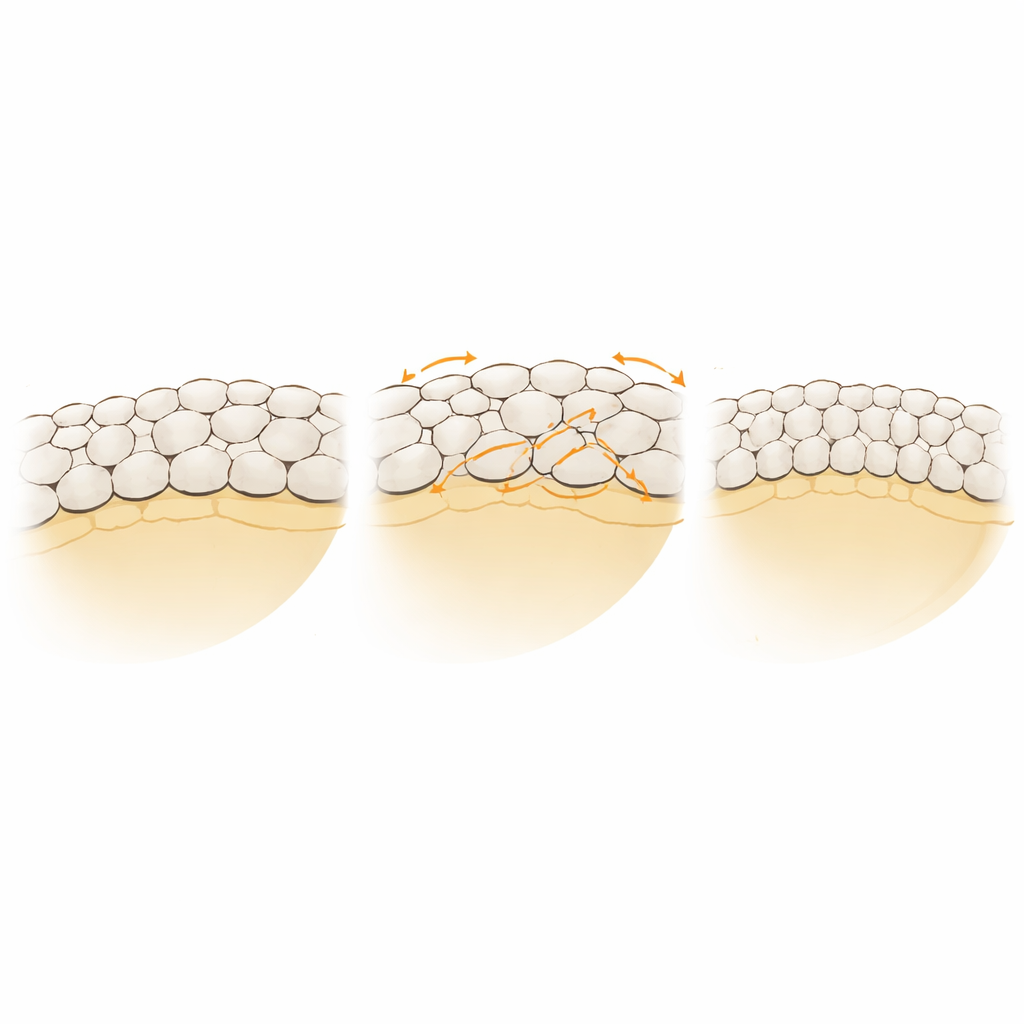
O que isso revela sobre tecidos vivos
Ao destilar um movimento embrionário complexo em pontos e molas, o estudo identifica dois ingredientes-chave para uma epibolia realista: um mecanismo para as células reorganizarem suas conexões sem romper a lâmina, e um mecanismo de feedback que balanceie as forças de tração ao redor da margem. Juntos, esses elementos permitem que uma camada epitelial delicada se espalhe muito, mude de forma de modo dramático e mantenha sua integridade. O trabalho sugere que embriões reais podem usar estratégias semelhantes — remodelamento local de junções que pode “destravar” o tecido quando necessário, e regulação de força que mantém uma frente de avanço sincronizada. Tais princípios provavelmente importam não só no desenvolvimento de peixes, mas em qualquer situação em que tecidos precisam expandir, fechar lacunas ou cicatrizar sem se desfazer.
Citação: Minsuk, S.B., Sego, T.J., Umulis, D.M. et al. Modeling epithelial deformation and cell rearrangement in response to external forces during Zebrafish epiboly. npj Syst Biol Appl 12, 63 (2026). https://doi.org/10.1038/s41540-026-00708-0
Palavras-chave: desenvolvimento de zebrafish, epibolia, mecânica epitelial, modelagem computacional, reorganização celular