Clear Sky Science · fr
Modélisation de la déformation épithéliale et du réarrangement cellulaire en réponse aux forces externes pendant l’épibolie du zebrafish
Comment un embryon précoce forme une peau protectrice
Avant qu’un embryon de zebrafish ne ressemble à un poisson, il doit accomplir un exploit remarquable : une mince feuille de cellules s’étend et scelle un énorme vitellus. Ce mouvement, appelé épibolie, est l’un des premiers changements morphologiques majeurs chez de nombreux embryons de poissons. Comprendre comment cette couche fragile peut s’étirer autant, demeurer intacte et se déplacer de façon coordonnée aide les scientifiques à saisir comment les embryons construisent des corps — et pourquoi les tissus échouent parfois, se déchirent ou cicatrisent mal lors de maladies ou de blessures.

Une feuille cellulaire qui doit s’étirer sans se rompre
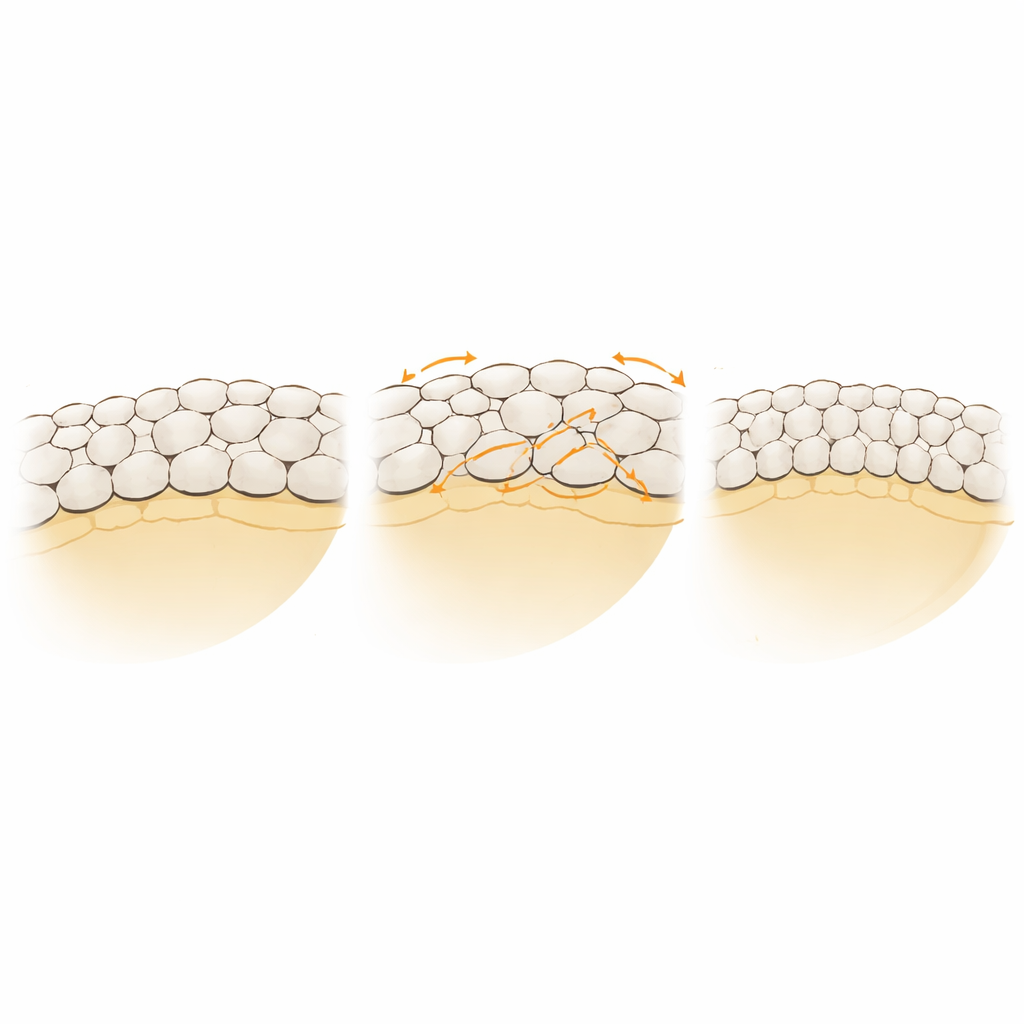
Au début de l’épibolie, l’embryon de zebrafish est majoritairement constitué d’une grande cellule vitelline surmontée de milliers de cellules beaucoup plus petites. La couche la plus externe est une mince feuille « cutanée » appelée enveloping layer (EVL). Pendant l’épibolie, l’EVL doit s’étendre d’un petit chapeau au sommet du vitellus pour l’entourer complètement, plus que doublant sa surface. Elle doit le faire tout en restant scellée vers l’extérieur et fermement attachée à ses voisines, malgré les forces de traction générées profondément dans le vitellus. Des expériences ont montré que le bord de l’EVL est d’abord irrégulier puis se redresse en un anneau lisse en se déplaçant, mais les règles mécaniques qui rendent cela possible restaient floues.
Construire un embryon virtuel
Pour sonder ces règles, les auteurs ont construit un modèle informatique de l’EVL utilisant une stratégie « à base d’agents ». Plutôt que de simuler chaque détail des formes cellulaires, ils ont représenté chaque cellule de l’EVL par un point — son centre de masse — sur la surface d’une sphère faisant office de vitellus. Ces points sont reliés par des ressorts virtuels qui imitent à la fois la résistance des cellules à la compression et l’adhérence des jonctions cellule–cellule. Le modèle tire uniquement sur les cellules situées au bord exposé de la feuille, reflétant la façon dont les embryons réels transmettent la force depuis le vitellus à travers les jonctions à la marge. Au fur et à mesure de l’avancement du temps simulé, les ressorts s’étirent ou se compriment et les points se déplacent, permettant à la couche de glisser sur le vitellus sphérique.
Laisser les cellules échanger leurs voisines en toute sécurité
Lorsque les liaisons cellule–cellule dans le modèle restaient fixes, l’EVL se comportait comme un élastique : elle s’étirait mais devenait irrégulière et rebondissait fortement lorsque la traction cessait. L’EVL réelle fait quelque chose de plus subtil : elle se réorganise en interne et ne revient pas brutalement en arrière. Pour capturer cela, les chercheurs ont autorisé les liaisons entre cellules voisines à se rompre aléatoirement puis à se reformer avec des cellules proches, représentant une version grossière de la façon dont les épithéliums échangent leurs voisines. Ils ont ajouté une règle simple d’« énergie » favorisant des arrangements locaux où chaque cellule présente un empilement approchant l’hexagone. Cela a empêché la formation de trous tout en permettant un réarrangement étendu. Avec ce remodelage, l’EVL virtuelle a pu s’étendre autour du vitellus, s’amincir et subir du cisaillement, puis rester stable lorsque la traction était supprimée. Le comportement du tissu n’était ni purement élastique ni purement plastique, mais « viscoélastoplastique » : il se déformait, se relâchait et se verrouillait partiellement dans sa nouvelle forme.
Garder le bord en mouvement synchronisé
Un mystère chez les embryons vivants est que toutes les parties du bord de l’EVL atteignent le bas du vitellus presque en même temps. Dans la première version du modèle, cependant, de petites différences aléatoires étaient amplifiées : une région du bord prenait de l’avance en formant une protrusion, tandis que d’autres restaient en retrait. Simplement resserrer l’anneau des cellules bordières n’a pas résolu le problème. L’équipe a alors ajouté une forme simple de rétroaction : les cellules de bord situées plus loin du pôle végétatif étaient tirées légèrement plus fort que celles déjà plus proches. Cette rétroaction négative a synchronisé le mouvement du bord sans changer le taux global d’expansion. Fait intéressant, les deux versions du modèle — avec ou sans cette rétroaction — ont redressé spontanément le bord initialement irrégulier au fur et à mesure que les cellules échangeaient continuellement leurs voisines, ce qui suggère que des réarrangements locaux rapides et l’augmentation de la tension lissent naturellement la frontière.
Ce que cela révèle sur les tissus vivants
En distillant un mouvement embryonnaire complexe en points et ressorts, l’étude identifie deux ingrédients clés pour une épibolie réaliste : un mécanisme permettant aux cellules de réorganiser leurs connexions sans rompre la feuille, et un mécanisme de rétroaction qui équilibre les forces de traction autour de la marge. Ensemble, ils permettent à une couche épithéliale délicate de s’étendre largement, de changer de forme de manière spectaculaire et de conserver son intégrité. Le travail suggère que les embryons réels peuvent utiliser des stratégies similaires : un remodelage local des jonctions qui peut « désencombrer » le tissu là où c’est nécessaire, et une régulation des forces qui maintient l’avance du front. De tels principes sont sans doute pertinents non seulement dans le développement des poissons, mais partout où les tissus doivent s’étendre, refermer des lacunes ou cicatriser sans se désintégrer.
Citation: Minsuk, S.B., Sego, T.J., Umulis, D.M. et al. Modeling epithelial deformation and cell rearrangement in response to external forces during Zebrafish epiboly. npj Syst Biol Appl 12, 63 (2026). https://doi.org/10.1038/s41540-026-00708-0
Mots-clés: développement du zebrafish, épibolie, mécanique épithéliale, modélisation computationnelle, réarrangement cellulaire