Clear Sky Science · es
Modelado de la deformación epitelial y el reordenamiento celular en respuesta a fuerzas externas durante la epibolia del pez cebra
Cómo un embrión temprano crea una piel protectora
Antes de que un embrión de pez cebra se parezca a un pez, debe realizar una hazaña notable: una delgada lámina de células se extiende y sella un enorme vitelo. Este movimiento, llamado epibolia, es uno de los primeros grandes cambios de forma en muchos embriones de peces. Entender cómo esta capa frágil puede estirarse tanto, mantenerse intacta y moverse de forma coordinada ayuda a los científicos a comprender cómo los embriones construyen cuerpos —y por qué los tejidos a veces fallan, se rompen o cicatrizan mal en enfermedad y lesión.

Una lámina celular que debe estirarse sin desgarrarse
Al inicio de la epibolia, el pez cebra temprano es en su mayor parte una enorme célula vitelina cubierta por miles de células mucho más pequeñas. La capa más externa es una lámina muy fina, parecida a una “piel”, llamada capa envolvente (EVL). Durante la epibolia, la EVL tiene que extenderse desde una pequeña tapa en la parte superior del vitelo hasta envolverlo por completo, más que duplicando su área. Debe hacerlo mientras permanece sellada hacia el exterior y firmemente unida a sus vecinas, a pesar de ser tirada por fuerzas generadas en lo profundo del vitelo. Los experimentos han mostrado que el borde de la EVL comienza irregular y luego se alisa en un anillo suave a medida que avanza, pero las reglas mecánicas que hacen esto posible han sido poco claras.
Construyendo un embrión virtual
Para investigar estas reglas, los autores construyeron un modelo informático de la EVL usando una estrategia “basada en agentes”. En lugar de simular cada detalle de las formas celulares, representaron cada célula de la EVL como un punto —su centro de masa— sobre la superficie de una esfera que sustituye al vitelo. Estos puntos están conectados por resortes virtuales que imitan tanto la resistencia de las células a ser comprimidas como la adhesión de las uniones célula–célula. El modelo tira solo de las células en el borde expuesto de la lámina, reflejando cómo los embriones reales transmiten fuerza desde el vitelo a través de las uniones en el margen. A medida que avanza el tiempo simulado, los resortes se estiran o comprimen y los puntos se mueven, permitiendo que la capa se deslice sobre el vitelo esférico.
Permitir que las células intercambien vecinas con seguridad
Cuando los enlaces célula–célula en el modelo eran fijos, la EVL se comportaba como una banda elástica: se estiraba pero se volvía dentada y rebotaba fuertemente cuando se detenía la tracción. La EVL real hace algo más sutil: se remodela internamente y no vuelve a su forma previa. Para capturar esto, los investigadores permitieron que los enlaces entre células vecinas se rompieran aleatoriamente y se volvieran a formar con células cercanas, representando una versión tosca de cómo los epitelios intercambian vecindarios. Añadieron una regla de “energía” simple que favorece disposiciones locales en las que cada célula tiene un empaque aproximadamente hexagonal. Esto evitó que la lámina desarrollara huecos mientras permitía un reordenamiento extenso. Con este remodelado, la EVL virtual pudo rodear el vitelo, adelgazarse y cizallarse, y luego permanecer estable cuando se eliminó la tracción. El comportamiento del tejido no fue ni puramente elástico ni puramente plástico, sino “viscoelastoplástico”: se deformó, relajó y parcialmente se fijó en su nueva forma.
Mantener el borde en movimiento sincronizado
Un enigma en embriones vivos es que todas las partes del borde de la EVL alcanzan el fondo del vitelo casi al mismo tiempo. En la primera versión del modelo, sin embargo, pequeñas diferencias aleatorias se amplificaban: una región del borde avanzaba formando una protrusión, mientras otras quedaban rezagadas. Simplemente tensar el anillo de células del borde no solucionó esto. El equipo añadió entonces una forma sencilla de retroalimentación: las células del borde que estaban más lejos del polo vegetal eran tiradas ligeramente con más fuerza que las que ya estaban más cerca. Esta retroalimentación negativa sincronizó el movimiento del borde sin cambiar la tasa global de expansión. Curiosamente, ambas versiones del modelo —con o sin esta retroalimentación— enderezaron espontáneamente el borde inicialmente irregular a medida que las células intercambiaban vecinas de forma continua, lo que sugiere que los reordenamientos locales rápidos y el aumento de tensión alisan naturalmente la frontera.
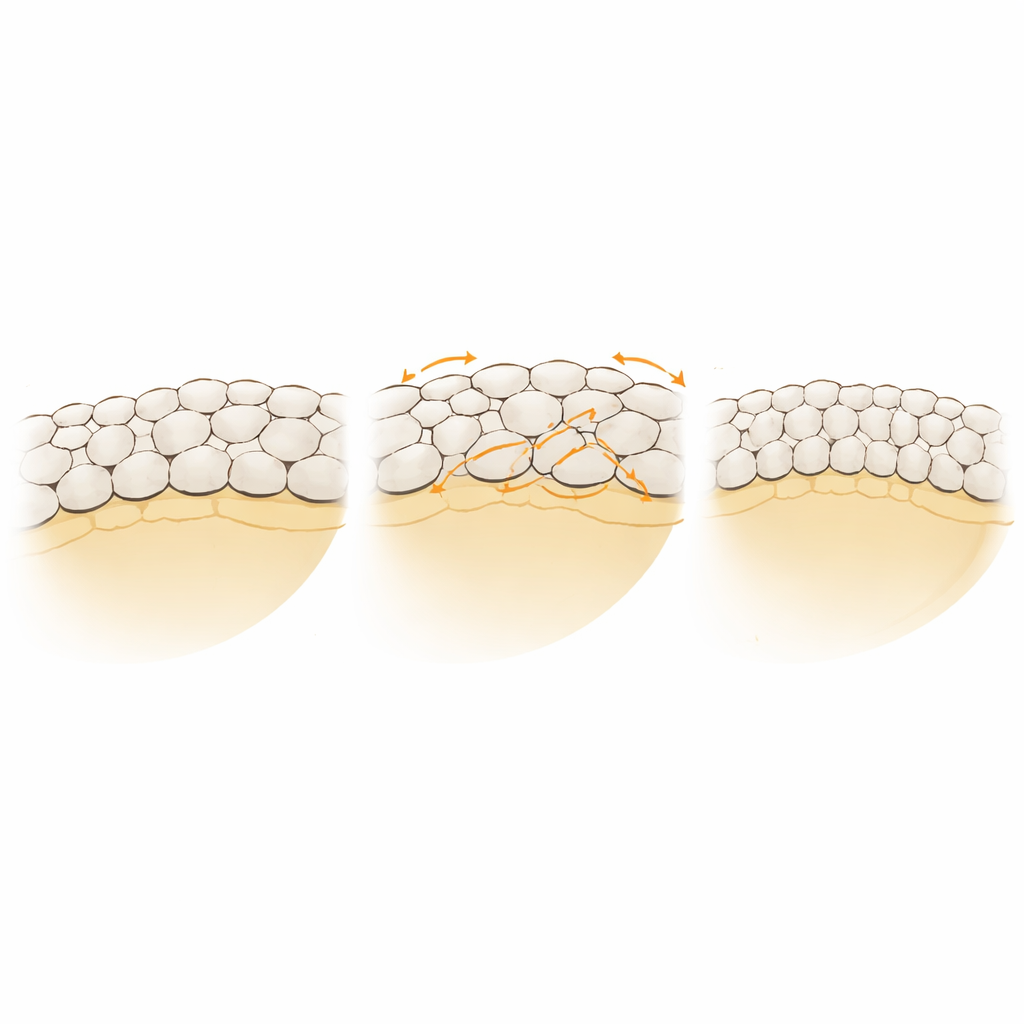
Qué revela esto sobre los tejidos vivos
Al destilar un movimiento embrionario complejo en puntos y resortes, el estudio identifica dos ingredientes clave para una epibolia realista: un modo por el que las células puedan reorganizar sus conexiones sin romper la lámina, y un mecanismo de retroalimentación que equilibre las fuerzas de tracción alrededor del margen. Juntos, permiten que una delicada capa epitelial se extienda ampliamente, cambie de forma de manera dramática y mantenga su integridad. El trabajo sugiere que los embriones reales pueden usar estrategias similares —el remodelado local de uniones que puede “desatascar” el tejido cuando es necesario, y la regulación de fuerzas que mantiene sincronizado un frente en avance. Tales principios probablemente importan no solo en el desarrollo de peces, sino dondequiera que los tejidos deban expandirse, cerrar huecos o sanar sin desintegrarse.
Cita: Minsuk, S.B., Sego, T.J., Umulis, D.M. et al. Modeling epithelial deformation and cell rearrangement in response to external forces during Zebrafish epiboly. npj Syst Biol Appl 12, 63 (2026). https://doi.org/10.1038/s41540-026-00708-0
Palabras clave: desarrollo del pez cebra, epibolia, mecánica epitelial, modelado computacional, reordenamiento celular