Clear Sky Science · de
Modellierung der Epithelverformung und Zellumlagerung als Reaktion auf äußere Kräfte während der Epibolie von Zebrafischen
Wie ein frühes Embryo eine schützende Haut bildet
Bevor ein Zebrafischembryo auch nur entfernt wie ein Fisch aussieht, muss er eine bemerkenswerte Leistung vollbringen: Ein dünnes Zellblatt breitet sich aus und verschließt einen riesigen Dotter. Diese Bewegung, Epibolie genannt, ist eine der ersten großen Formänderungen bei vielen Fischembryonen. Zu verstehen, wie diese fragile Schicht sich so weit dehnen, intakt bleiben und sich koordiniert bewegen kann, hilft Wissenschaftlern zu begreifen, wie Embryonen Körper aufbauen — und warum Gewebe bei Krankheit oder Verletzung manchmal versagen, einreißen oder schlecht heilen.

Ein Zellblatt, das sich dehnen muss, ohne zu reißen
Zu Beginn der Epibolie besteht der frühe Zebrafisch größtenteils aus einer riesigen Dotterzelle, die von Tausenden deutlich kleineren Zellen bedeckt ist. Die äußerste dieser Schichten ist ein sehr dünnes, „hautartiges“ Blatt, die sogenannte enveloping layer (EVL). Während der Epibolie muss sich die EVL von einer kleinen Kappe an der Spitze des Dotters so weit ausbreiten, dass sie ihn vollständig umhüllt — ihre Fläche mehr als verdoppelnd. Dabei muss sie nach außen hin verschlossen und fest an ihren Nachbarn befestigt bleiben, obwohl sie von Kräften gezogen wird, die tief im Dotter erzeugt werden. Experimente haben gezeigt, dass der Rand der EVL anfangs gezackt ist und sich dann beim Vorrücken zu einem glatten Ring glättet, doch die mechanischen Regeln, die dies ermöglichen, waren unklar.
Aufbau eines virtuellen Embryos
Um diese Regeln zu untersuchen, bauten die Autorinnen und Autoren ein Computermodell der EVL unter Verwendung einer „agentenbasierten“ Strategie. Statt jede Einzelheit der Zellformen zu simulieren, stellten sie jede EVL-Zelle als einen Punkt — ihren Schwerpunkt — auf der Oberfläche einer Kugel dar, die den Dotter repräsentiert. Diese Punkte sind durch virtuelle Federn verbunden, die sowohl den Widerstand der Zellen gegen Zusammendrücken als auch die Klebrigkeit der Zell–Zell-Verbindungen nachbilden. Das Modell zieht nur an den Zellen am freiliegenden Rand des Blatts, was widerspiegelt, wie reale Embryonen Kraft vom Dotter über Verbindungen am Rand übertragen. Mit fortschreitender Simulationszeit dehnen oder komprimieren sich die Federn und die Punkte bewegen sich, sodass die Schicht über den kugelförmigen Dotter gleiten kann.
Zellen sicher Nachbarn wechseln lassen
Wenn Zell–Zell-Verbindungen im Modell fixiert waren, verhielt sich die EVL wie ein Gummiband: Sie dehnte sich, wurde aber gezackt und schnappte heftig zurück, sobald das Ziehen aufhörte. Die reale EVL verhält sich subtiler — sie remodeliert sich intern und schnellt nicht zurück. Um dies abzubilden, erlaubten die Forschenden, dass Verbindungen zwischen benachbarten Zellen zufällig gelöst und mit nahen Zellen neu geknüpft werden, was eine grobe Darstellung dessen ist, wie Epithelien Nachbarn austauschen. Sie fügten eine einfache „Energie“-Regel hinzu, die lokale Anordnungen begünstigt, in denen jede Zelle annähernd sechseckig gepackt ist. Das verhinderte, dass die Schicht Löcher entwickelte, und erlaubte gleichzeitig umfangreiche Umlagerungen. Mit diesem Remodeling konnte sich die virtuelle EVL um den Dotter ausbreiten, ausdünnen und scheren und danach stabil bleiben, wenn die Zugkraft wegfiel. Das Verhalten des Gewebes war weder rein elastisch noch rein plastisch, sondern „viskoelastoplastisch“: es verformte sich, entspannte und sperrte sich teilweise in seine neue Form ein.
Den sich bewegenden Rand im Gleichschritt halten
Ein Rätsel in lebenden Embryonen ist, dass alle Teile des EVL-Rands nahezu gleichzeitig den Boden des Dotters erreichen. In der ersten Version des Modells wurden winzige zufällige Unterschiede jedoch verstärkt: Ein Abschnitt des Rands eilte voraus und bildete eine Ausstülpung, während andere zurückblieben. Einfaches Straffen des Rings aus Randzellen behob das Problem nicht. Das Team fügte daraufhin eine einfache Form von Feedback hinzu: Randzellen, die weiter vom vegetativen Pol entfernt waren, wurden etwas stärker gezogen als solche, die bereits näher waren. Dieses negative Feedback synchronisierte die Bewegung des Randes, ohne die Gesamtgeschwindigkeit der Ausdehnung zu verändern. Interessanterweise glätteten beide Modellversionen — mit oder ohne dieses Feedback — spontan den anfangs gezackten Rand, während Zellen ständig die Nachbarn tauschten, was darauf hindeutet, dass schnelle lokale Umlagerungen und steigende Spannung die Grenze natürlich begradigen.
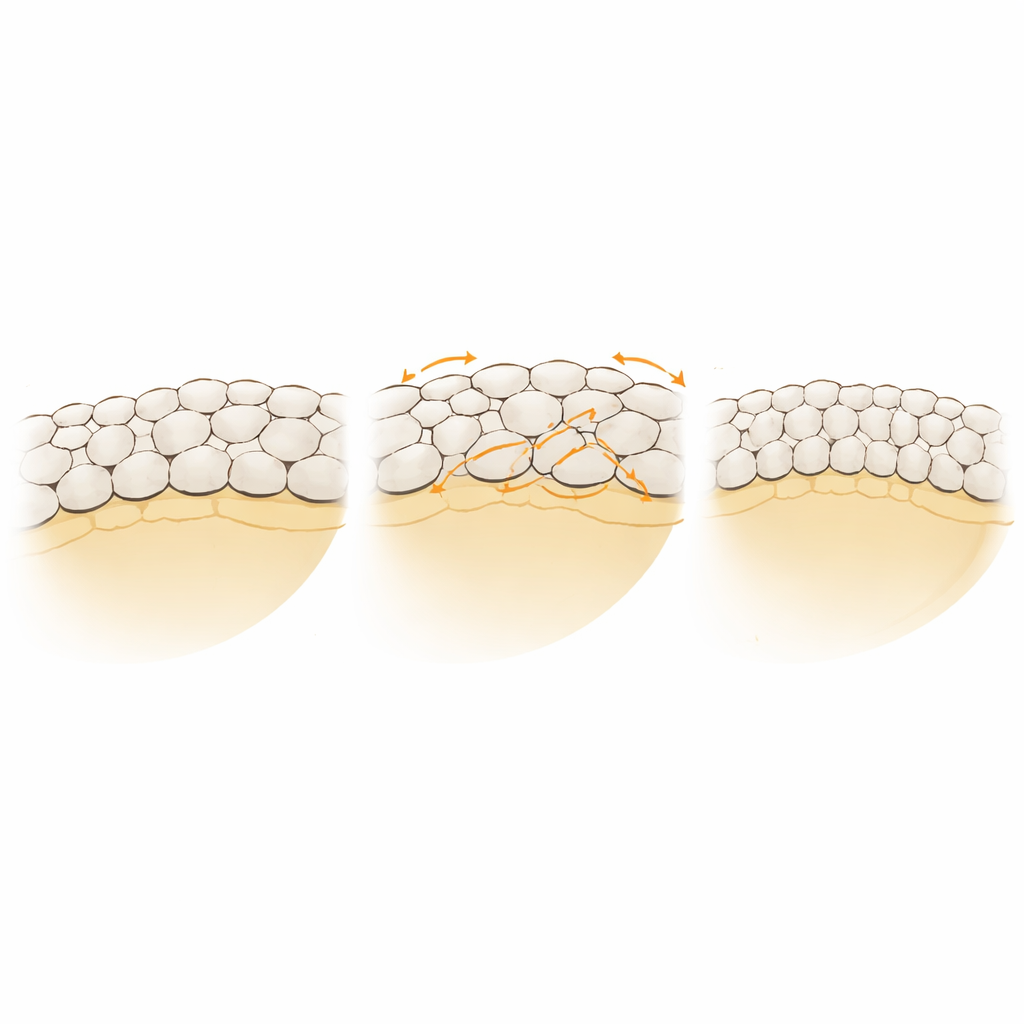
Was dies über lebende Gewebe verrät
Indem sie eine komplexe embryonale Bewegung auf Punkte und Federn reduzierten, identifiziert die Studie zwei Schlüsselelemente für realistische Epibolie: eine Möglichkeit, dass Zellen ihre Verbindungen reorganisieren, ohne das Blatt zu zerreißen, und einen Feedbackmechanismus, der die Zugkräfte am Rand ausbalanciert. Zusammen erlauben diese, dass eine zarte epithelialle Schicht weitreichend ausbreitet, ihre Form dramatisch ändert und dabei ihre Integrität bewahrt. Die Arbeit legt nahe, dass reale Embryonen ähnliche Strategien nutzen könnten — lokales Junction-Remodeling, das Gewebe dort „entjammt“, wo es nötig ist, und Kraftregulierung, die eine voranschreitende Front im Gleichschritt hält. Solche Prinzipien dürften nicht nur in der Fischentwicklung wichtig sein, sondern überall dort, wo Gewebe sich ausdehnen, Lücken schließen oder heilen müssen, ohne auseinanderzufallen.
Zitation: Minsuk, S.B., Sego, T.J., Umulis, D.M. et al. Modeling epithelial deformation and cell rearrangement in response to external forces during Zebrafish epiboly. npj Syst Biol Appl 12, 63 (2026). https://doi.org/10.1038/s41540-026-00708-0
Schlüsselwörter: Zebrafischentwicklung, Epibolie, Epithelmechanik, Computationales Modellieren, Zellumlagerung