Clear Sky Science · pt
Variantes TP53 de baixa penetrância são principalmente hipomórficas: um problema subestimado com alta relevância clínica
Por que alguns riscos hereditários de câncer passam despercebidos
O gene TP53, frequentemente chamado de guardião do nosso DNA, é famoso por seu papel crucial em impedir que células se tornem cancerosas. Médicos já sabem há muito tempo que certas mutações raras e "tudo ou nada" em TP53 podem praticamente garantir câncer cedo na vida. Este artigo explora um lado mais silencioso e pouco compreendido do TP53: variantes hereditárias que enfraquecem, mas não destroem completamente, o poder protetor do gene. Essas variantes sutis são muito mais comuns do que se pensava e podem transformar a forma como avaliamos o risco de câncer e planejamos o rastreamento em muitas famílias.
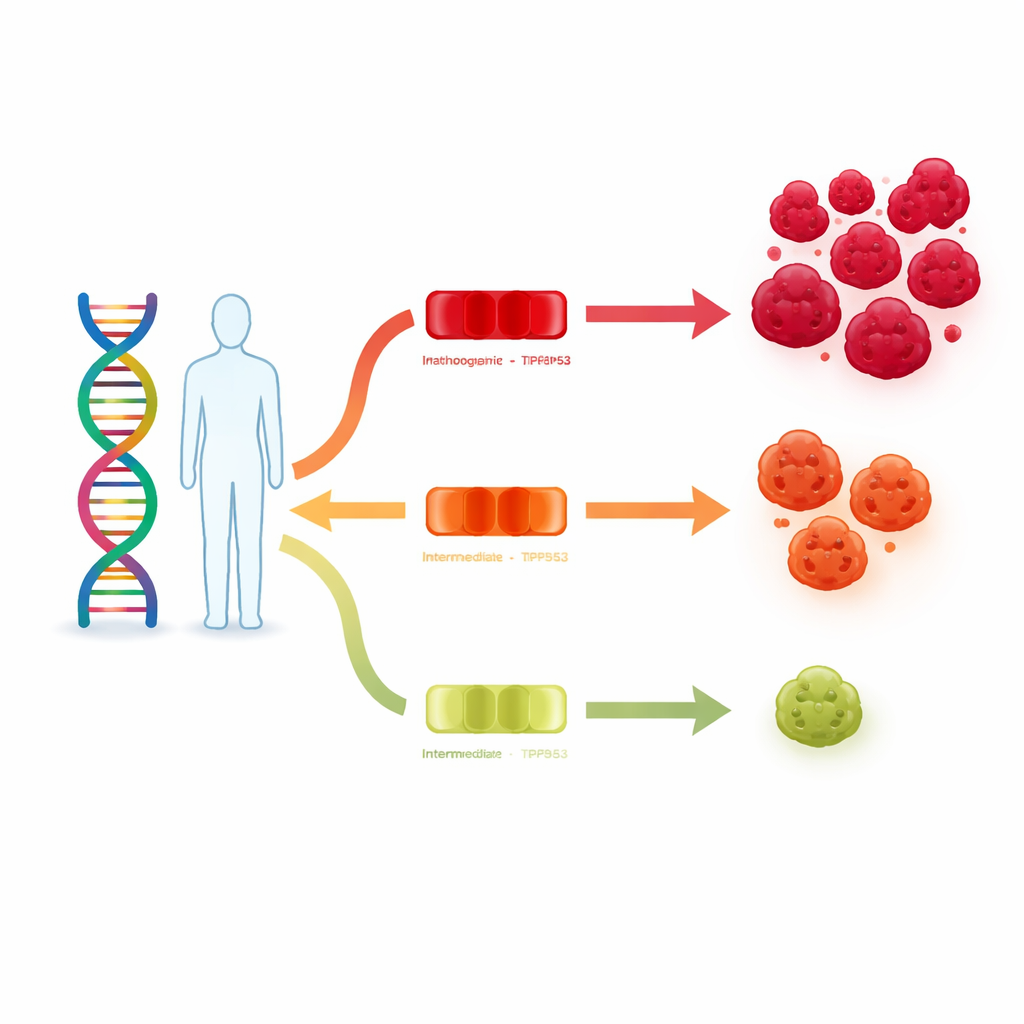
Um gene guardião chave com muitos graus de força
O TP53 indica às células quando pausar, reparar danos ou se autodestruir se o DNA estiver muito lesionado. Mutações clássicas de alto risco em TP53, observadas na síndrome de Li-Fraumeni, desativam esse guardião quase por completo, deixando as pessoas com alta probabilidade de desenvolver múltiplos cânceres em idades jovens. Mas muitas alterações em TP53 são variantes de missense, que trocam apenas uma letra do DNA e podem enfraquecer a proteína apenas parcialmente. Até agora, a maior parte da atenção foi direcionada às formas mais perigosas, enquanto as variantes mais brandas, de baixa penetrância — que aumentam o risco de câncer apenas modestamente e nem sempre em todos os portadores — permanecem em uma zona cinzenta.
Encontrando os causadores discretos em grandes bancos de mutações
Os autores analisaram a edição de 2025 do banco de dados UMD_TP53, a maior coleção mundial de mutações de TP53 vindas de tumores e casos hereditários, e a cruzaram com outros conjuntos de dados populacionais e de câncer. Eles investigaram com que frequência cada variante TP53 aparecia em tumores (somática) versus sendo herdada (germline), calculando uma "razão germline-versus-somatic" (GVSr). A maioria das mutações dirigidas ao câncer em TP53 apresenta razões baixas, surgindo frequentemente como mudanças adquiridas em tumores. Em contraste, a equipe descobriu um conjunto distinto de variantes com GVSr incomumente alto: apareciam desproporcionalmente como alterações herdadas, mas eram representadas apenas modestamente como motoras independentes em tumores. Muitas dessas já haviam sido relatadas em famílias com padrões de câncer atípicos ou mais brandos, sugerindo que podem constituir uma classe especial de baixa penetrância.
Guardas de meio período: o que os testes funcionais revelam
Para entender o que essas variantes de alto GVSr realmente fazem nas células, os pesquisadores combinaram dados de vários experimentos em grande escala que testaram sistematicamente milhares de variantes de TP53 em leveduras e células de mamíferos. Em todos esses ensaios independentes, emergiu o mesmo padrão: as variantes de alto GVSr raramente se comportavam como TP53 completamente inativo, mas também não eram totalmente normais. Em vez disso, mostraram atividade intermediária — suficientemente fortes para ativar muitos genes protetores, porém claramente mais fracas que a versão saudável. Amostras tumorais e linhagens celulares que carregavam essas variantes também exibiram apenas um amortecimento parcial dos programas gênicos controlados por TP53, diferente do desligamento dramático observado com mutações clássicas em hotspots ou nonsense. Em conjunto, isso coloca a maioria dessas variantes na categoria "hipomórfica": enfraquecidas, mas não eliminadas.
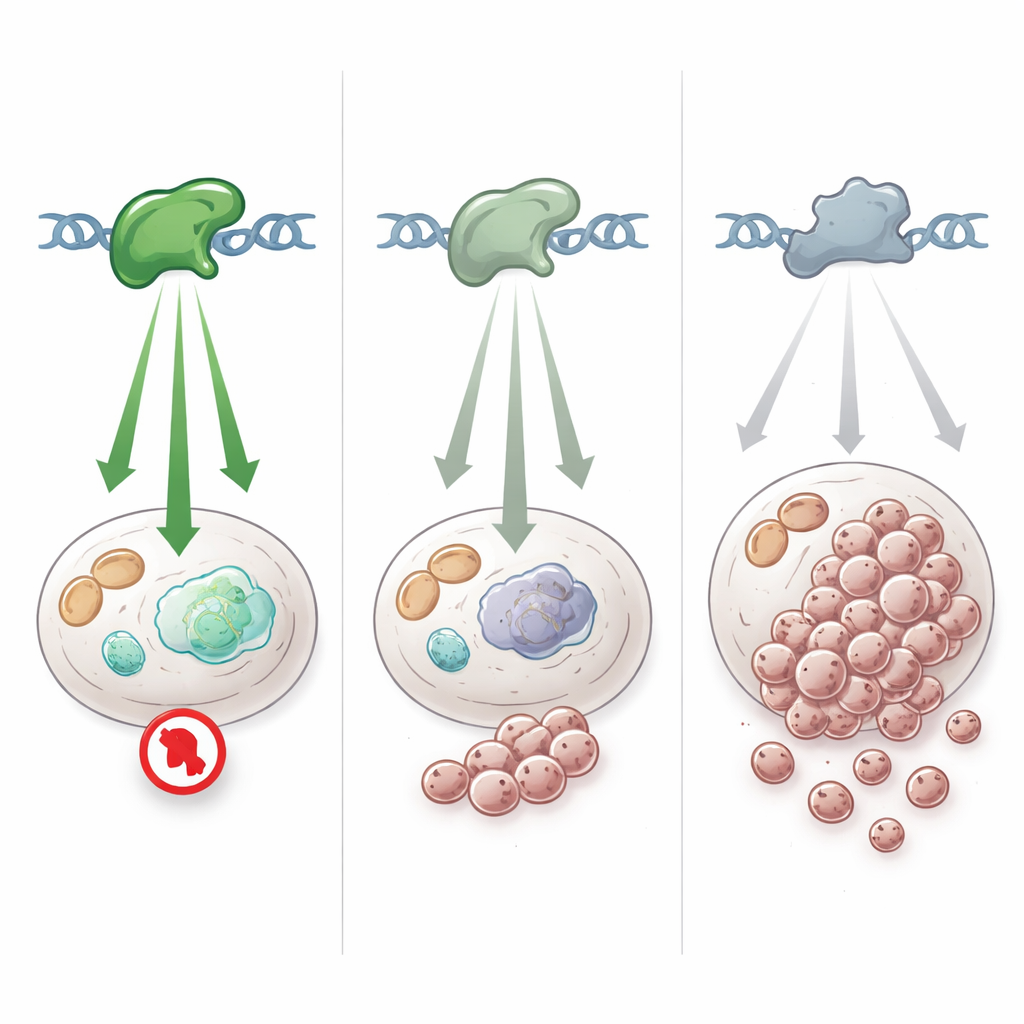
Como variantes sutis moldam o risco de câncer na vida real
Dados genéticos e clínicos sugerem que pessoas que herdam essas variantes hipomórficas de TP53 enfrentam um espectro de risco de câncer mais baixo e mais variável do que na síndrome clássica de Li-Fraumeni. Algumas variantes, como alterações nas posições 181 ou 337 da proteína, concentram-se em populações específicas e estão associadas a taxas aumentadas de certos cânceres, como tumores de mama ou cânceres adrenocorticais pediátricos, mas com penetrância incompleta — muitos portadores nunca desenvolvem câncer ou o desenvolvem em idade mais avançada. Tumores que surgem em portadores frequentemente adquirem uma segunda mutação TP53 mais disruptiva, implicando que a variante mais fraca sozinha não é suficientemente potente para iniciar o câncer, mas ainda pode contribuir para o risco quando combinada com outros eventos ou genes modificadores.
O que isso significa para pacientes e suas famílias
Este trabalho mostra que muitas variantes hereditárias de TP53 não são simplesmente seguras ou perigosas; elas se situam ao longo de um continuum de atividade. As variantes hipomórficas recém-definidas com alto GVSr atuam como guardiões de meio período: reduzem, mas não abolvem, as defesas naturais da célula contra o câncer. Para os pacientes, isso significa que alguns achados em TP53 reportados como incertos ou conflitantes podem, na verdade, conferir um aumento real, embora moderado, no risco. Reconhecer esse grupo e distingui‑lo da variação de fundo inócua permitirá aconselhamento genético mais nuançado, cronogramas de rastreamento mais adequados e, com o tempo, estratégias terapêuticas que explorem a função residual do TP53. Os autores estimam que tais variantes hipomórficas de baixa penetrância podem representar mais de um terço de todas as mutações TP53 fora dos hotspots, sublinhando sua importância para a oncologia de precisão.
Citação: Rodriguez, L., Leroy, B., Toledo, F. et al. Low-penetrance TP53 variants are mainly hypomorphic: an underestimated issue with high clinical significance. npj Genom. Med. 11, 22 (2026). https://doi.org/10.1038/s41525-026-00568-x
Palavras-chave: variantes TP53, mutações hipomórficas, risco de câncer de baixa penetrância, aconselhamento genético, oncologia de precisão