Clear Sky Science · it
Le varianti TP53 a bassa penetranza sono principalmente ipomorfiche: un problema sottovalutato con alta rilevanza clinica
Perché alcuni rischi ereditari di cancro passano inosservati
Il gene TP53, spesso chiamato il guardiano del nostro DNA, è noto per il suo ruolo cruciale nell’impedire la trasformazione cellulare in senso tumorale. I medici sanno da tempo che alcune mutazioni rare e di tipo "tutto o niente" in TP53 possono quasi garantire l’insorgenza di tumori in età giovane. Questo articolo esplora un lato più discreto e molto meno compreso di TP53: variazioni ereditate che indeboliscono, ma non annullano completamente, la capacità protettiva del gene. Queste varianti sfumate sono molto più comuni di quanto si pensasse e potrebbero ridefinire come valutiamo il rischio di cancro e pianifichiamo lo screening per molte famiglie.
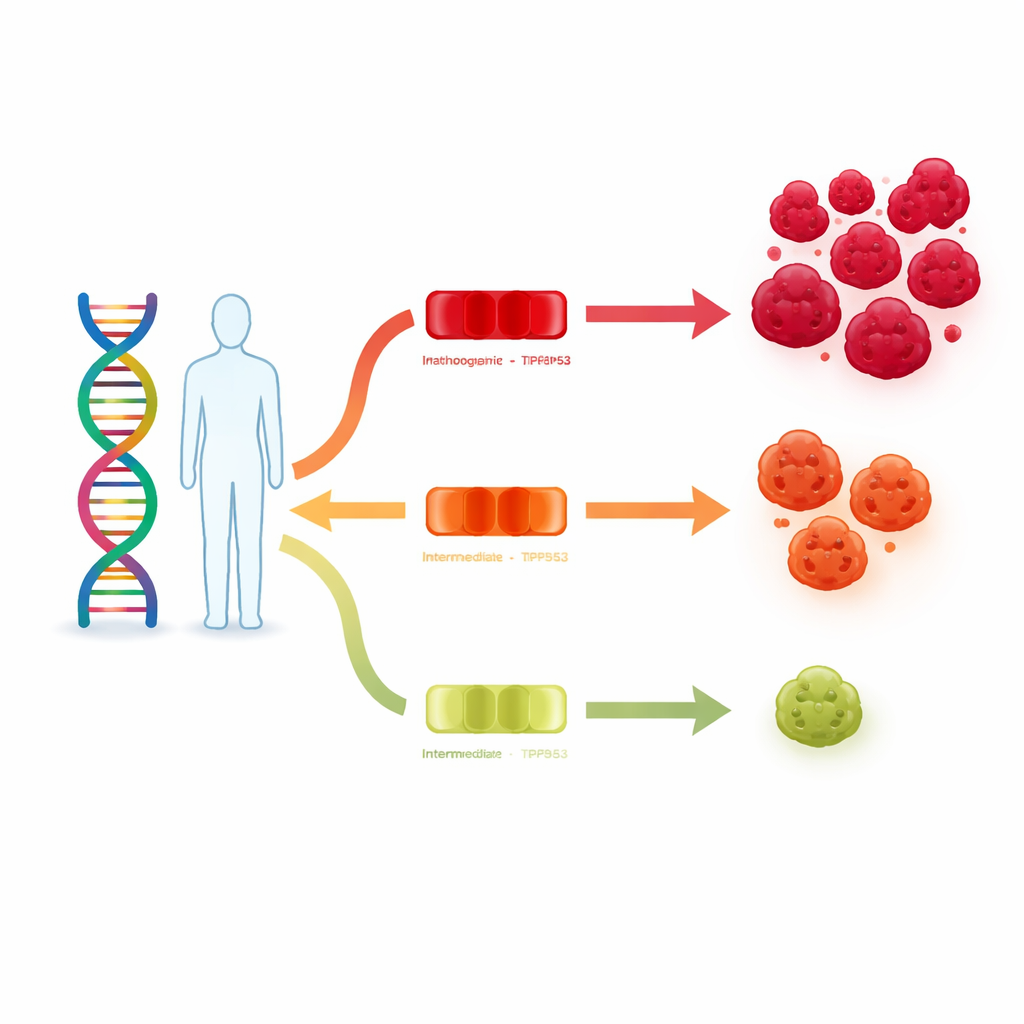
Un gene guardiano con molte sfumature di forza
TP53 indica alle cellule quando fermarsi, riparare i danni o autodistruggersi se il loro DNA è troppo compromesso. Le mutazioni classiche ad alto rischio di TP53, osservate nella sindrome di Li-Fraumeni, disattivano questo guardiano quasi del tutto, lasciando le persone con una probabilità molto elevata di sviluppare più tumori in giovane età. Tuttavia molte alterazioni di TP53 sono varianti missenso, che modificano una sola lettera del DNA e possono indebolire la proteina solo in parte. Finora, la maggior attenzione è stata rivolta alle forme più pericolose, mentre le varianti più lievi e a bassa penetranza — quelle che aumentano il rischio di cancro in modo modesto e non in tutti i portatori — sono rimaste in una zona grigia.
Trovare i colpevoli silenziosi nei vasti database di mutazioni
Gli autori hanno analizzato la release 2025 del database UMD_TP53, la più ampia raccolta di mutazioni di TP53 da tumori e casi ereditari nel mondo, e l’hanno incrociata con altri dataset tumorali e di popolazione. Si sono concentrati sulla frequenza con cui ciascuna variante TP53 appariva nei tumori (somatica) rispetto a essere ereditata (germinale), calcolando un “rapporto germinale-versus-somatico” (GVSr). La maggior parte delle mutazioni oncogeniche di TP53 mostra rapporti bassi, comparendo frequentemente come alterazioni acquisite nei tumori. Al contrario, il gruppo ha identificato un insieme distinto di varianti con GVSr insolitamente elevati: comparivano sproporzionatamente spesso come alterazioni ereditate ma risultavano solo modestamente rappresentate come driver autonomi nei tumori. Molte di queste erano già state segnalate in famiglie con pattern tumorali atipici o più lievi, suggerendo che potrebbero costituire una classe speciale a bassa penetranza.
Guardiani part-time: cosa rivelano i test funzionali
Per comprendere cosa fanno realmente queste varianti ad alto GVSr nelle cellule, i ricercatori hanno combinato dati provenienti da diversi esperimenti su larga scala che avevano testato sistematicamente migliaia di varianti TP53 in lieviti e cellule di mammifero. In questi saggi indipendenti è emerso lo stesso schema: le varianti ad alto GVSr raramente si comportavano come TP53 completamente inattivo, ma non erano neppure completamente normali. Mostravano invece un’attività intermedia — sufficiente ad attivare molti geni protettivi ma chiaramente più debole rispetto alla versione sana. I campioni tumorali e le linee cellulari tumorali portatori di queste varianti mostravano anch’essi solo un attenuamento parziale dei programmi genici controllati da TP53, a differenza dello spegnimento drammatico osservato con mutazioni hotspot o nonsense classiche. Complessivamente, questo colloca la maggior parte di queste varianti nella categoria “ipomorfica”: indebolite ma non annullate.
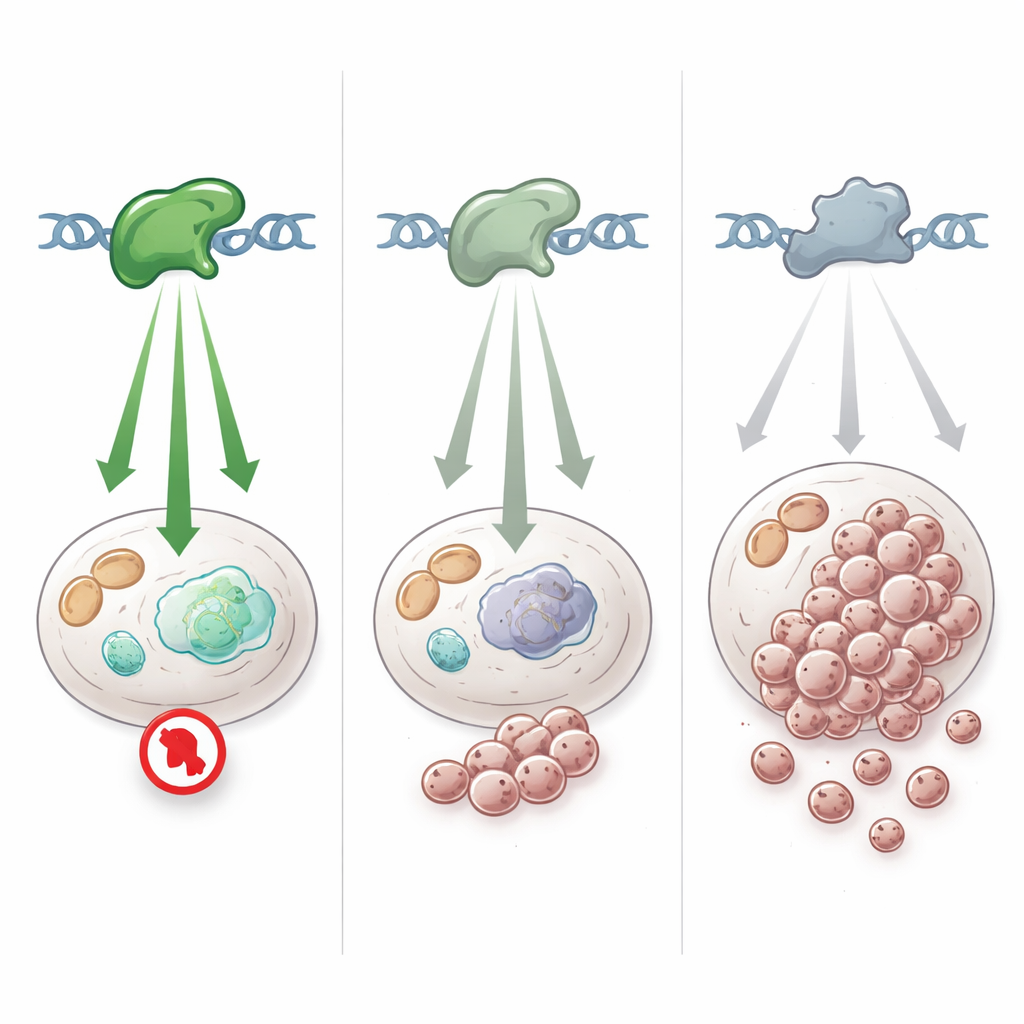
Come le varianti sottili modellano il rischio di cancro nella vita reale
Dati genetici e clinici suggeriscono che le persone che ereditano queste varianti ipomorfiche di TP53 affrontano uno spettro di rischio tumorale più basso e più variabile rispetto alla sindrome di Li-Fraumeni classica. Alcune varianti, come alterazioni nelle posizioni 181 o 337 della proteina, si concentrano in popolazioni particolari e sono associate a tassi aumentati di certi tumori, come alcuni carcinomi della mammella o tumori surrenalici infantili, ma con penetranza incompleta — molti portatori non sviluppano mai un tumore o lo fanno in età più avanzata. I tumori che insorgono nei portatori spesso acquisiscono una seconda mutazione TP53 più distruttiva, implicando che la variante più debole da sola non sia sufficiente per avviare il cancro ma possa comunque contribuire al rischio quando combinata con altri eventi o geni modificatori.
Cosa significa per i pazienti e le loro famiglie
Questo lavoro mostra che molte varianti ereditarie di TP53 non sono semplicemente sicure o pericolose; si collocano lungo un continuum di effetto. Le varianti ipomorfiche recentemente identificate con alto GVSr agiscono come guardiani part-time: riducono, ma non abolicono, le difese naturali della cellula contro il cancro. Per i pazienti ciò significa che alcune varianti TP53 segnalate come di significato incerto o contrastante potrebbero in realtà comportare un aumento reale, seppure moderato, del rischio. Riconoscere questo gruppo e distinguerlo dalla variazione neutrale di fondo consentirà una consulenza genetica più sfumata, programmi di screening più mirati e, col tempo, strategie terapeutiche che sfruttino la funzione residua di TP53. Gli autori stimano che tali varianti ipomorfiche a bassa penetranza potrebbero rappresentare più di un terzo di tutte le mutazioni TP53 non hotspot, sottolineandone l’importanza per l’oncologia di precisione.
Citazione: Rodriguez, L., Leroy, B., Toledo, F. et al. Low-penetrance TP53 variants are mainly hypomorphic: an underestimated issue with high clinical significance. npj Genom. Med. 11, 22 (2026). https://doi.org/10.1038/s41525-026-00568-x
Parole chiave: varianti TP53, mutazioni ipomorfiche, rischio di cancro a bassa penetranza, consulenza genetica, oncologia di precisione