Clear Sky Science · pl
Warianty TP53 o niskiej penetracji są głównie hipomorficzne: niedoszacowany problem o dużym znaczeniu klinicznym
Dlaczego niektóre dziedziczne ryzyka nowotworowe pozostają niewidoczne
Gen TP53, często nazywany strażnikiem naszego DNA, jest znany z kluczowej roli w powstrzymywaniu komórek przed przemianą w nowotwór. Lekarze od dawna wiedzą, że pewne rzadkie, „wszystko albo nic” mutacje TP53 mogą niemal gwarantować rozwój raka we wczesnym wieku. Niniejszy artykuł bada jednak cichszą, dużo mniej zrozumianą stronę TP53: dziedziczne zmiany, które osłabiają, ale nie całkowicie niszczą ochronną funkcję genu. Te subtelne warianty są znacznie częstsze, niż sądzono dotychczas, i mogą zmienić sposób oceny ryzyka nowotworowego oraz planowania badań przesiewowych dla wielu rodzin.
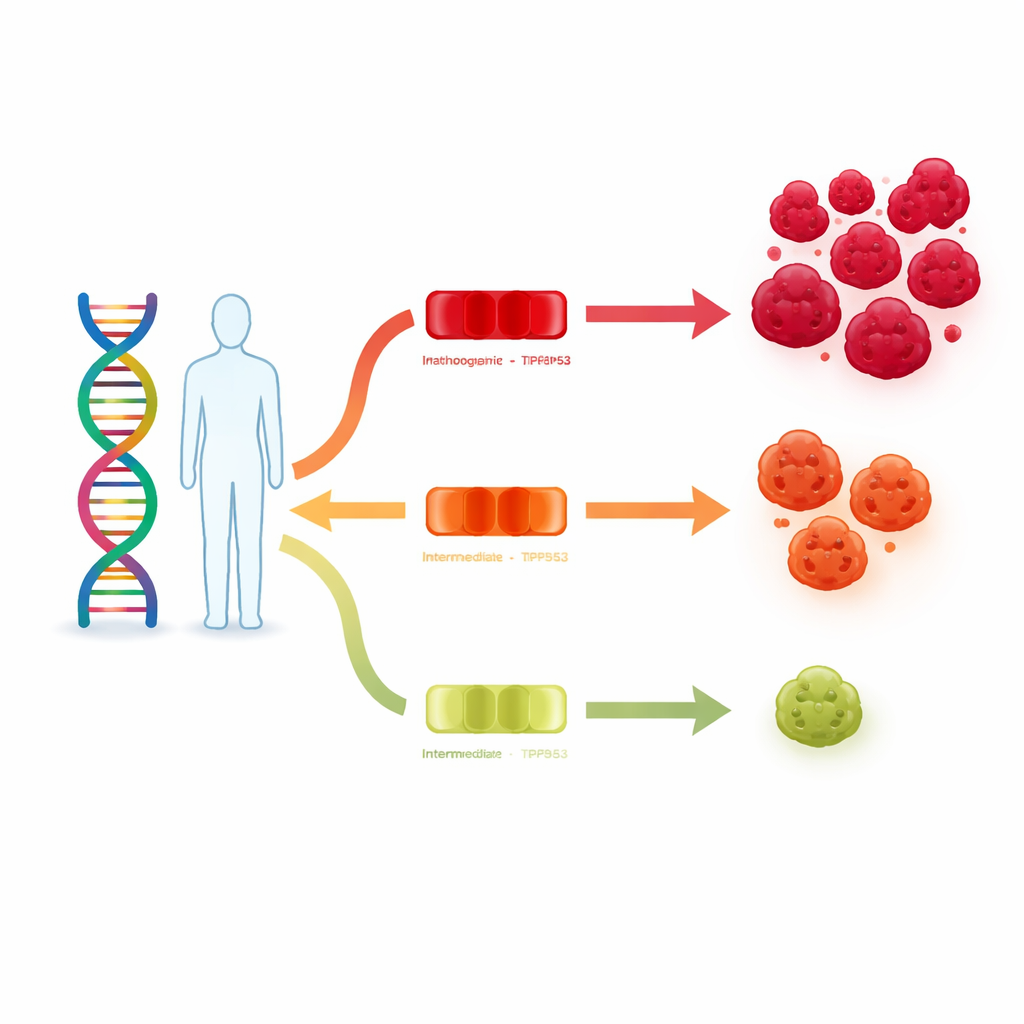
Kluczowy gen-strażnik o różnych stopniach siły
TP53 informuje komórki, kiedy mają się zatrzymać, naprawić uszkodzenia lub ulec samozniszczeniu, jeśli ich DNA jest zbyt zniszczone. Klasyczne mutacje TP53 o wysokim ryzyku, obserwowane w zespole Li-Fraumeni, praktycznie wyłączają tego strażnika, co wiąże się z bardzo dużym prawdopodobieństwem wystąpienia wielu nowotworów we wczesnym wieku. Jednak wiele zmian w TP53 to warianty missense, które zamieniają tylko jedną literę DNA i mogą jedynie częściowo osłabić białko. Do tej pory większość uwagi poświęcano najniebezpieczniejszym formom, podczas gdy łagodniejsze warianty o niskiej penetracji — podnoszące ryzyko raka tylko umiarkowanie i nie u każdego nosiciela — pozostawały w strefie szarości.
Wykrywanie cichych sprawców w ogromnych bazach mutacji
Autorzy przeanalizowali wydanie bazy UMD_TP53 z 2025 roku, największy zbiór mutacji TP53 z guzów i przypadków dziedzicznych na świecie, i skonfrontowali go z innymi zestawami danych onkologicznych i populacyjnych. Skupili się na częstości występowania poszczególnych wariantów TP53 w guzach (somatycznych) w porównaniu z wariantami dziedzicznymi (germinalnymi), obliczając „stosunek germline-versus-somatic” (GVSr). Większość napędzających nowotwór mutacji TP53 wykazuje niskie stosunki, pojawiając się często jako zmiany nabyte w guzach. W przeciwieństwie do tego zespół odkrył wyraźną grupę wariantów o nietypowo wysokim GVSr: występowały one nieproporcjonalnie często jako zmiany dziedziczne, ale były tylko umiarkowanie reprezentowane jako samodzielne czynniki napędzające w guzach. Wiele z nich już wcześniej zgłaszano w rodzinach z nietypowymi lub łagodniejszymi wzorcami nowotworowymi, co sugeruje, że mogą one tworzyć odrębną klasę o niskiej penetracji.
Stróżowie na pół etatu: co ujawniają testy funkcjonalne
Aby zrozumieć, co te warianty o wysokim GVSr faktycznie robią w komórkach, badacze połączyli dane z kilku dużych eksperymentów, które systematycznie testowały tysiące wariantów TP53 w drożdżach i komórkach ssaków. We wszystkich tych niezależnych testach wyłonił się ten sam wzorzec: warianty o wysokim GVSr rzadko zachowywały się jak całkowicie uszkodzony TP53, ale też nie były w pełni normalne. Zamiast tego wykazywały aktywność pośrednią — na tyle silną, by aktywować wiele genów ochronnych, lecz wyraźnie słabszą niż wersja zdrowa. Próbki guzów i linie komórkowe raka z tymi wariantami także pokazywały jedynie częściowe osłabienie programów genów kontrolowanych przez TP53, w przeciwieństwie do dramatycznego wyciszenia obserwowanego przy klasycznych hotspotowych lub nonsensownych mutacjach. W sumie większość tych wariantów można zaklasyfikować jako „hipomorficzne”: osłabione, ale nie zniszczone.
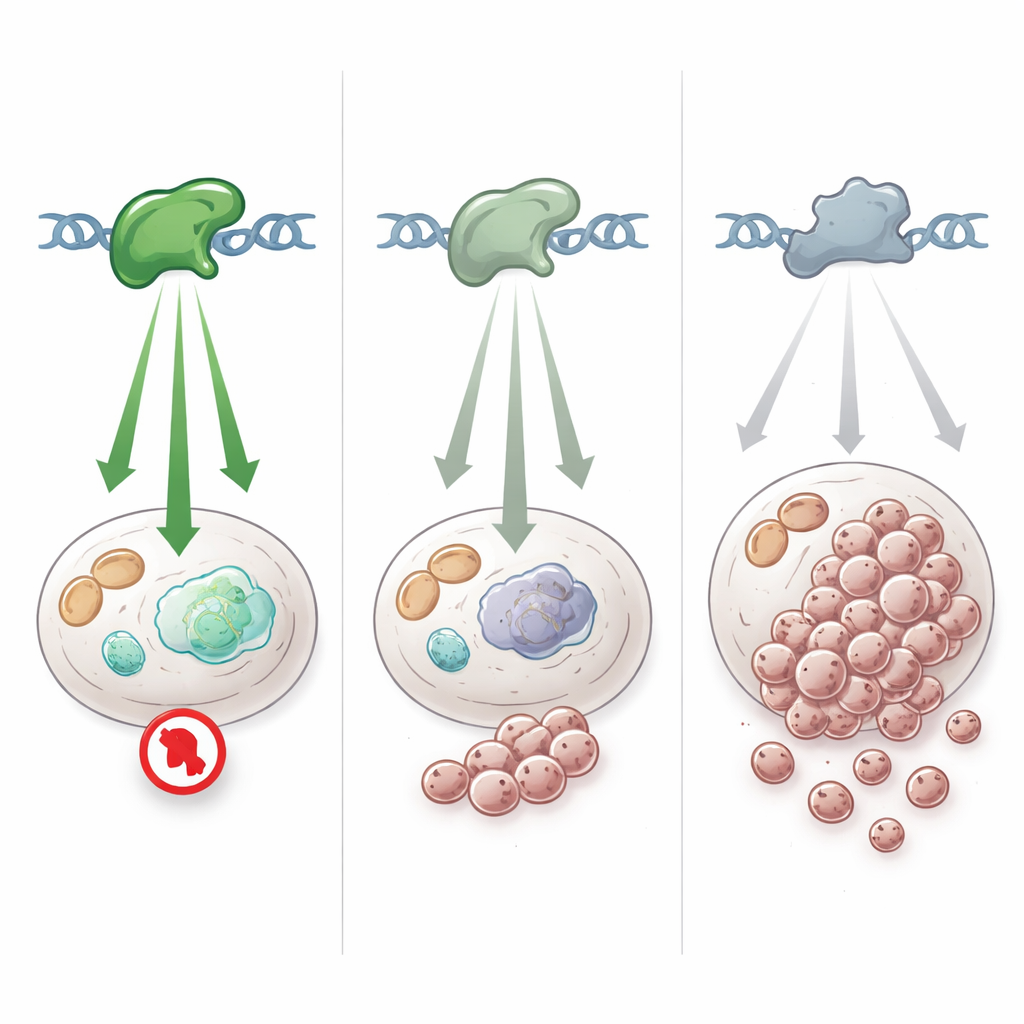
Jak subtelne warianty kształtują ryzyko raka w praktyce
Dane genetyczne i kliniczne sugerują, że osoby dziedziczące te hipomorficzne warianty TP53 stoją przed wachlarzem ryzyka nowotworowego, które jest niższe i bardziej zmienne niż w klasycznym zespole Li-Fraumeni. Niektóre warianty, takie jak zmiany w pozycjach 181 lub 337 białka, koncentrują się w określonych populacjach i wiążą się ze zwiększoną zapadalnością na pewne nowotwory, np. raka piersi czy dziecięce guzy nadnerczy, ale z niepełną penetracją — wielu nosicieli wcale nie rozwija raka albo robi to później w życiu. Guzy rozwijające się u nosicieli często zyskują drugą, bardziej destrukcyjną mutację TP53, co sugeruje, że słabszy wariant sam w sobie nie jest wystarczający do wywołania nowotworu, lecz może przyczyniać się do ryzyka w połączeniu z dodatkowymi uszkodzeniami lub modyfikującymi genami.
Co to oznacza dla pacjentów i ich rodzin
Praca ta pokazuje, że wiele dziedzicznych wariantów TP53 nie jest po prostu bezpiecznych lub niebezpiecznych; leżą one na kontinuum siły działania. Nowo zdefiniowane warianty o wysokim GVSr, hipomorficzne, działają jak strażnicy na pół etatu: osłabiają, ale nie likwidują naturalnych mechanizmów obronnych komórki przed rakiem. Dla pacjentów oznacza to, że niektóre wyniki TP53 opisywane jako niejednoznaczne lub sprzeczne mogą w rzeczywistości wiązać się z realnym, choć umiarkowanym, wzrostem ryzyka. Rozpoznanie tej grupy i oddzielenie jej od nieszkodliwych wariantów tła pozwoli na bardziej wyrafinowane poradnictwo genetyczne, lepiej dopasowane programy badań przesiewowych oraz w przyszłości strategie terapeutyczne wykorzystujące zachowaną funkcję TP53. Autorzy szacują, że takie warianty o niskiej penetracji i hipomorficznym charakterze mogą stanowić ponad jedną trzecią wszystkich wariantów TP53 poza hotspotami, podkreślając ich znaczenie dla onkologii precyzyjnej.
Cytowanie: Rodriguez, L., Leroy, B., Toledo, F. et al. Low-penetrance TP53 variants are mainly hypomorphic: an underestimated issue with high clinical significance. npj Genom. Med. 11, 22 (2026). https://doi.org/10.1038/s41525-026-00568-x
Słowa kluczowe: warianty TP53, mutacje hipomorficzne, ryzyko raka o niskiej penetracji, poradnictwo genetyczne, onkologia precyzyjna