Clear Sky Science · pt
CRAGE-RB-PI-seq revela a dinâmica transcricional de bactérias associadas a plantas durante a colonização das raízes
Por que a vida oculta nas raízes importa
Cada raiz de planta é cercada por uma cidade subterrânea movimentada de micróbios que ajudam as plantas a crescer, combater doenças ou, às vezes, causá‑las. Ainda assim, apesar de ferramentas poderosas de DNA que nos dizem quem está lá, sabemos surpreendentemente pouco sobre o que essas bactérias estão realmente fazendo enquanto vivem nas raízes. Este estudo apresenta uma nova forma de “escutar” milhares de genes bacterianos ao mesmo tempo enquanto micróbios benéficos colonizam raízes de plantas, revelando como eles se adaptam, cooperam com a planta e driblam suas defesas.
Observando interruptores bacterianos ligar e desligar
Os genes nas bactérias são controlados por pequenas regiões de DNA chamadas promotores, que funcionam como interruptores liga‑desliga. Medir a atividade desses interruptores dentro das plantas tem sido muito difícil porque o RNA vegetal ofusca a pequena quantidade de RNA bacteriano. Os autores resolveram isso construindo uma biblioteca especial de promotores de uma conhecida bactéria benéfica de raízes, Pseudomonas simiae WCS417, e marcando cada promotor com um código de barras de DNA único. Em seguida, inseriram esses interruptores codificados no cromossomo bacteriano usando uma plataforma versátil de engenharia genética, permitindo rastrear a atividade de milhares de interruptores genéticos apenas lendo seus códigos de barras.
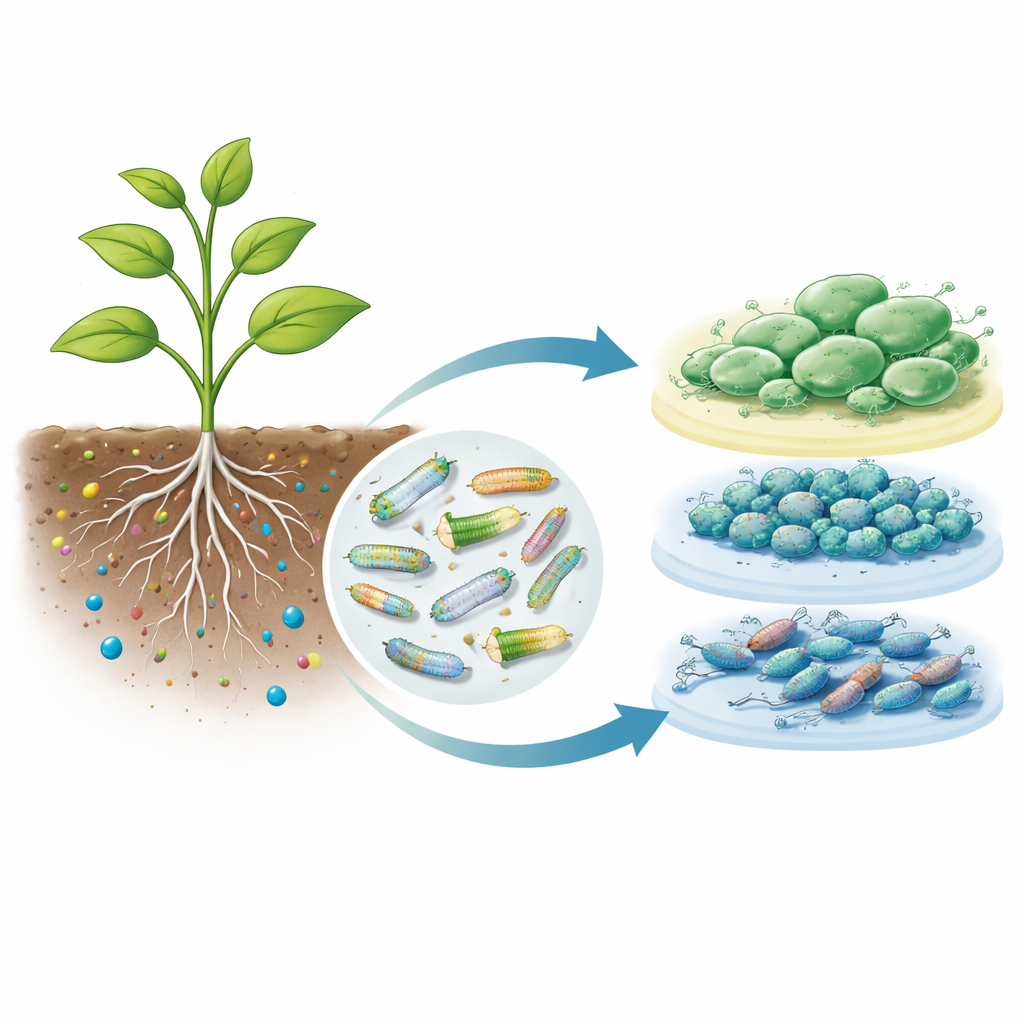
Uma nova maneira de ler o comportamento bacteriano nas raízes
O novo fluxo de trabalho, chamado CRAGE-RB-PI-seq, funciona em duas etapas. Primeiro, segmentos curtos de DNA imediatamente a montante de mais de 5.000 genes bacterianos foram sintetizados e agrupados em bibliotecas, cada segmento ligado a um código de barras aleatório. Essas bibliotecas foram integradas em um local seguro do genoma bacteriano para que as células permanecessem saudáveis. Quando as bactérias modificadas foram cultivadas em diferentes meios de laboratório, as leituras dos códigos de barras corresponderam de perto ao sequenciamento tradicional de RNA, confirmando que os códigos refletiam fielmente a atividade dos promotores. Essa etapa mostrou que o método pode detectar com precisão quais interruptores bacterianos respondem a mudanças de nutrientes ou estresse.
Acompanhando a colonização do primeiro contato até a estadia de longo prazo
Os pesquisadores então saíram dos frascos para plantas vivas, permitindo que as bactérias modificadas colonizassem as raízes de plântulas jovens de Arabidopsis. Ao amostrar raízes minutos, horas e dias após a inoculação, acompanharam como a atividade dos promotores mudou ao longo do tempo. No início, genes ligados ao movimento e à detecção de sinais químicos foram fortemente ativados, sugerindo que as bactérias rapidamente nadam em direção e exploram a superfície da raiz. Em poucas horas, interruptores que controlam crescimento e uso de nutrientes ligaram, à medida que as bactérias começaram a se alimentar de exsudatos radiculares. Mais tarde, outros conjuntos de interruptores se tornaram dominantes, incluindo os envolvidos na formação de biofilmes protetores e no gerenciamento do estresse, marcando uma transição de crescimento rápido para residência de longo prazo.
Como bactérias amigas driblam as defesas das plantas
Os dados com resolução temporal também destacaram um punhado de genes que ajudam a bactéria a viver pacificamente nas raízes ao domesticar as defesas da planta. Alguns promotores dirigiam genes que produzem moléculas conhecidas por reduzir a acidez local e atenuar respostas imunes da planta. Outros ligaram muito mais tarde e estavam ligados à proteção contra espécies reativas de oxigênio e enzimas que podem degradar paredes celulares bacterianas. Ao estudar mutantes incapazes de produzir certas proteínas, como uma desidrogenase de xantina que ajuda a lidar com explosões oxidativas e um inibidor de lisozima que protege células contra enzimas que degradam paredes, a equipe mostrou que essas defesas de ação tardia são cruciais para a colonização bem‑sucedida das raízes.
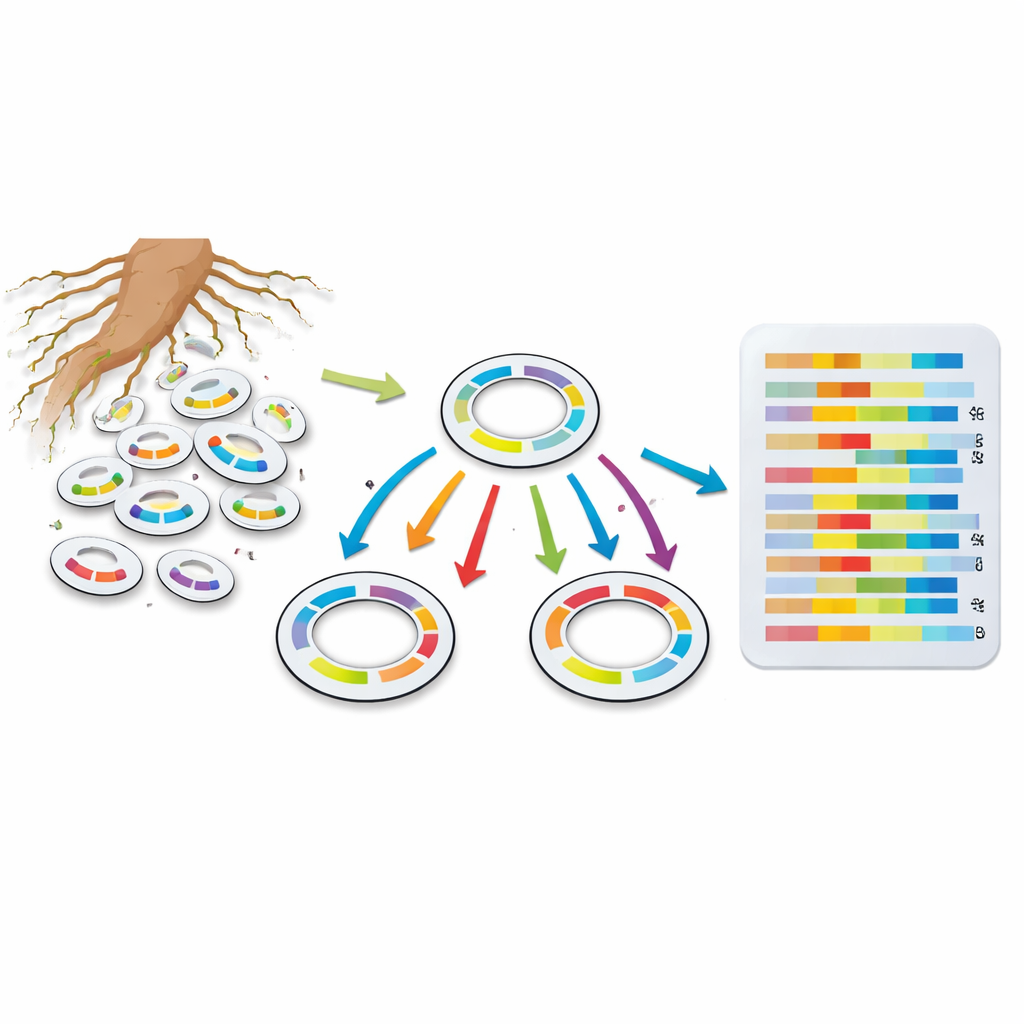
Levando a precisão do laboratório a solos do mundo real
Para ver se essa abordagem funciona fora de placas de ágar idealizadas, a equipe repetiu seus experimentos em um sistema parecido com solo, à base de argila. Embora o RNA bacteriano fosse mais escasso e as condições mais severas, o método de códigos de barras ainda forneceu padrões significativos. Em comparação com o sistema em placas, genes de metabolismo central foram menos ativos, enquanto funções de resposta ao estresse e de manutenção tornaram‑se mais importantes ao longo do tempo, compondo um quadro de bactérias se preparando para sobreviver em um ambiente mais difícil e pobre em nutrientes.
O que isso significa para as culturas futuras
Ao transformar milhares de interruptores genéticos invisíveis em códigos de barras legíveis, este estudo mostra como bactérias benéficas de raízes ajustam seus modos de vida ao primeiro contato com as raízes, ao crescer e ao se estabelecerem em uma parceria de longo prazo. Revela que comportamentos iniciais como movimento e alimentação cedem rapidamente lugar a traços que desarmam a imunidade vegetal e resistem ao estresse. Como o método pode, em princípio, ser aplicado a muitas espécies bacterianas diferentes, ele abre a porta para mapear sistematicamente como micróbios úteis se comportam em ambientes vegetais reais. Esse conhecimento poderia orientar o desenvolvimento de inoculantes microbianos e estratégias de engenharia que tornem as lavouras mais resilientes, produtivas e menos dependentes de insumos químicos.
Citação: Honda, T., Yu, S., Mai, D. et al. CRAGE-RB-PI-seq reveals transcriptional dynamics of plant-associated bacteria during root colonization. Nat Commun 17, 3021 (2026). https://doi.org/10.1038/s41467-026-69903-1
Palavras-chave: microbioma radicular, bactérias benéficas, regulação gênica, imunidade das plantas, biologia sintética