Clear Sky Science · es
CRAGE-RB-PI-seq revela la dinámica transcripcional de bacterias asociadas a las plantas durante la colonización de raíces
Por qué importa la vida oculta en las raíces
Cada raíz vegetal está rodeada por una bulliciosa ciudad subterránea de microbios que ayudan al crecimiento de la planta, la protegen frente a enfermedades o, en ocasiones, las causan. Sin embargo, a pesar de las potentes herramientas de ADN que nos dicen quiénes están allí, aún sabemos sorprendentemente poco sobre lo que estas bacterias hacen realmente mientras viven en las raíces. Este estudio presenta una nueva forma de “escuchar” miles de genes bacterianos a la vez mientras microbios beneficiosos colonizan las raíces de las plantas, revelando cómo se adaptan, cooperan con la planta y esquivan sus defensas.
Viendo cómo los interruptores bacterianos se encienden y apagan
Los genes en bacterias están controlados por cortas regiones de ADN llamadas promotores, que actúan como interruptores de encendido y apagado. Medir la actividad de estos interruptores dentro de las plantas ha sido muy difícil porque el ARN vegetal enmascara la pequeña cantidad de ARN bacteriano. Los autores resolvieron esto construyendo una biblioteca especial de promotores de una conocida bacteria beneficiosa de raíces, Pseudomonas simiae WCS417, y etiquetando cada promotor con una secuencia de ADN única (código de barras). Luego insertaron estos interruptores codificados por barras en el cromosoma bacteriano usando una plataforma de ingeniería genética versátil, lo que les permitió rastrear la actividad de miles de interruptores génicos simplemente leyendo sus códigos de barras.
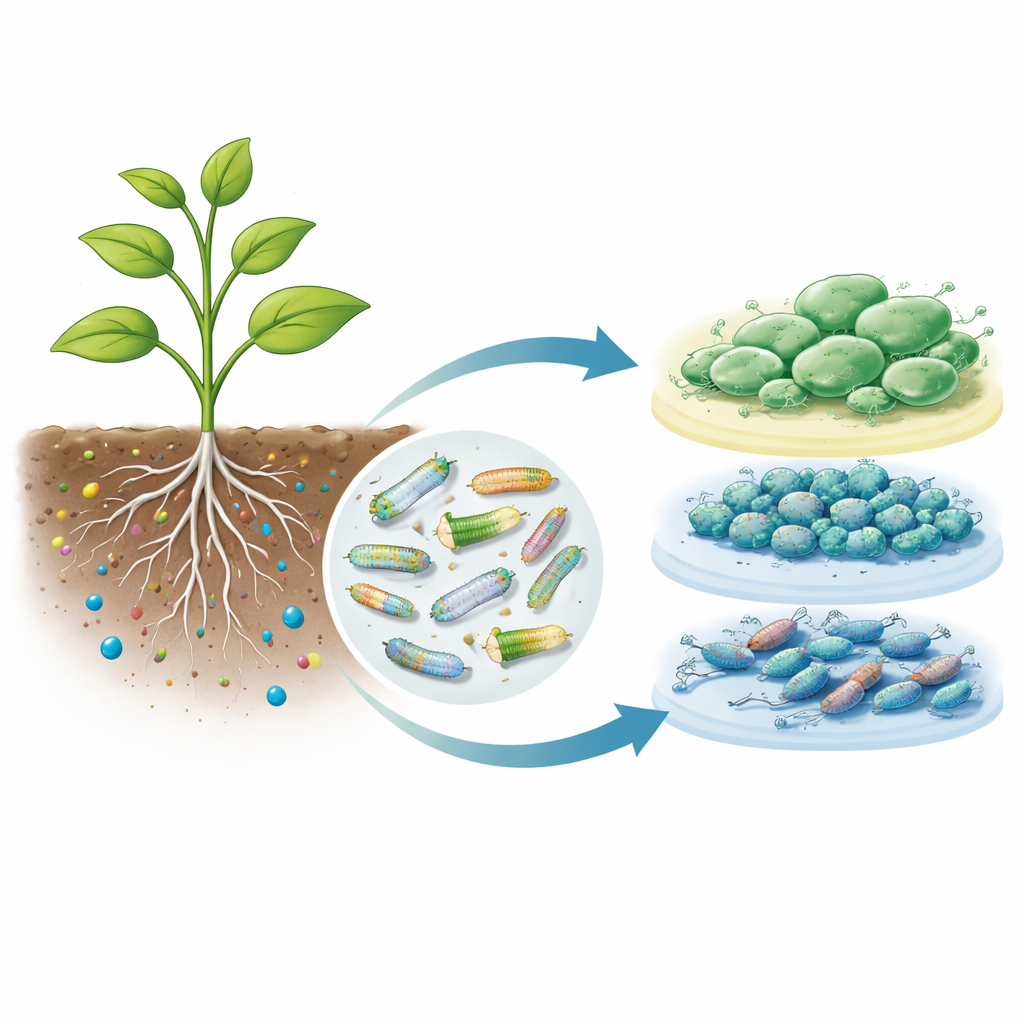
Una nueva forma de leer el comportamiento bacteriano en las raíces
El nuevo flujo de trabajo, denominado CRAGE-RB-PI-seq, funciona en dos etapas. Primero, se sintetizaron segmentos cortos de ADN inmediatamente aguas arriba de más de 5.000 genes bacterianos y se agruparon en bibliotecas, cada segmento vinculado a un código de barras aleatorio. Estas bibliotecas se integraron en un lugar seguro del genoma bacteriano para que las células permanecieran sanas. Cuando las bacterias modificadas se cultivaron en diferentes medios de laboratorio, las lecturas de los códigos de barras coincidieron estrechamente con la secuenciación tradicional de ARN, confirmando que los códigos de barras reflejaban fielmente la actividad de los promotores. Este paso demostró que el método puede detectar con precisión qué interruptores bacterianos responden a cambios en nutrientes o estrés.
Siguiendo la colonización desde el primer contacto hasta la estancia a largo plazo
Los investigadores pasaron luego de matraces a plantas vivas, permitiendo que las bacterias modificadas colonizaran las raíces de plántulas jóvenes de Arabidopsis. Mediante muestreos de raíces a los minutos, horas y días tras la inoculación, rastrearon cómo cambiaba la actividad de los promotores a lo largo del tiempo. Al principio, se activaron con fuerza genes vinculados al movimiento y la detección de sustancias químicas, lo que sugiere que las bacterias nadan rápidamente hacia y exploran la superficie de la raíz. A las pocas horas, se encendieron interruptores que controlan el crecimiento y el uso de nutrientes, cuando las bacterias empezaron a alimentarse de los exudados radiculares. Más tarde, otros conjuntos de interruptores se hicieron dominantes, incluidos los implicados en la formación de biofilms protectores y la gestión del estrés, marcando una transición del crecimiento rápido a la residencia a largo plazo.
Cómo las bacterias amistosas evitan las defensas vegetales
Los datos temporales también destacaron un puñado de genes que ayudan a la bacteria a convivir pacíficamente en las raíces al atenuar las defensas de la planta. Algunos promotores impulsaron genes que producen moléculas conocidas por reducir la acidez local y suavizar las respuestas inmunitarias de la planta. Otros se activaron mucho más tarde y se asociaron con la protección frente a especies reactivas de oxígeno y enzimas que pueden degradar las paredes celulares bacterianas. Al estudiar mutantes incapaces de producir ciertas proteínas, como una xantina deshidrogenasa que ayuda a sobrellevar estallidos oxidativos y un inhibidor de lisozimas que protege las células de enzimas que degradan la pared, el equipo mostró que estas defensas de acción tardía son cruciales para la colonización exitosa de las raíces.
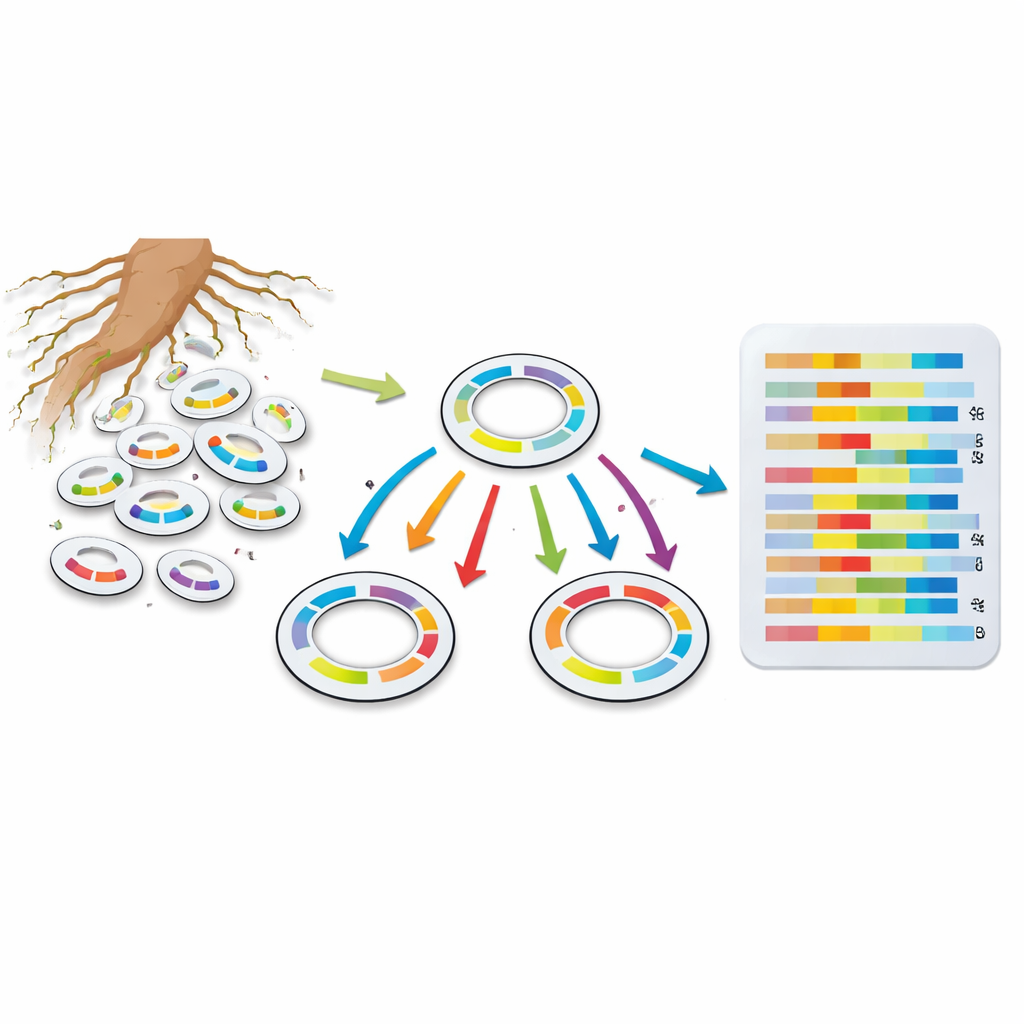
Llevando la precisión de laboratorio a suelos del mundo real
Para ver si este enfoque funciona fuera de placas de agar idealizadas, el equipo repitió sus experimentos en un sistema similar a suelo, a base de arcilla. Aunque el ARN bacteriano era más escaso y las condiciones más duras, el método de códigos de barras aún proporcionó patrones significativos. En comparación con el sistema en placa, los genes de metabolismo central estaban menos activos, mientras que las funciones de respuesta al estrés y mantenimiento se volvieron más importantes con el tiempo, encajando con una imagen de bacterias preparándose para sobrevivir en un entorno más duro y pobre en nutrientes.
Qué significa esto para los cultivos del futuro
Al convertir miles de interruptores genéticos invisibles en códigos de barras legibles, este estudio muestra cómo las bacterias beneficiosas de la raíz ajustan su estilo de vida desde que aterrizan en las raíces, crecen y se establecen en una asociación a largo plazo. Revela que comportamientos tempranos como el movimiento y la alimentación dan paso rápidamente a rasgos que desactivan la inmunidad vegetal y resisten el estrés. Dado que, en principio, el método puede aplicarse a muchas especies bacterianas diferentes, abre la puerta a mapear de forma sistemática cómo se comportan los microbios útiles dentro de entornos vegetales reales. Ese conocimiento podría guiar el diseño de inoculantes microbianos y estrategias de ingeniería que hagan los cultivos más resistentes, productivos y menos dependientes de insumos químicos.
Cita: Honda, T., Yu, S., Mai, D. et al. CRAGE-RB-PI-seq reveals transcriptional dynamics of plant-associated bacteria during root colonization. Nat Commun 17, 3021 (2026). https://doi.org/10.1038/s41467-026-69903-1
Palabras clave: microbioma radicular, bacterias beneficiosas, regulación génica, inmunidad vegetal, biología sintética