Clear Sky Science · fr
CRAGE-RB-PI-seq révèle la dynamique transcriptionnelle des bactéries associées aux plantes lors de la colonisation des racines
Pourquoi la vie cachée sur les racines est importante
Chaque racine végétale est entourée d’une ville souterraine animée de microbes qui aident les plantes à croître, à repousser les maladies, ou parfois à les provoquer. Pourtant, malgré des outils ADN puissants qui nous disent qui est présent, nous savons encore étonnamment peu sur ce que ces bactéries font réellement lorsqu’elles vivent sur les racines. Cette étude présente une nouvelle manière « d’écouter » des milliers de gènes bactériens en même temps pendant que des microbes symbiotiques colonisent les racines, révélant comment ils s’adaptent, coopèrent avec la plante et contournent ses défenses.
Observer l’allumage et l’extinction des interrupteurs bactériens
Les gènes bactériens sont contrôlés par de courtes régions d’ADN appelées promoteurs, qui agissent comme des interrupteurs on/off. Mesurer l’activité de ces interrupteurs à l’intérieur des plantes a été très difficile parce que l’ARN végétal noie la quantité infime d’ARN bactérien. Les auteurs ont résolu ce problème en construisant une bibliothèque spéciale de promoteurs provenant d’une bactérie racinaire bénéfique bien connue, Pseudomonas simiae WCS417, et en marquant chaque promoteur avec un code-barres d’ADN unique. Ils ont ensuite inséré ces interrupteurs codés dans le chromosome bactérien à l’aide d’une plateforme d’ingénierie génétique polyvalente, leur permettant de suivre l’activité de milliers d’interrupteurs géniques simplement en lisant leurs codes-barres.
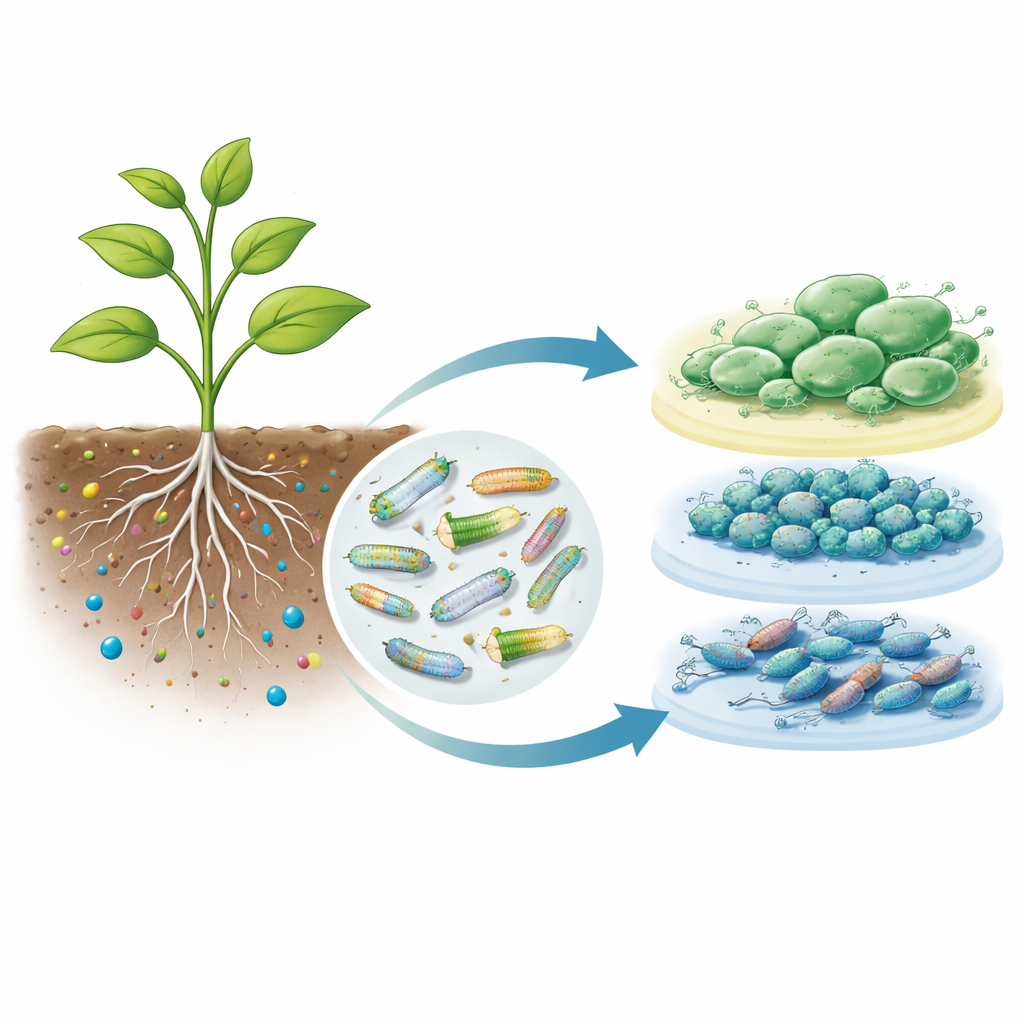
Une nouvelle façon de lire le comportement bactérien sur les racines
Le nouveau protocole, appelé CRAGE-RB-PI-seq, fonctionne en deux étapes. D’abord, de courts segments d’ADN situés juste en amont de plus de 5 000 gènes bactériens ont été synthétisés et regroupés en bibliothèques, chaque segment lié à un code-barres aléatoire. Ces bibliothèques ont été intégrées à un emplacement sûr du génome bactérien afin de préserver la santé des cellules. Lorsque les bactéries modifiées ont été cultivées dans différents milieux de laboratoire, les lectures des codes-barres correspondaient étroitement au séquençage d’ARN traditionnel, confirmant que les codes-barres reflètent fidèlement l’activité des promoteurs. Cette étape a montré que la méthode peut détecter avec précision quels interrupteurs bactériens répondent aux changements de nutriments ou au stress.
Suivre la colonisation du premier contact à l’établissement à long terme
Les chercheurs sont ensuite passés des flacons aux plantes vivantes, laissant les bactéries modifiées coloniser les racines de jeunes semis d’Arabidopsis. En échantillonnant les racines quelques minutes, heures et jours après l’inoculation, ils ont suivi l’évolution de l’activité des promoteurs au fil du temps. Au début, les gènes liés au mouvement et à la détection de molécules étaient fortement activés, suggérant que les bactéries nagent rapidement vers la surface racinaire et l’explorent. En quelques heures, les interrupteurs contrôlant la croissance et l’utilisation des nutriments se sont activés alors que les bactéries commençaient à se nourrir des exsudats racinaires. Plus tard, d’autres ensembles d’interrupteurs sont devenus dominants, notamment ceux impliqués dans la formation de biofilms protecteurs et la gestion du stress, marquant une transition d’une croissance rapide vers une résidence à long terme.
Comment les bactéries amies contournent les défenses des plantes
Les données temporelles ont également mis en évidence une poignée de gènes aidant la bactérie à vivre paisiblement sur les racines en modérant les défenses de la plante. Certains promoteurs régulaient des gènes produisant des molécules connues pour diminuer l’acidité locale et atténuer les réponses immunitaires de la plante. D’autres s’activaient beaucoup plus tard et étaient liés à la protection contre les espèces réactives de l’oxygène et aux enzymes pouvant dégrader les parois bactériennes. En étudiant des mutants incapables de produire certaines protéines, comme une xanthine déshydrogénase qui aide à gérer les explosions oxydatives et un inhibiteur de lysozyme qui protège les cellules des enzymes dégradant la paroi, l’équipe a montré que ces défenses à action tardive sont cruciales pour une colonisation racinaire réussie.
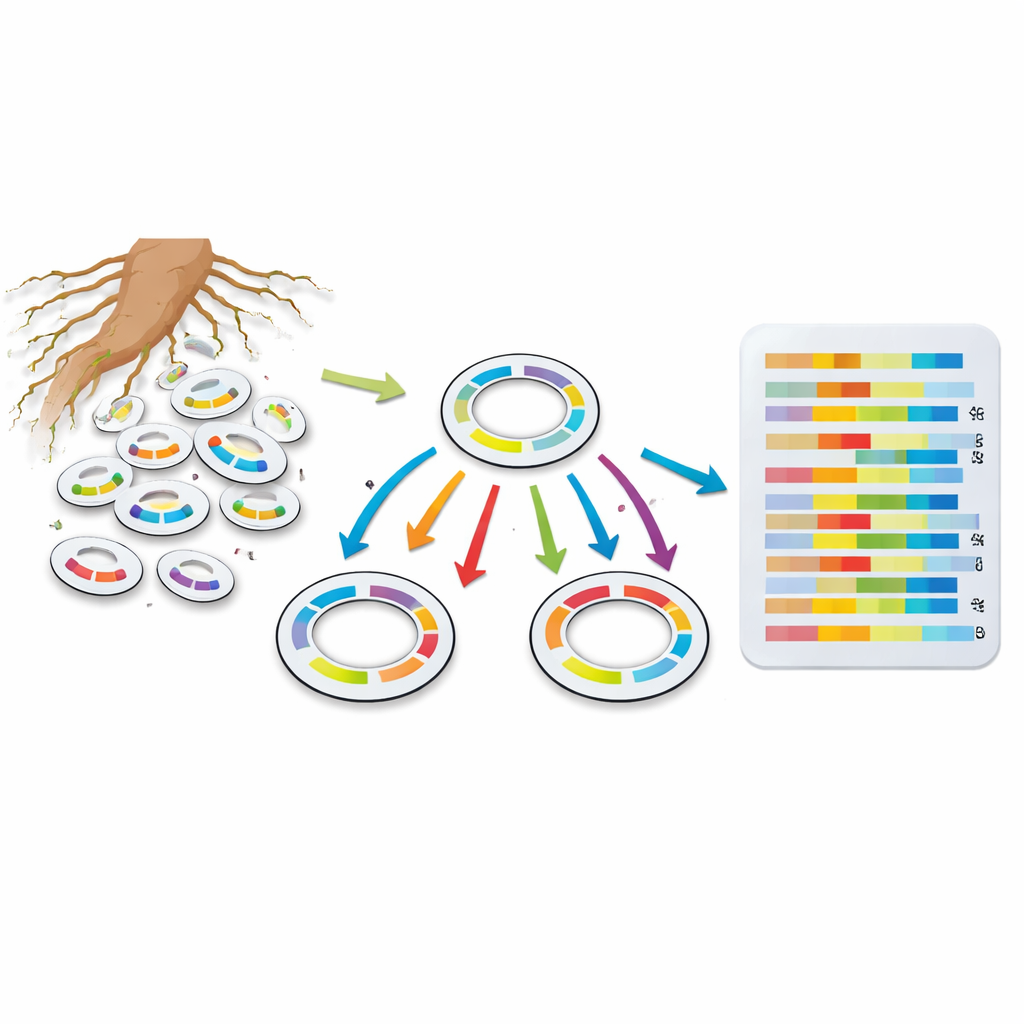
Apporter la précision du laboratoire aux sols du monde réel
Pour tester si cette approche fonctionne en dehors des plaques d’agar idéalisées, l’équipe a répété ses expériences dans un dispositif argileux imitant le sol. Même si l’ARN bactérien était plus rare et que les conditions plus rudes, la méthode par codes-barres a encore fourni des schémas significatifs. Par rapport au système sur plaque, les gènes du métabolisme central étaient moins actifs, tandis que les fonctions de réponse au stress et de maintenance prenaient de l’importance avec le temps, correspondant à un tableau où les bactéries se replient pour survivre dans un environnement plus difficile et pauvre en nutriments.
Ce que cela annonce pour les cultures futures
En transformant des milliers d’interrupteurs génétiques invisibles en codes-barres lisibles, cette étude montre comment les bactéries racinaires bénéfiques ajustent leur mode de vie lorsqu’elles arrivent sur les racines, croissent et s’installent dans un partenariat à long terme. Elle révèle que des comportements précoces comme le mouvement et l’alimentation cèdent rapidement la place à des traits qui désarment l’immunité des plantes et résistent au stress. Parce que la méthode peut, en principe, être appliquée à de nombreuses espèces bactériennes différentes, elle ouvre la voie à une cartographie systématique du comportement des microbes utiles dans des environnements végétaux réels. Ces connaissances pourraient guider la conception d’inoculants microbiens et de stratégies d’ingénierie pour rendre les cultures plus résilientes, productives et moins dépendantes des intrants chimiques.
Citation: Honda, T., Yu, S., Mai, D. et al. CRAGE-RB-PI-seq reveals transcriptional dynamics of plant-associated bacteria during root colonization. Nat Commun 17, 3021 (2026). https://doi.org/10.1038/s41467-026-69903-1
Mots-clés: microbiome racinaire, bactéries bénéfiques, régulation génique, immunité des plantes, biologie synthétique