Clear Sky Science · de
CRAGE-RB-PI-seq enthüllt die Transkriptionsdynamik pflanzenassoziierter Bakterien während der Wurzelkolonisierung
Warum das verborgene Leben an Wurzeln wichtig ist
Jede Pflanzenwurzel ist von einer geschäftigen unterirdischen Stadt aus Mikroben umgeben, die Pflanzen beim Wachsen helfen, Krankheit abwehren oder sie manchmal verursachen. Trotz leistungsfähiger DNA-Methoden, die sagen, wer dort ist, wissen wir überraschend wenig darüber, was diese Bakterien tatsächlich tun, während sie auf den Wurzeln leben. Diese Studie stellt eine neue Methode vor, um „mitzuhören“ und gleichzeitig Tausende bakterieller Gene zu verfolgen, während nützliche Mikroben Wurzeln kolonisieren, und zeigt, wie sie sich anpassen, mit der Pflanze kooperieren und deren Abwehrmechanismen umgehen.
Beobachten, wie bakterielle Schalter an- und ausgeschaltet werden
Gene bei Bakterien werden von kurzen DNA-Regionen namens Promotoren gesteuert, die wie An-/Ausschalter wirken. Die Aktivität dieser Schalter in Pflanzen zu messen war sehr schwierig, weil Pflanzen-RNA die winzige Menge bakterieller RNA überlagert. Die Autoren lösten dieses Problem, indem sie eine spezielle Bibliothek von Promotoren eines bekannten nützlichen Wurzelbakteriums, Pseudomonas simiae WCS417, erstellten und jeden Promotor mit einem eindeutigen DNA-Barcode versehen. Diese barcodierten Schalter wurden dann mithilfe einer vielseitigen genetischen Plattform in das bakterielle Chromosom eingefügt, sodass sie die Aktivität von Tausenden Gen-Schaltern allein durch das Auslesen ihrer Barcodes verfolgen konnten.
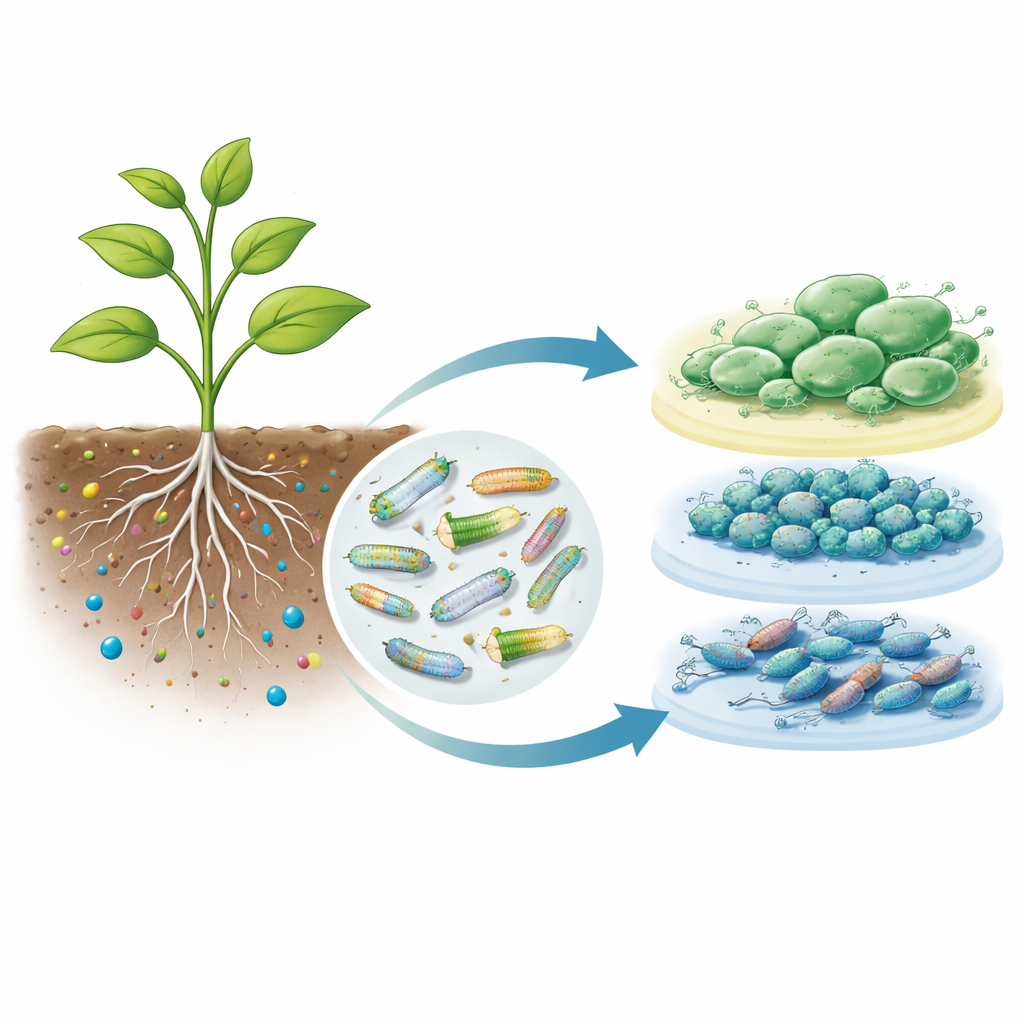
Eine neue Möglichkeit, bakterielles Verhalten an Wurzeln zu lesen
Der neue Arbeitsablauf, CRAGE-RB-PI-seq genannt, funktioniert in zwei Stufen. Zuerst wurden kurze DNA-Abschnitte direkt stromaufwärts von mehr als 5.000 bakteriellen Genen synthetisiert und in Bibliotheken gruppiert, wobei jeder Abschnitt mit einem zufälligen Barcode verknüpft war. Diese Bibliotheken wurden an einer sicheren Stelle im bakteriellen Genom integriert, sodass die Zellen gesund blieben. Wenn die ingenieurbiologisch veränderten Bakterien in verschiedenen Labormedien gezüchtet wurden, stimmten die Barcode-Auslesungen eng mit herkömmlicher RNA-Sequenzierung überein, was bestätigte, dass die Barcodes die Promotoraktivität zuverlässig widerspiegeln. Dieser Schritt zeigte, dass die Methode genau erkennen kann, welche bakteriellen Schalter auf Änderungen in Nährstoffen oder Stress reagieren.
Kolonisierung von erstem Kontakt bis zur langfristigen Ansiedlung verfolgen
Die Forscher gingen dann von Erlenmeyerkolben zu lebenden Pflanzen über und ließen die ingenieurisierten Bakterien die Wurzeln junger Arabidopsis-Sämlinge kolonisieren. Durch Probenahme der Wurzeln Minuten, Stunden und Tage nach der Inokulation verfolgten sie, wie sich die Promotoraktivität im Zeitverlauf änderte. Zu Beginn wurden Gene, die mit Bewegung und chemischer Wahrnehmung verknüpft sind, stark aktiviert, was darauf hindeutet, dass Bakterien schnell zur Wurzeloberfläche schwimmen und diese erkunden. Innerhalb weniger Stunden schalteten Promotoren, die Wachstum und Nährstoffnutzung steuern, ein, als die Bakterien begannen, von Wurzelexsudaten zu leben. Später dominierten andere Schalter, darunter solche für den Aufbau schützender Biofilme und für Stressmanagement, was einen Wechsel von schnellem Wachstum zu langfristigem Verweilen markiert.
Wie freundliche Bakterien pflanzliche Abwehr umgehen
Die zeitaufgelösten Daten hoben auch eine Handvoll Gene hervor, die dem Bakterium helfen, friedlich auf Wurzeln zu leben, indem sie pflanzliche Abwehrmaßnahmen abschwächen. Einige Promotoren trieben Gene an, die Moleküle produzieren, von denen bekannt ist, dass sie die lokale Säure verringern und pflanzliche Immunantworten abschwächen. Andere schalteten viel später und waren mit Schutz vor reaktiven Sauerstoffspezies sowie Enzymen verbunden, die bakterielle Zellwände angreifen können. Durch die Untersuchung von Mutanten, die bestimmte Proteine nicht herstellen können — etwa eine Xanthin-Dehydrogenase, die beim Umgang mit oxidativen Explosionen hilft, und einen Lysozym-Inhibitor, der Zellen vor wandabbauenden Enzymen schützt — zeigten die Autoren, dass diese spät wirkenden Abwehrmechanismen entscheidend für eine erfolgreiche Wurzelkolonisierung sind.
Laborpräzision ins reale Bodenleben bringen
Um zu prüfen, ob der Ansatz auch außerhalb idealisierter Agarplatten funktioniert, wiederholte das Team seine Experimente in einem tonbasierten, bodenähnlichen Aufbau. Obwohl bakterielle RNA dort seltener war und die Bedingungen härter, lieferte die Barcode-Methode weiterhin aussagekräftige Muster. Im Vergleich zum Plattensystem waren Gene für den zentralen Stoffwechsel weniger aktiv, während Stressreaktions- und Erhaltungsfunktionen mit der Zeit wichtiger wurden — ein Bild von Bakterien, die sich in einer raueren, nährstoffarmen Umgebung auf das Überleben einstellen.
Was das für zukünftige Kulturen bedeutet
Indem Tausende unsichtbarer genetischer Schalter in lesbare Barcodes verwandelt wurden, zeigt diese Studie, wie nützliche Wurzelbakterien ihren Lebensstil anpassen, wenn sie zuerst auf Wurzeln landen, wachsen und eine langfristige Partnerschaft eingehen. Sie offenbart, dass frühe Verhaltensweisen wie Bewegung und Nahrungsaufnahme schnell Merkmalen weichen, die die Pflanzenimmunität ausschalten und Stress widerstehen. Da die Methode prinzipiell auf viele verschiedene Bakterienarten anwendbar ist, öffnet sie die Tür zu systematischen Karten darüber, wie hilfreiche Mikroben in realen Pflanzenumgebungen agieren. Solches Wissen könnte die Entwicklung mikrobieller Inokulanzien und Engineering-Strategien leiten, die Pflanzen widerstandsfähiger, produktiver und weniger abhängig von chemischen Inputs machen.
Zitation: Honda, T., Yu, S., Mai, D. et al. CRAGE-RB-PI-seq reveals transcriptional dynamics of plant-associated bacteria during root colonization. Nat Commun 17, 3021 (2026). https://doi.org/10.1038/s41467-026-69903-1
Schlüsselwörter: Wurzelmikrobiom, nützliche Bakterien, Genregulation, Pflanzenimmunität, synthetische Biologie