Clear Sky Science · pt
Síntese catalítica térmica de amônia usando compósito de urânio/graphdiyne em condições brandas
Por que um novo caminho para a amônia é importante
A amônia é um gigante silencioso da vida moderna. Ela sustenta a produção de fertilizantes para a agricultura global e está surgindo como um potencial vetor de energia. Ainda assim, a forma como a produzimos atualmente — o processo Haber–Bosch centenário — consome enormes quantidades de combustíveis fósseis, opera em temperaturas escaldantes e pressões esmagadoras, e emite vastas quantidades de dióxido de carbono. Este estudo explora uma abordagem radicalmente diferente: um catalisador feito de átomos de urânio ancorados em uma folha ultrafina de carbono chamada graphdiyne, capaz de transformar nitrogênio e hidrogênio em amônia sob condições muito mais brandas, apontando para um futuro mais limpo para esse produto químico essencial.

Construindo um palco melhor para a reação
Os pesquisadores começam com graphdiyne, um material bidimensional de carbono formado por anéis de benzeno ligados por cadeias curtas de carbono. Sua estrutura cria poros triangulares, grande área superficial e uma lacuna eletrônica intrínseca que pode ser ajustada mudando o número de camadas empilhadas. Usando dióxido de carbono supercrítico, eles crescem folhas de graphdiyne extremamente finas, desde camada única até múltiplas camadas, e então medem cuidadosamente sua espessura e propriedades eletrônicas. Eles descobrem que, à medida que mais camadas são adicionadas, a banda proibida do material diminui de forma previsível e que uma versão de cinco camadas oferece um panorama eletrônico particularmente favorável para interagir com metais e ativar o nitrogênio.
Emparelhando urânio com carbono sob medida
Para transformar essa folha de carbono em um catalisador funcional, a equipe introduz urânio usando uma solução reativa de iodeto de urânio. Camadas finas de graphdiyne são destruídas por esse tratamento, então eles partem de um filme de oito camadas e o corroem parcialmente, terminando com um andaime estável de graphdiyne de cinco camadas decorado com minúsculos aglomerados de urânio. Microscopia eletrônica avançada mostra que esses aglomerados são formados por apenas alguns átomos de urânio, espaçados de maneira regular na rede de carbono em distâncias bem adequadas para “agarrar” uma molécula de nitrogênio entre dois sítios metálicos vizinhos. Medidas espectroscópicas confirmam que o urânio se encontra principalmente em estados de oxidação intermediários e que elétrons fluem do urânio para o graphdiyne, remodelando sutilmente os orbitais 5f do metal, que são conhecidos por serem poderosos, porém difíceis de controlar nas ligações químicas.
Produzindo amônia suavemente — e comprovando sua origem
Com esse compósito urânio/graphdiyne em mãos, os pesquisadores testam a produção de amônia a partir de nitrogênio e hidrogênio em temperaturas em torno de 150 °C e pressões próximas a 15 bar — muito abaixo das condições típicas do Haber–Bosch. Cromatografia iônica mostra que o catalisador produz muito mais amônia do que os controles em branco e catalisadores convencionais de comparação sob as mesmas condições, alcançando uma das maiores taxas relatadas para operação tão branda. O catalisador também funciona repetidamente ao longo de vários ciclos sem perda significativa de atividade. Para verificar que o nitrogênio no produto realmente se origina do gás fornecido, a equipe realiza experimentos de marcação com nitrogênio‑15 e detecta a assinatura isotópica correspondente no amônio resultante, descartando contaminação ou decomposição de fontes de nitrogênio de fundo.
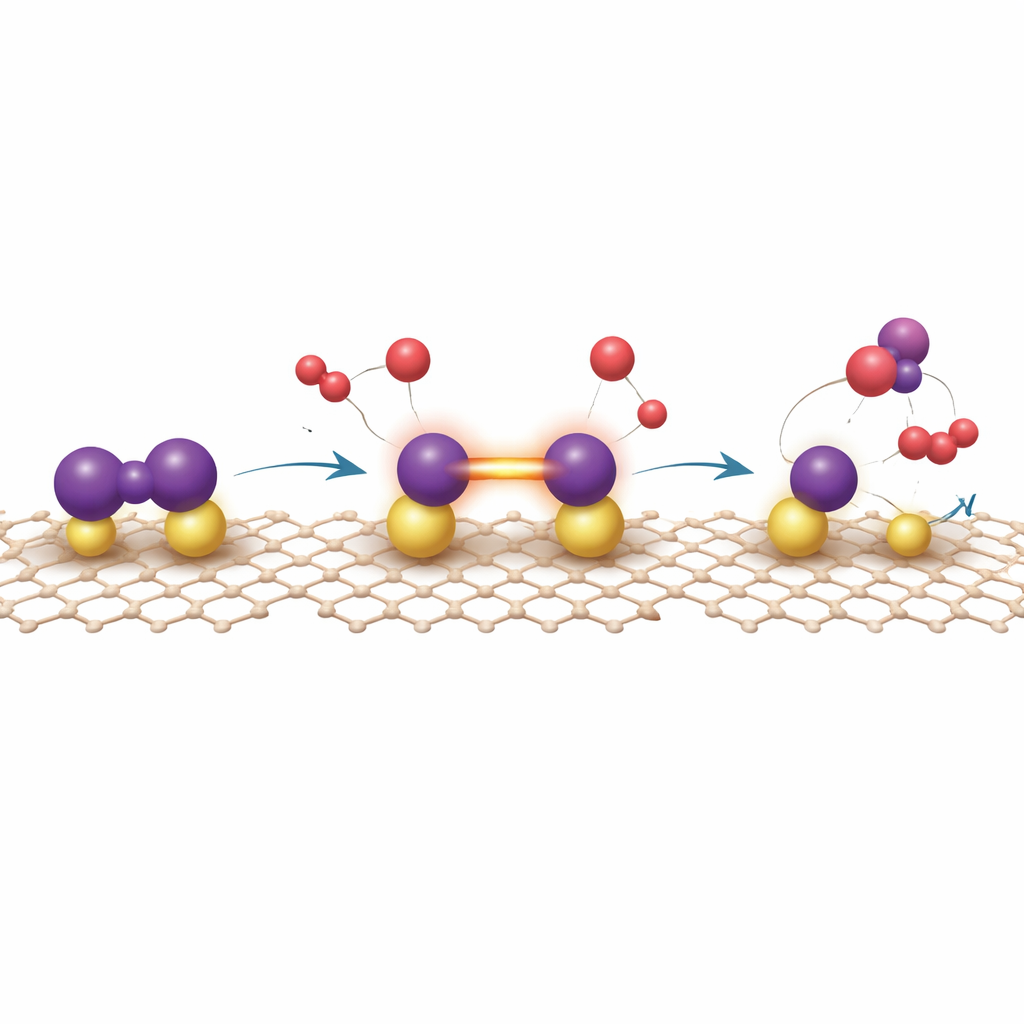
Esmiuçando como o catalisador realmente funciona
Experimentos isoladamente não conseguem revelar por completo como essa superfície incomum rompe a teimosa ligação nitrogênio–nitrogênio. Os autores, portanto, combinam espectroscopias de raios X com cálculos quântico‑mecânicos. A teoria mostra que o nitrogênio prefere se ligar em modo “ponte” entre dois átomos de urânio, fazendo com que sua ligação se alongue e seus orbitais antibonding sejam preenchidos por elétrons doados de retorno pelos estados 5f do urânio, que por sua vez são ajustados pela interação com o graphdiyne. A partir desse estado ativado, átomos de hidrogênio adicionam‑se de forma escalonada a uma extremidade da molécula de nitrogênio — o chamado caminho distal — gerando eventualmente amônia que dessorve relativamente fácil, reiniciando os centros de urânio. Rotas concorrentes em que o nitrogênio se divide completamente em átomos separados acabam prendendo o nitrogênio com força excessiva, tornando a reação subsequente lenta. Cálculos também indicam que o hidrogênio se liga apenas moderadamente ao sítio ativo, explicando por que o catalisador resiste ao “envenenamento” por hidrogênio, um problema comum em catalisadores metálicos convencionais.
O que isso significa para uma química mais limpa
Em conjunto, os resultados mostram que uma parceria cuidadosamente projetada entre urânio e graphdiyne pode conduzir a síntese de amônia de forma eficiente em condições muito mais brandas do que as usadas nas plantas atuais. O andaime de graphdiyne estabiliza o urânio na forma e espaçamento corretos, enquanto seu sistema eletrônico estendido remodela os orbitais 5f do metal para ativar o nitrogênio e guiar a reação por uma rota produtiva e facilmente reversível. Embora esse catalisador específico ainda não esteja pronto para substituir unidades industriais Haber–Bosch, ele demonstra uma ideia de projeto poderosa: átomos de actinídeos ancorados em estruturas de carbono sob medida podem realizar transformações químicas exigentes de maneiras que, um dia, podem ser tanto mais eficientes em energia quanto mais ambientalmente amigáveis.
Citação: Xiong, S., Wang, W., Wang, F. et al. Thermal catalytic synthesis of ammonia using uranium/graphdiyne composite at mild conditions. Nat Commun 17, 2894 (2026). https://doi.org/10.1038/s41467-026-69691-8
Palavras-chave: síntese de amônia, fixação de nitrogênio, catalisador de urânio, graphdiyne, química verde