Clear Sky Science · pl
Termiczno‑katalityczna synteza amoniaku z użyciem kompozytu uran/graphdiyne w łagodnych warunkach
Dlaczego nowa droga do amoniaku ma znaczenie
Amoniak jest cichym gigantem współczesnego życia. Stanowi podstawę produkcji nawozów dla globalnego rolnictwa i pojawia się jako potencjalny nośnik energii. Tymczasem sposób, w jaki obecnie go wytwarzamy — stoletni proces Habera–Boscha — pochłania ogromne ilości paliw kopalnych, pracuje w ekstremalnych temperaturach i przy wysokich ciśnieniach oraz emituje olbrzymie ilości dwutlenku węgla. W badaniu tym badacze proponują radykalnie inną drogę: katalizator zbudowany z atomów uranu osadzonych na ultracienkiej warstwie węgla zwanej graphdiyne, zdolny przekształcać azot i wodór w amoniak w znacznie łagodniejszych warunkach, co daje nadzieję na czystszą przyszłość dla tej istotnej chemikalii.

Budowanie lepszej sceny dla reakcji
Naukowcy zaczynają od graphdiyne, dwuwymiarowego materiału węglowego zbudowanego z pierścieni benzenowych połączonych krótkimi łańcuchami węglowymi. Jego struktura tworzy trójkątne porowatości, dużą powierzchnię właściwą i wbudowaną przerwę energetyczną (bandgap), którą można regulować przez zmianę liczby warstw. Przy użyciu dwutlenku węgla w stanie nadkrytycznym otrzymują niezwykle cienkie arkusze graphdiyne — od pojedynczych warstw po układy wielowarstwowe — a następnie precyzyjnie mierzą ich grubość i właściwości elektroniczne. Stwierdzają, że wraz ze wzrostem liczby warstw przerwa energetyczna maleje w przewidywalny sposób, a pięciowarstwowa wersja oferuje szczególnie korzystne warunki elektroniczne do współpracy z metalami i aktywacji azotu.
Połączenie uranu z autorskim węglem
Aby przekształcić tę warstwę węgla w działający katalizator, zespół wprowadza uran przy użyciu reaktywnego roztworu jodku uranu. Cienkie warstwy graphdiyne ulegają zniszczeniu pod wpływem tego zabiegu, więc badacze zaczynają od ośmiowarstwowego filmu i częściowo go trawią, kończąc na stabilnym pięciowarstwowym szkielecie graphdiyne ozdobionym drobnymi klastrami uranu. Zaawansowana mikroskopia elektronowa pokazuje, że klastry te składają się z zaledwie kilku atomów uranu, regularnie rozmieszczonych w sieci węglowej w odległościach sprzyjających „uchwyceniu” cząsteczki azotu między dwoma sąsiednimi miejscami metalicznymi. Pomiary spektroskopowe potwierdzają, że uran występuje głównie w stanach pośrednich utlenienia, a elektrony przepływają z uranu do graphdiyne, subtelnie przekształcając orbitale 5f metalu, które są znane jako silne, ale trudne do kontrolowania uczestniki wiązań chemicznych.
Łagodne otrzymywanie amoniaku — i udowodnienie jego pochodzenia
Mając w ręku ten kompozyt uran/graphdiyne, badacze testują produkcję amoniaku z azotu i wodoru w temperaturach około 150 °C i przy ciśnieniach bliskich 15 bar — znacznie poniżej typowych warunków Habera–Boscha. Chromatografia jonowa wykazuje, że katalizator wytwarza znacznie więcej amoniaku niż próby kontrolne i konwencjonalne katalizatory porównawcze w tych samych warunkach, osiągając jeden z najwyższych zgłaszanych współczynników dla tak łagodnej operacji. Katalizator działa również powtarzalnie w kilku cyklach bez znaczącej utraty aktywności. Aby zweryfikować, że azot w produkcie rzeczywiście pochodzi z zasilania gazowego, zespół przeprowadza eksperymenty z izotopowym znakowaniem azotem‑15 i wykrywa odpowiadający podpis izotopowy w powstającym amonowym, wykluczając zanieczyszczenie lub rozkład źródeł azotu tła.
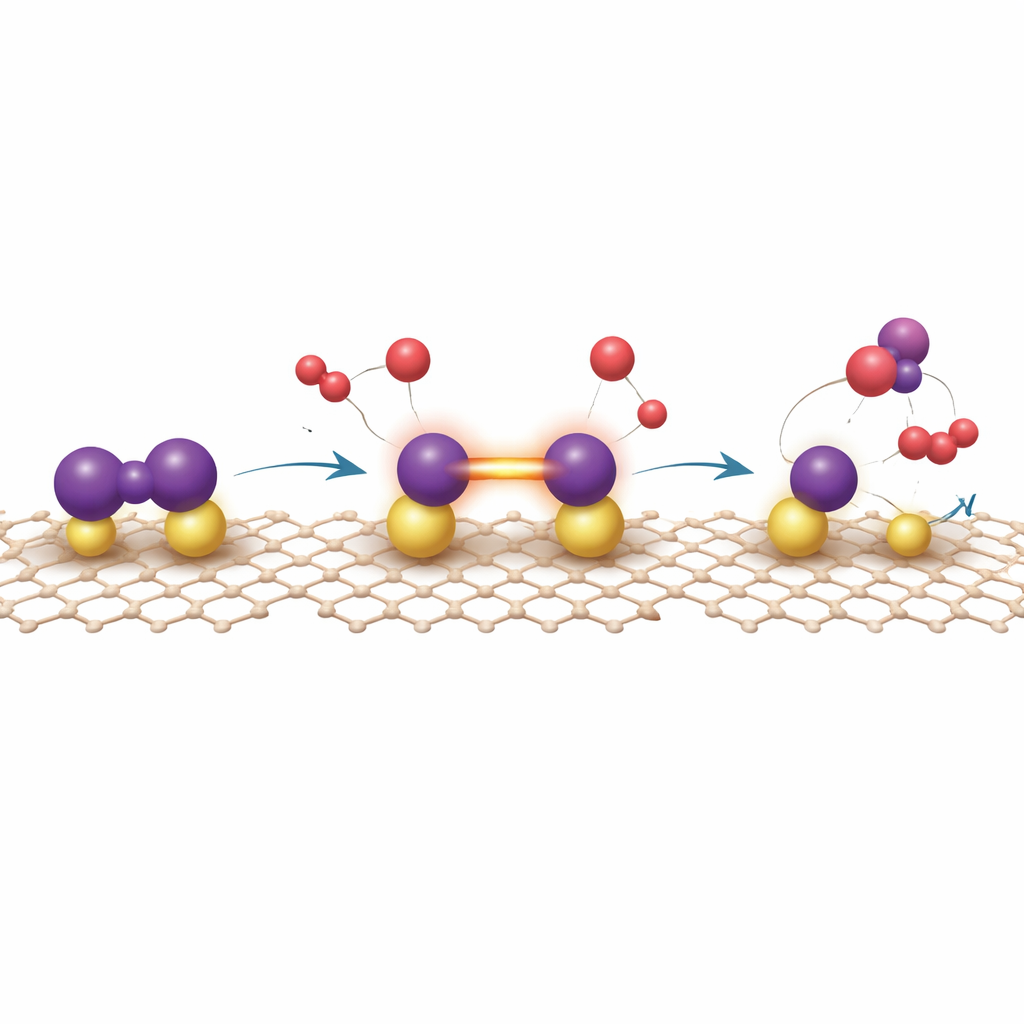
Zajrzeć, jak katalizator rzeczywiście działa
Sama eksperymentacja nie wystarcza, by w pełni ujawnić, jak ta niezwykła powierzchnia rozrywa oporną wiązanie azot–azot. Autorzy łączą więc spektroskopię rentgenowską z obliczeniami kwantowo‑mechanicznymi. Teoria pokazuje, że azot preferuje wiązanie w sposób „mostkowy” między dwoma atomami uranu, co powoduje wydłużenie jego wiązania i napełnienie orbitali antywiążących elektronami zwrotnymi (back‑donation) z orbitali 5f uranu, które same są kształtowane przez interakcję z graphdiyne. Z tak aktywowanego stanu atomy wodoru dodają się stopniowo do jednego końca cząsteczki azotu — tzw. droga distalna — ostatecznie dając amoniak, który dość łatwo odszczepia się, przywracając centra uranowe. Konkurencyjne ścieżki, w których azot całkowicie rozpada się na osobne atomy, okazują się zbyt mocno wiązać azot, spowalniając dalszą reakcję. Obliczenia wskazują również, że wodór wiąże się umiarkowanie do miejsca aktywnego, co wyjaśnia, dlaczego katalizator jest odporny na „zatrucie” przez wodór — typowy problem konwencjonalnych katalizatorów metalicznych.
Co to oznacza dla czystszej chemii
W podsumowaniu, wyniki pokazują, że starannie zaprojektowane partnerstwo między uranem a graphdiyne może napędzać syntezę amoniaku wydajnie w znacznie łagodniejszych warunkach niż te stosowane w dzisiejszych zakładach. Szkielet graphdiyne stabilizuje uran w odpowiedniej formie i odstępie, podczas gdy jego rozległy system elektronowy przekształca orbitale 5f metalu, by aktywować azot i prowadzić reakcję w produktywną, łatwo odwracalną drogą. Chociaż ten konkretny katalizator nie jest jeszcze gotowy, by zastąpić przemysłowe jednostki Habera–Boscha, demonstruje potężny pomysł projektowy: atomy aktynowców osadzone na dopasowanych ramach węglowych mogą przeprowadzać wymagające przekształcenia chemiczne w sposób, który kiedyś może okazać się bardziej energooszczędny i przyjaźniejszy dla środowiska.
Cytowanie: Xiong, S., Wang, W., Wang, F. et al. Thermal catalytic synthesis of ammonia using uranium/graphdiyne composite at mild conditions. Nat Commun 17, 2894 (2026). https://doi.org/10.1038/s41467-026-69691-8
Słowa kluczowe: synteza amoniaku, wiązanie azotu, katalizator uranowy, graphdiyne, zielona chemia