Clear Sky Science · de
Thermisch-katalytische Synthese von Ammoniak mit Uran/Graphdiyin‑Verbund unter milden Bedingungen
Warum ein neuer Weg zur Ammoniakproduktion wichtig ist
Ammoniak ist ein stiller Gigant des modernen Lebens. Es bildet die Grundlage der Düngerproduktion für die weltweite Landwirtschaft und wird zunehmend als möglicher Energieträger diskutiert. Doch die derzeit übliche Herstellung — das über ein Jahrhundert alte Haber‑Bosch‑Verfahren — verbraucht enorme Mengen fossiler Brennstoffe, läuft bei sehr hohen Temperaturen und Drücken und verursacht große CO2‑Emissionen. Diese Studie untersucht einen grundlegend anderen Ansatz: einen Katalysator aus Uranatomen, die auf einem ultradünnen Kohlenstoffblatt namens Graphdiyin verankert sind und in der Lage sind, unter deutlich milderen Bedingungen Stickstoff und Wasserstoff zu Ammoniak zu verbinden. Das deutet auf eine sauberere Zukunft für dieses unverzichtbare Chemikalie hin.

Eine bessere Bühne für die Reaktion schaffen
Die Forscher beginnen mit Graphdiyin, einem zweidimensionalen Kohlenstoffmaterial aus Benzolringen, die durch kurze Kohlenstoffketten verbunden sind. Seine Struktur erzeugt dreieckige Poren, eine große Oberfläche und eine eingebaute elektronische Bandlücke, die durch Variation der Schichtanzahl einstellbar ist. Mithilfe überkritischen Kohlendioxids züchten sie extrem dünne Graphdiyin‑Schichten von Einzel‑ bis Mehrfachlagen und bestimmen anschließend genau deren Dicke und elektronische Eigenschaften. Sie finden, dass die Bandlücke mit zunehmender Schichtzahl auf vorhersagbare Weise schrumpft und dass eine fünf‑lagige Variante eine besonders günstige elektronische Umgebung für Wechselwirkungen mit Metallen und die Aktivierung von Stickstoff bietet.
Uran mit maßgeschneidertem Kohlenstoff paaren
Um dieses Kohlenstoffblatt in einen funktionierenden Katalysator zu verwandeln, führt das Team Uran mittels einer reaktiven Uraniodidlösung ein. Dünne Graphdiyin‑Schichten werden durch diese Behandlung zerstört, daher beginnen sie mit einem acht‑lagigen Film und ätzen ihn partiell herunter, sodass ein stabiles fünf‑lagiges Graphdiyin‑Gerüst mit winzigen Uranclustern entsteht. Fortgeschrittene Elektronenmikroskopie zeigt, dass diese Cluster nur aus wenigen Uranatomen bestehen, regelmäßig auf dem Kohlenstoffgitter verteilt und in Abständen angeordnet sind, die geeignet sind, ein Stickstoffmolekül zwischen zwei benachbarten Metallstellen „einzufangen“. Spektroskopische Messungen bestätigen, dass Uran vorwiegend in intermediären Oxidationszuständen vorliegt und dass Elektronen vom Uran in das Graphdiyin fließen, wodurch die 5f‑Orbitale des Metalls subtil umgestaltet werden — jene Orbitale, die starke, aber schwer zu kontrollierende Beiträge zur chemischen Bindung leisten können.
Ammoniak schonend herstellen — und nachweisen, woher es stammt
Mit diesem Uran/Graphdiyin‑Verbund testen die Forscher die Ammoniakproduktion aus Stickstoff und Wasserstoff bei Temperaturen um 150 °C und Drücken nahe 15 bar — weit unter den typischen Haber‑Bosch‑Bedingungen. Ionenchromatographie zeigt, dass der Katalysator unter denselben Bedingungen deutlich mehr Ammoniak produziert als Kontrollen ohne Katalysator und konventionelle Vergleichskatalysatoren und erreicht damit eine der höchsten berichteten Raten für so milde Bedingungen. Der Katalysator arbeitet außerdem über mehrere Zyklen wiederholt ohne nennenswerten Aktivitätsverlust. Um zu verifizieren, dass der Stickstoff im Produkt tatsächlich aus der Gaszufuhr stammt, führen die Forscher Markierungsexperimente mit Stickstoff‑15 durch und detektieren die entsprechende isotopische Signatur im resultierenden Ammonium, womit Verunreinigungen oder die Zersetzung von Hintergrund‑Stickstoffquellen ausgeschlossen werden.
Einen Blick darauf werfen, wie der Katalysator tatsächlich wirkt
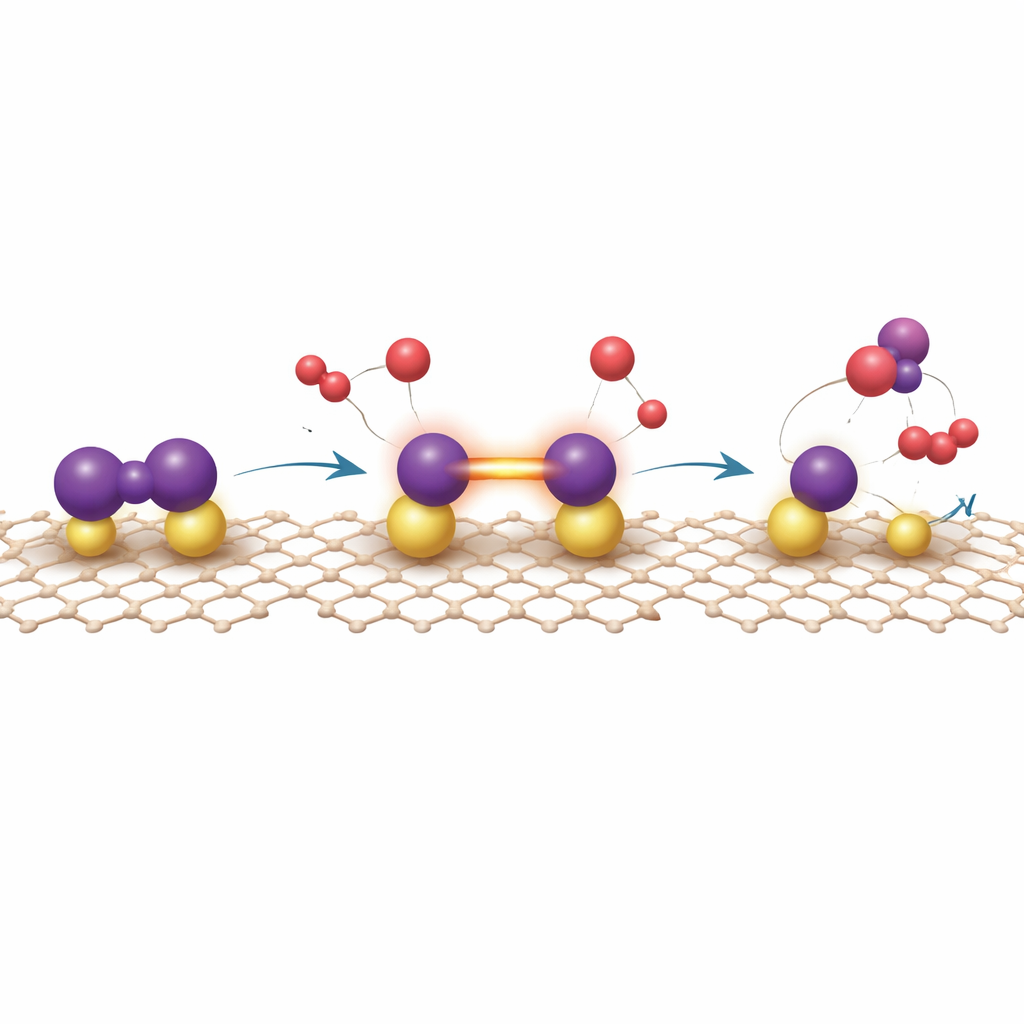
Alleinige Experimente können nicht vollständig enthüllen, wie diese ungewöhnliche Oberfläche die robuste Stickstoff‑Stickstoff‑Bindung bricht. Die Autoren kombinieren deshalb Röntgenspektroskopien mit quantenmechanischen Berechnungen. Die Theorie zeigt, dass Stickstoff bevorzugt in einer „Brücken“‑Bindung zwischen zwei Uranatomen adsorbiert, wodurch seine Bindung gedehnt wird und seine antibindenden Orbitale durch Rückspende von Elektronen aus den 5f‑Zuständen des Urans gefüllt werden — diese Zustände werden wiederum durch die Wechselwirkung mit Graphdiyin abgestimmt. Aus diesem aktivierten Zustand fügen sich Wasserstoffatome schrittweise an ein Ende des Stickstoffmoleküls an — ein sogenannter distaler Pfad — und führen schließlich zu Ammoniak, das sich relativ leicht desorbiert und die Uranzentren wieder freisetzt. Konkurrenzwege, bei denen Stickstoff vollständig in einzelne Atome gespalten wird, binden diesen zu stark und hemmen weitere Reaktionen. Rechnungen zeigen außerdem, dass Wasserstoff nur moderat an der aktiven Stelle bindet, was erklärt, warum der Katalysator gegenüber einer Wasserstoff„vergiftung“, einem häufigen Problem konventioneller Metallkatalysatoren, resistent ist.
Was das für sauberere Chemie bedeutet
In der Summe zeigen die Ergebnisse, dass eine sorgfältig gestaltete Partnerschaft zwischen Uran und Graphdiyin die Ammoniaksynthese bei deutlich milderen Bedingungen effizient antreiben kann als die Anlagen von heute. Das Graphdiyin‑Gerüst stabilisiert Uran in genau der richtigen Form und Anordnung, während sein ausgedehntes Elektronensystem die 5f‑Orbitale des Metalls so umformt, dass Stickstoff aktiviert und der Reaktionsweg in eine produktive, leicht umkehrbare Richtung gelenkt wird. Zwar ist dieser spezifische Katalysator noch nicht bereit, industrielle Haber‑Bosch‑Anlagen zu ersetzen, doch er demonstriert eine potente Gestaltungsidee: Aktinoiden‑Atome, verankert auf maßgeschneiderten Kohlenstoffgerüsten, können anspruchsvolle chemische Umsetzungen auf eine Weise durchführen, die eines Tages sowohl energieeffizienter als auch umweltfreundlicher sein könnte.
Zitation: Xiong, S., Wang, W., Wang, F. et al. Thermal catalytic synthesis of ammonia using uranium/graphdiyne composite at mild conditions. Nat Commun 17, 2894 (2026). https://doi.org/10.1038/s41467-026-69691-8
Schlüsselwörter: Ammoniaksynthese, Stickstofffixierung, Uran‑Katalysator, Graphdiyin, grüne Chemie