Clear Sky Science · pt
Um kit genético para a bactéria intestinal humana Mediterraneibacter gnavus identifica polissacarídeos capsulares como um fator competitivo de colonização
Por que o “revestimento” de um microbio intestinal importa
Nossos intestinos abrigam trilhões de microrganismos que podem nos ajudar ou nos prejudicar. Um residente comum, a bactéria Mediterraneibacter gnavus, costuma aparecer em números maiores em pessoas com doenças inflamatórias intestinais, como a doença de Crohn. Ainda assim, nem todas as linhagens dessa espécie se comportam da mesma forma. Este estudo faz uma pergunta simples, porém importante: quais genes tornam algumas linhagens de M. gnavus melhores em viver no intestino, e como isso afeta a inflamação?
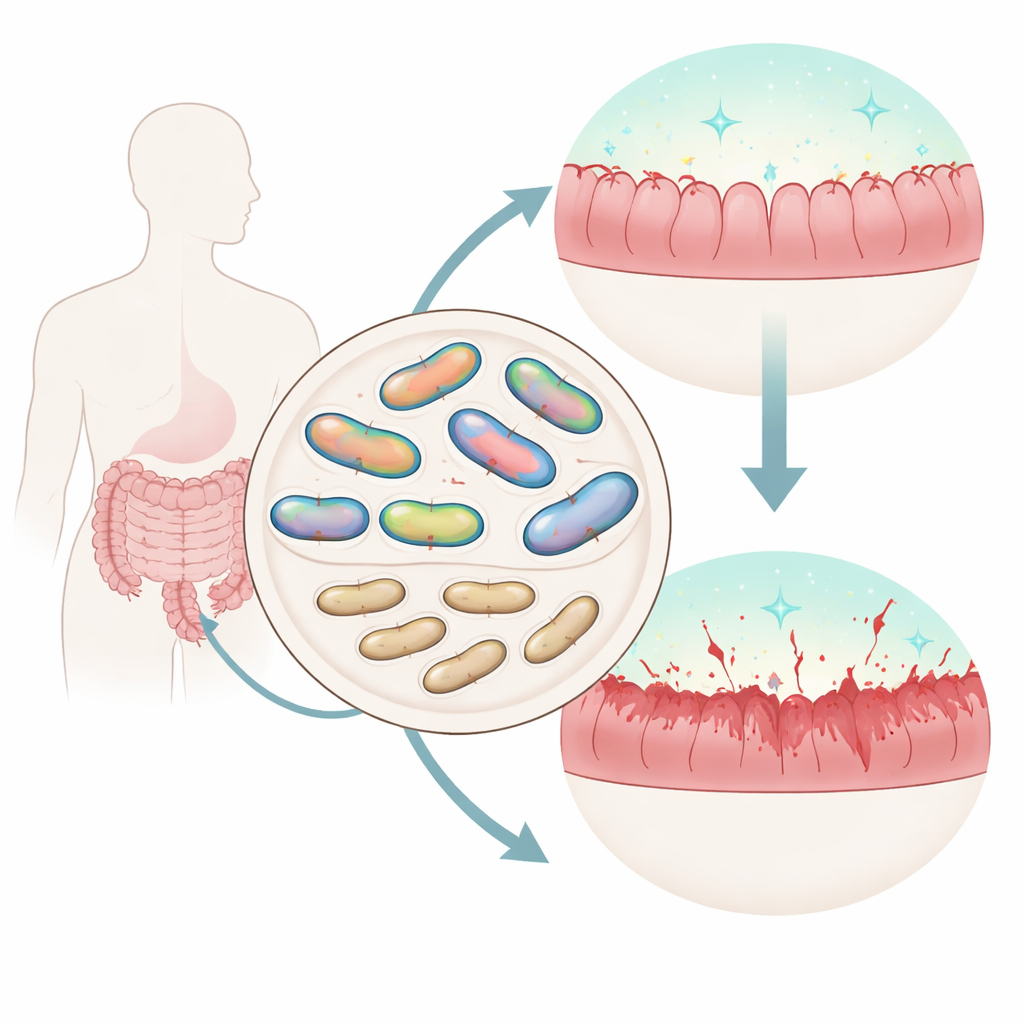
Construindo uma caixa de ferramentas para editar um micróbio teimoso
Muitas bactérias intestinais são difíceis de manipular geneticamente, o que retardou os esforços para entender a função de genes individuais. Os pesquisadores primeiro solucionaram esse obstáculo técnico para M. gnavus. Eles criaram plasmídeos shuttle que podem mover DNA entre E. coli e M. gnavus, junto com interruptores para ativar genes apenas quando necessário e um conjunto de marcadores fluorescentes brilhantes para rastrear células bacterianas. Também adaptaram dois sistemas para alterar permanentemente o genoma: um método de inserção de DNA móvel e uma abordagem baseada em CRISPR/Cas9. Juntos, essas ferramentas permitiram deletar ou interromper genes específicos, marcar linhagens com cor e verificar os efeitos tanto em placas de laboratório quanto em camundongos.
Localizando genes que moldam a superfície bacteriana
Munidos desse kit, a equipe concentrou-se em genes chamados sortases, que atuam como grampeadores moleculares que prendem proteínas e açúcares à parede celular bacteriana. M. gnavus carrega oito genes de sortase previstos. Ao inativar a maioria deles um a um, os cientistas mostraram que uma enzima, SrtB3, é essencial para fixar proteínas altamente ativadoras do sistema imune — chamadas superantígenos — à superfície celular. Quando SrtB3 foi perdido, essas proteínas não eram mais ancoradas; em vez disso, vazavam para o meio circundante, e a ligação de anticorpos à superfície celular caiu acentuadamente. Isso confirmou que tipos individuais de sortase se especializam em lidar com conjuntos distintos de moléculas de superfície.
Uma cápsula açucarada que aumenta a colonização intestinal
As descobertas mais marcantes centraram-se em outra sortase, SrtB4. Ao microscópio, células normais de M. gnavus parecem rodeadas por um “halo” pálido: uma cápsula feita de açúcares complexos que forma um revestimento macio ao redor de cada bactéria. Quando o gene srtB4 foi desativado, esse halo desapareceu. Colorações químicas e microscopia eletrônica confirmaram uma perda significativa do polissacarídeo capsular, e as células aglomeraram-se fortemente em vez de formar pelletes soltos. Examinando os genes vizinhos a srtB4 no cromossomo, os pesquisadores descobriram um cluster de genes previsto para construir e anexar essa cápsula. A desativação de vários desses genes vizinhos produziu o mesmo aspecto sem cápsula, vinculando todo o cluster à fabricação da cápsula.
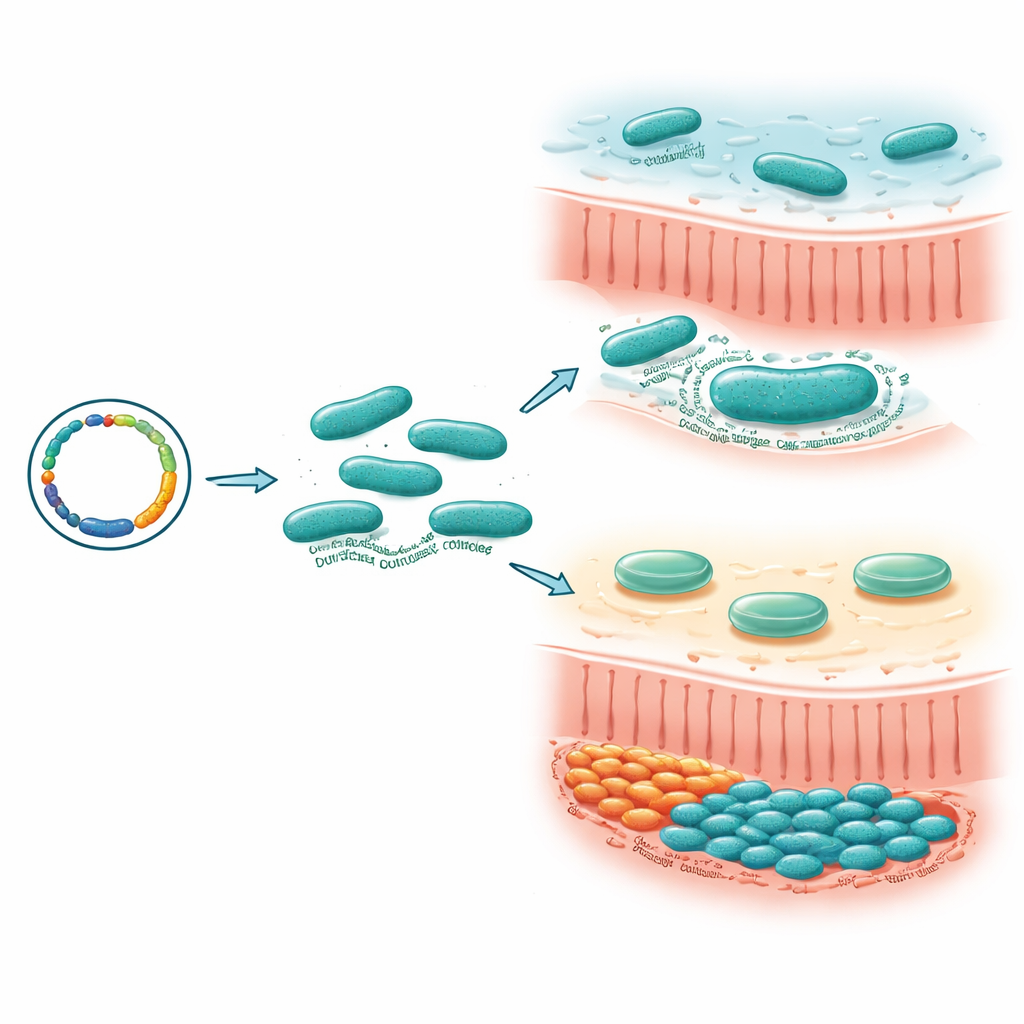
Da competição no intestino de camundongos à inflamação
Para testar por que a cápsula importa, a equipe colocou linhagens normais e mutantes em competição dentro de camundongos isentos de germes. Quando linhagens deficientes em cápsula foram misturadas com suas contrapartes encapsuladas e administradas aos animais, os mutantes perderam rapidamente terreno e quase desapareceram do intestino, mesmo crescendo bem em cultura laboratorial. Isso mostrou que a cápsula dá a M. gnavus uma vantagem competitiva acentuada durante a colonização intestinal real. Mas a história não terminou na colonização. Em cultura de células, as linhagens sem cápsula desencadearam níveis muito mais altos de sinais inflamatórios por células imunes de camundongo do que a linhagem encapsulada. Em um modelo de colite quimicamente induzida em camundongos, os animais colonizados com o mutante deficiente em cápsula sofreram maior perda de peso e pontuações de doença mais severas, embora o número total de bactérias fosse semelhante.
Ligação com doenças humanas e o que isso pode significar
Finalmente, os autores compararam muitos genomas completos de linhagens de M. gnavus isoladas de pessoas. Eles descobriram que o cluster de genes relacionado à cápsula que contém srtB4 estava presente muito mais frequentemente em linhagens de indivíduos saudáveis do que em linhagens de pacientes com doença de Crohn. Outras linhagens que careciam desse cluster também não produziram uma cápsula visível em laboratório. Embora sejam necessárias mais amostragens, esse padrão sugere que linhagens portadoras de cápsula podem ser residentes de longo prazo melhores e provocar menos inflamação, enquanto linhagens “nuas”, sem a cápsula, podem ser mais danosas ao revestimento intestinal.
Mensagem principal para a saúde intestinal
Este trabalho mostra que um único trecho de genes que controla um revestimento externo açucarado pode decidir se M. gnavus vence a batalha pela colonização do intestino e quão fortemente ele provoca inflamação. A nova caixa de ferramentas genética agora torna possível dissecar muitas outras características desse micróbio e de seus parentes. Para não especialistas, a ideia-chave é que nem todos os membros de uma espécie bacteriana são iguais: diferenças genéticas sutis em estruturas de superfície, como cápsulas, podem inclinar a balança entre um companheiro benéfico e um desencadeador nocivo de doença.
Citação: Obana, N., Nakato, G., Nomura, N. et al. A genetic toolkit for the human gut bacterium Mediterraneibacter gnavus identifies capsular polysaccharides as a competitive colonization factor. Nat Commun 17, 3855 (2026). https://doi.org/10.1038/s41467-026-69022-x
Palavras-chave: microbioma intestinal, Mediterraneibacter gnavus, cápsula bacteriana, doença inflamatória intestinal, genética CRISPR