Clear Sky Science · de
Ein genetisches Werkzeugset für das menschliche Darmbakterium Mediterraneibacter gnavus identifiziert kapsuläre Polysaccharide als Faktor für konkurrenzfähige Kolonisierung
Warum die „Hülle" eines Darmmikrobe wichtig ist
In unserem Darm leben Billionen von Mikroben, die uns nützen oder schaden können. Ein häufiger Bewohner, das Bakterium Mediterraneibacter gnavus, kommt bei Menschen mit entzündlichen Darmerkrankungen wie Morbus Crohn oft vermehrt vor. Aber nicht alle Stämme dieser Art verhalten sich gleich. Die Studie stellt eine einfache, aber wichtige Frage: Welche Gene machen einige M. gnavus-Stämme besser geeignet zum Leben im Darm, und wie beeinflusst das Entzündungen?
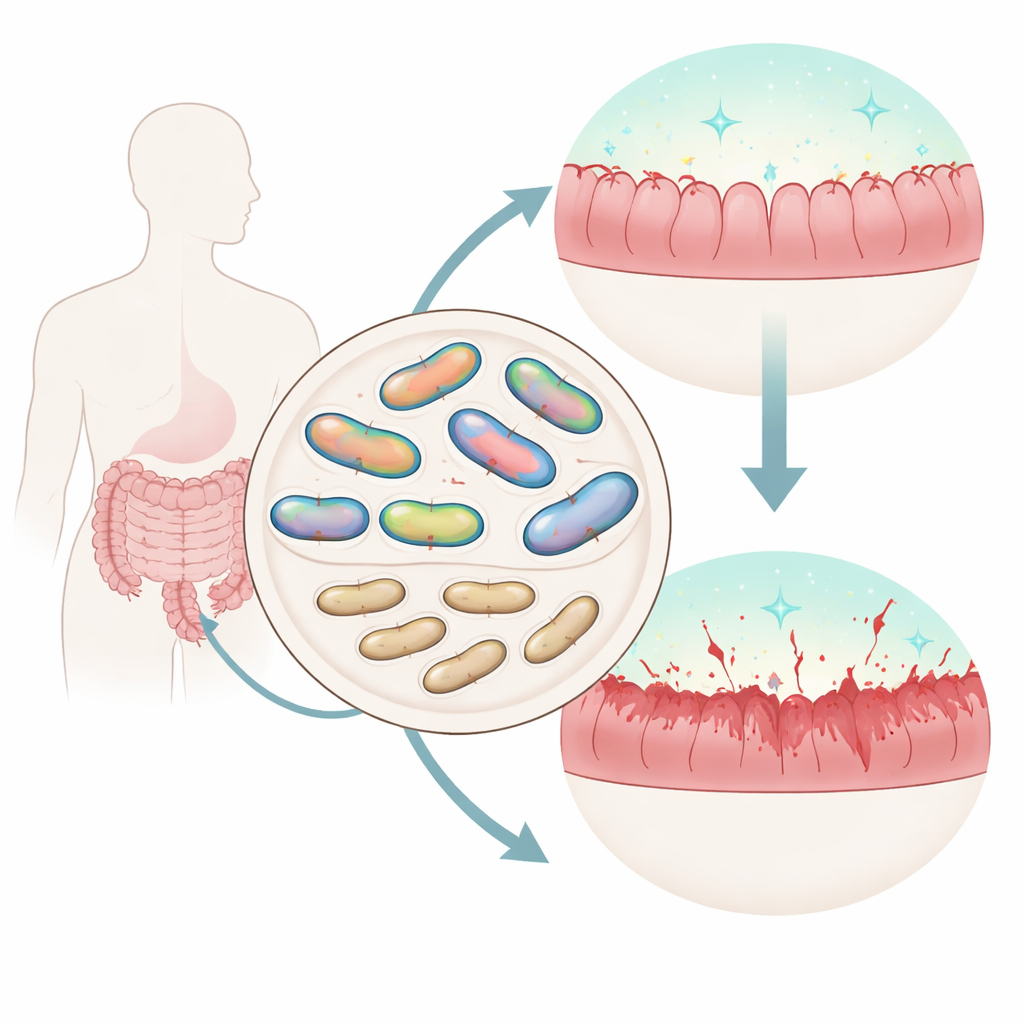
Ein Werkzeugkasten, um ein störrisches Mikroben zu editieren
Viele Darmbakterien sind genetisch schwer zu bearbeiten, was die Aufklärung der Funktionen einzelner Gene erschwert hat. Die Forschenden beseitigten zunächst dieses technische Hindernis für M. gnavus. Sie entwickelten Shuttle-Plasmide, die DNA zwischen E. coli und M. gnavus hin- und her transportieren können, zusammen mit Schaltern, um Gene nur bei Bedarf einzuschalten, und einer Reihe heller Fluoreszenzmarker zur Verfolgung einzelner Zellen. Außerdem passten sie zwei Systeme an, um das Genom dauerhaft zu verändern: eine Methode zur mobilen DNA-Einfügung und einen CRISPR/Cas9-basierten Ansatz. Zusammen ermöglichten diese Werkzeuge das gezielte Löschen oder Stören spezieller Gene, das Färben von Stämmen und das Überprüfen der Effekte sowohl im Labor als auch in Mäusen.
Gene ausmachen, die die Bakterienoberfläche formen
Mit diesem Werkzeugkasten konzentrierte sich das Team auf Gene, die Sortasen genannt werden — molekulare „Heftgeräte“, die Proteine und Zucker an die bakterielle Zellwand anheften. M. gnavus trägt acht vorhergesagte Sortase-Gene. Durch das nacheinander Entfernen der meisten dieser Gene zeigten die Forschenden, dass ein Enzym, SrtB3, essentiell ist, um stark immunaktivierende Proteine — sogenannte Superantigene — an der Zelloberfläche zu befestigen. Fehlt SrtB3, sind diese Proteine nicht mehr verankert; stattdessen treten sie in das umgebende Medium aus, und die Antikörperbindung an der Zelloberfläche fällt deutlich ab. Das bestätigt, dass einzelne Sortasetypen spezialisiert sind auf verschiedene Mengen von Oberflächenmolekülen.
Eine zuckerreiche Kapsel, die die Darmkolonisierung stärkt
Die auffälligsten Befunde drehten sich um eine andere Sortase, SrtB4. Unter dem Mikroskop erscheinen normale M. gnavus-Zellen von einem blassen „Halo“ umgeben: einer Kapsel aus komplexen Zuckern, die jede Bakterienzelle wie einen weichen Mantel umgibt. Wenn das srtB4-Gen ausgeschaltet wurde, verschwand dieses Halo. Chemische Färbungen und Elektronenmikroskopie bestätigten einen deutlichen Verlust kapsulärer Polysaccharide, und die Zellen verklumpten stark statt lockere Pellets zu bilden. In unmittelbarer Nähe von srtB4 auf dem Chromosom entdeckten die Forschenden einen Gencluster, der vermutlich den Bau und die Anheftung dieser Kapsel ermöglicht. Das Stören mehrerer dieser Nachbar-Gene erzeugte denselben kapselarmen Phänotyp und verband den gesamten Cluster mit der Kapselbiosynthese.
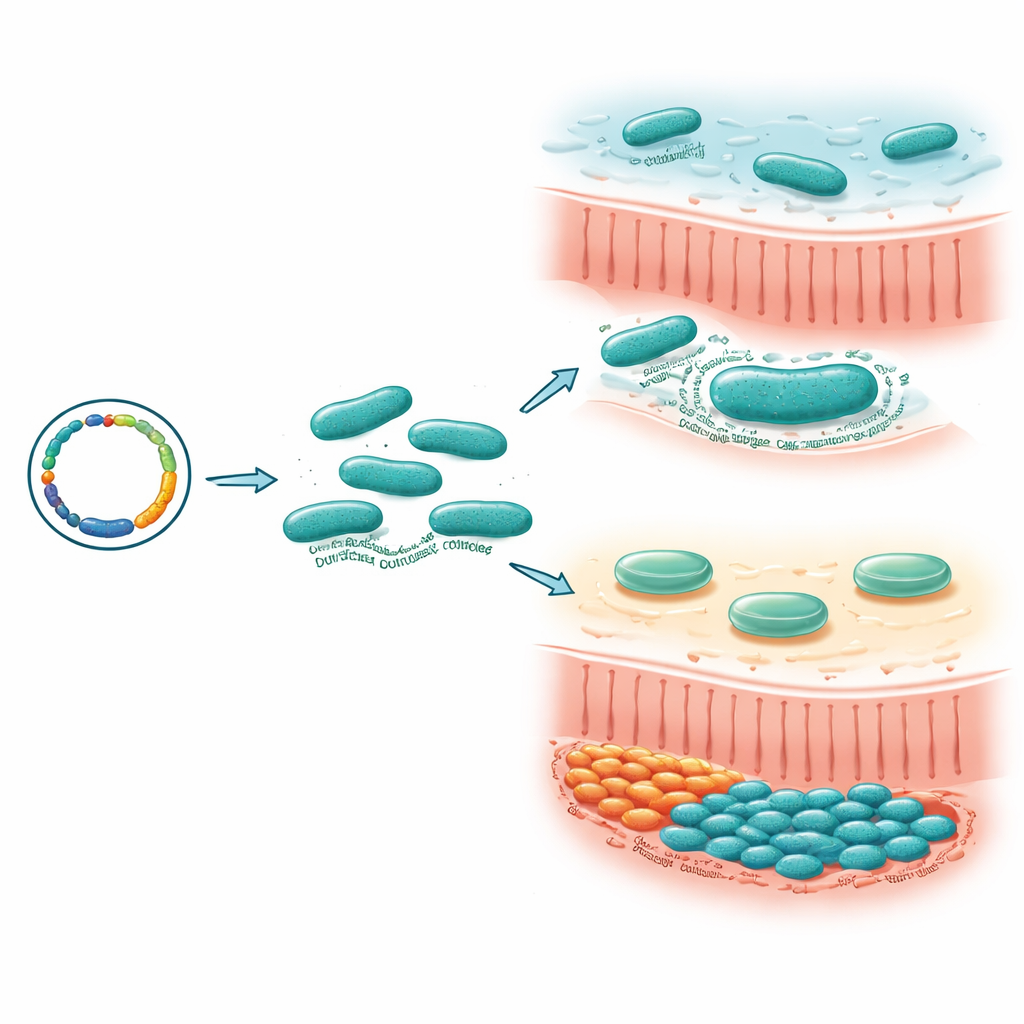
Von Konkurrenz im Mausdarm bis zur Entzündung
Um zu testen, warum die Kapsel wichtig ist, setzten die Forschenden normale und mutierte Stämme in keimfreien Mäusen gegeneinander ein. Wenn kapseldefiziente Stämme zusammen mit ihren kapseltragenden Gegenstücken gefüttert wurden, verloren die Mutanten schnell an Boden und verschwanden nahezu aus dem Darm, obwohl sie im Labormedium gut wuchsen. Das zeigte, dass die Kapsel M. gnavus einen deutlichen Wettbewerbsvorteil bei der tatsächlichen Darmkolonisierung verschafft. Die Geschichte endete aber nicht bei der Kolonisierung: In Zellkultur lösten kapsellose Stämme deutlich höhere entzündliche Signale von Maus-Immunzellen aus als der kapseltragende Stamm. In einem Mausmodell chemisch induzierter Kolitis erlitten Tiere, die mit dem kapseldefizienten Mutanten kolonisiert waren, stärkeren Gewichtsverlust und höhere Krankheitswerte, obwohl die Gesamtbakterienzahlen ähnlich waren.
Bezüge zur menschlichen Krankheit und mögliche Bedeutung
Zum Schluss verglichen die Autorinnen und Autoren viele vollständige Genome von M. gnavus-Stämmen, die aus Menschen isoliert wurden. Sie fanden, dass der kapselbezogene Gencluster mit srtB4 deutlich häufiger in Stämmen aus gesunden Individuen vorkam als in Stämmen von Morbus-Crohn-Patienten. Andere Stämme, denen dieser Cluster fehlte, bildeten im Labor ebenfalls keine sichtbare Kapsel. Zwar sind weitere Proben nötig, doch dieses Muster legt nahe, dass kapseltragende Stämme möglicherweise bessere Langzeitbewohner sind und weniger Entzündungen verursachen, während „nackte" Stämme ohne Kapsel dem Darm eher schaden könnten.
Fazit für die Darmgesundheit
Die Arbeit zeigt, dass ein einzelner Genabschnitt, der einen zuckerhaltigen Außenmantel steuert, darüber entscheiden kann, ob M. gnavus die Kolonisierung des Darms gewinnt und wie stark es Entzündungen auslöst. Das neue genetische Werkzeugset ermöglicht nun, viele weitere Merkmale dieses Mikroben und seiner Verwandten zu untersuchen. Für Nichtfachleute ist die Kernaussage: Nicht alle Mitglieder einer Bakterienart sind gleich — feine genetische Unterschiede in Oberflächenstrukturen wie Kapseln können darüber entscheiden, ob ein Keim ein nützlicher Begleiter oder ein krankheitsauslösender Faktor ist.
Zitation: Obana, N., Nakato, G., Nomura, N. et al. A genetic toolkit for the human gut bacterium Mediterraneibacter gnavus identifies capsular polysaccharides as a competitive colonization factor. Nat Commun 17, 3855 (2026). https://doi.org/10.1038/s41467-026-69022-x
Schlüsselwörter: Darmmikrobiom, Mediterraneibacter gnavus, bakterielle Kapsel, entzündliche Darmkrankheit, CRISPR-Genetik