Clear Sky Science · it
Un kit genetico per il batterio intestinale umano Mediterraneibacter gnavus identifica i polisaccaridi capsulari come fattore competitivo di colonizzazione
Perché il “mantello” di un microbo intestinale conta
I nostri intestini ospitano trilioni di microrganismi che possono aiutarci o nuocerci. Un residente comune, il batterio Mediterraneibacter gnavus, si trova spesso in numero maggiore nelle persone con malattie infiammatorie intestinali come il morbo di Crohn. Tuttavia non tutti i ceppi di questa specie si comportano allo stesso modo. Questo studio pone una domanda semplice ma importante: quali geni rendono alcuni ceppi di M. gnavus più adatti a vivere nell’intestino e come ciò influisce sull’infiammazione?
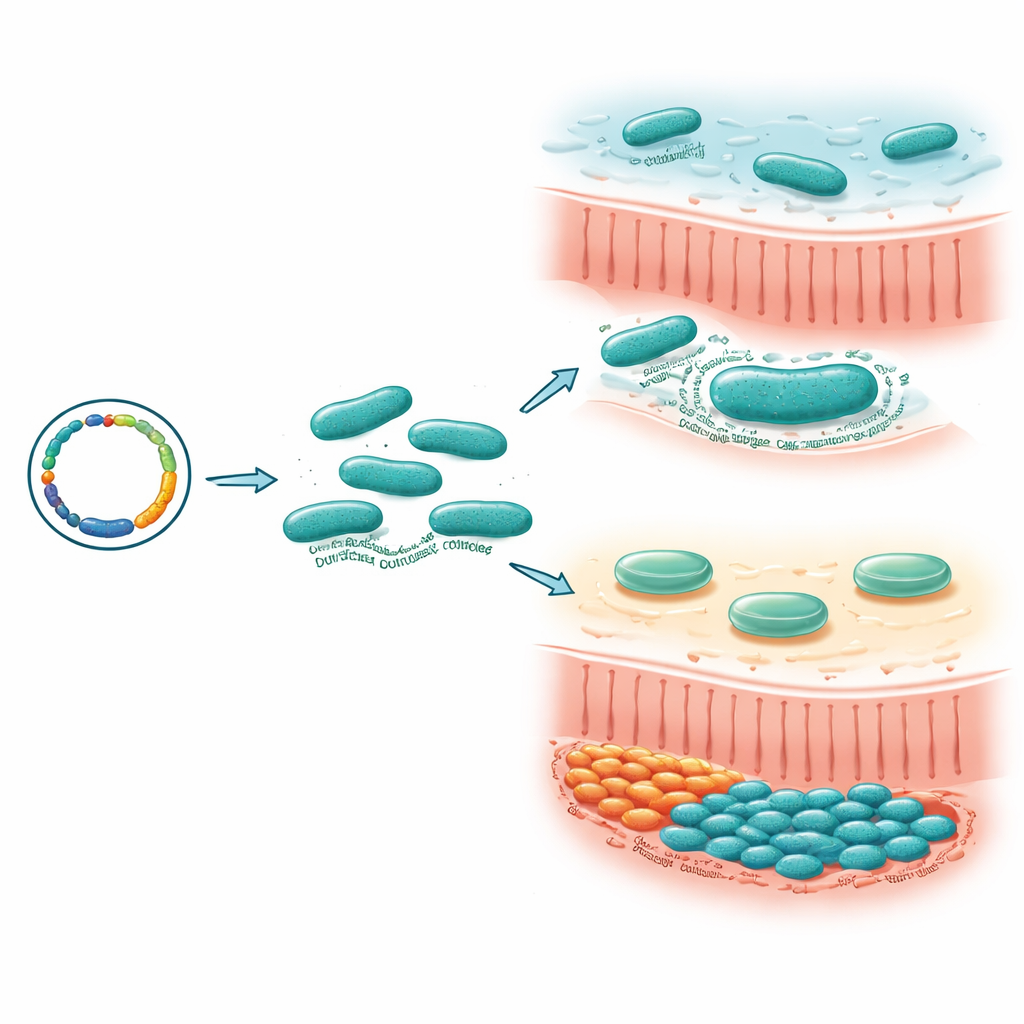
Costruire una cassetta degli attrezzi per modificare un microbo ostinato
Molti batteri intestinali sono difficili da manipolare geneticamente, il che ha rallentato gli sforzi per capire la funzione dei singoli geni. I ricercatori hanno prima risolto questo ostacolo tecnico per M. gnavus. Hanno creato plasmidi shuttle in grado di trasferire DNA avanti e indietro tra E. coli e M. gnavus, insieme a interruttori per attivare i geni solo quando necessario e un set di marcatori fluorescenti brillanti per tracciare le cellule batteriche. Hanno inoltre adattato due sistemi per modifiche genomiche permanenti: un metodo di inserimento di DNA mobile e un approccio basato su CRISPR/Cas9. Insieme, questi strumenti hanno permesso di eliminare o interrompere geni specifici, marcare ceppi con colori e verificare gli effetti sia in piastre di laboratorio sia nei topi.
Individuare i geni che plasmano la superficie batterica
Con questo kit, il team si è concentrato su geni chiamati sortasi, che agiscono come graffatrici molecolari che fissano proteine e zuccheri alla parete cellulare batterica. M. gnavus possiede otto sortasi previste. Disattivando la maggior parte di esse una per una, gli scienziati hanno dimostrato che un enzima, SrtB3, è essenziale per ancorare all’esterno potenti proteine attivanti del sistema immunitario—chiamate superantigeni. Quando SrtB3 veniva perso, queste proteine non erano più ancorate; invece fuoriuscivano nel mezzo circostante e il legame degli anticorpi sulla superficie cellulare precipitava. Ciò ha confermato che tipi diversi di sortasi si specializzano nella gestione di insiemi distinti di molecole di superficie.
Una capsula zuccherina che migliora la colonizzazione intestinale
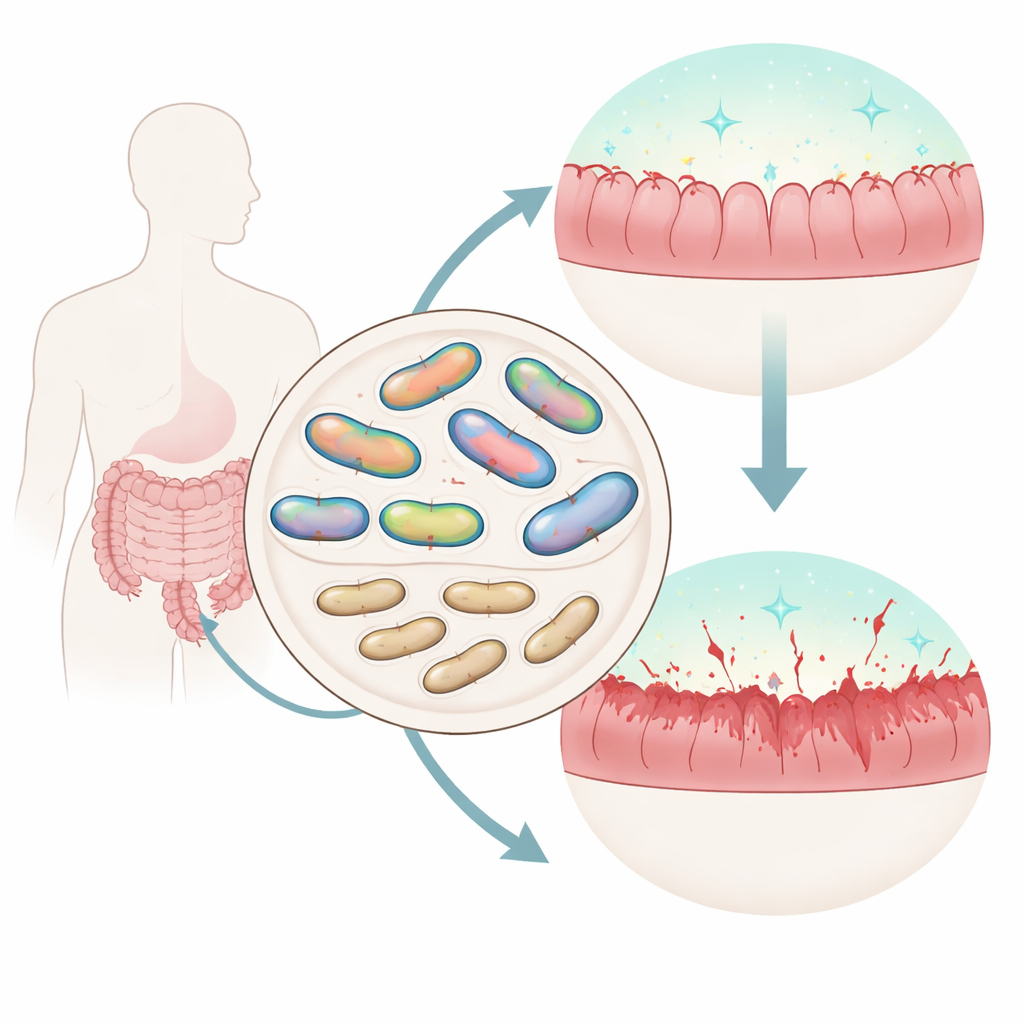
I risultati più sorprendenti si sono concentrati su un’altra sortasi, SrtB4. Al microscopio, le cellule normali di M. gnavus appaiono circondate da un tenue “alone”: una capsula fatta di zuccheri complessi che forma un rivestimento soffice attorno a ogni batterio. Quando il gene srtB4 è stato disattivato, questo alone è scomparso. Colorazioni chimiche e microscopia elettronica hanno confermato una perdita importante di polisaccaride capsulare, e le cellule tendevano ad aggregarsi strettamente anziché formare pellet sciolti. Esaminando i geni vicini a srtB4 sul cromosoma, i ricercatori hanno scoperto un gruppo di geni previsti per costruire e fissare questa capsula. L’interruzione di più di questi geni adiacenti ha prodotto lo stesso fenotipo privo di capsula, collegando l’intero cluster alla produzione della capsula.
Dalla competizione nel tubo digerente del topo all’infiammazione
Per testare perché la capsula sia importante, il team ha messo a confronto ceppi normali e mutanti all’interno di topi gnotobiotici. Quando ceppi privi di capsula sono stati miscelati con i loro equivalenti capsulati e somministrati agli animali, i mutanti hanno rapidamente perso terreno e sono quasi scomparsi dall’intestino, nonostante crescessero perfettamente in coltura di laboratorio. Ciò ha dimostrato che la capsula conferisce a M. gnavus un netto vantaggio competitivo durante la colonizzazione intestinale reale. Ma la storia non finisce con la colonizzazione. In colture cellulari, i ceppi senza capsula hanno indotto livelli molto più elevati di segnali infiammatori dalle cellule immunitarie murine rispetto al ceppo capsulato. In un modello murino di colite indotta chimicamente, gli animali colonizzati con il mutante privo di capsula hanno subito una perdita di peso maggiore e punteggi di malattia più severi, pur avendo numeri batterici complessivi simili.
Collegamenti con le malattie umane e possibili implicazioni
Infine, gli autori hanno confrontato molteplici genomi completi di ceppi di M. gnavus isolati da persone. Hanno scoperto che il cluster di geni legato alla capsula contenente srtB4 era presente molto più spesso nei ceppi provenienti da individui sani rispetto ai ceppi isolati da pazienti con morbo di Crohn. Altri ceppi privi di questo cluster non riuscivano anch’essi a produrre una capsula visibile in laboratorio. Sebbene siano necessari campionamenti più estesi, questo pattern suggerisce che i ceppi portatori di capsula potrebbero essere residenti a lungo termine più tollerati e provocare meno infiammazione, mentre i ceppi “nudi” senza capsula potrebbero arrecare maggior danno alla mucosa intestinale.
Messaggio chiave per la salute intestinale
Questo lavoro mostra che un singolo tratto genetico che controlla un rivestimento zuccherino esterno può determinare se M. gnavus prevale nella colonizzazione intestinale e quanto intensamente suscita infiammazione. Il nuovo kit genetico rende ora possibile analizzare molte altre caratteristiche di questo microbo e dei suoi parenti. Per i non specialisti, l’idea fondamentale è che non tutti i membri di una specie batterica sono uguali: differenze genetiche sottili nelle strutture di superficie, come le capsule, possono ribaltare l’equilibrio tra un compagno utile e un innesco dannoso di malattia.
Citazione: Obana, N., Nakato, G., Nomura, N. et al. A genetic toolkit for the human gut bacterium Mediterraneibacter gnavus identifies capsular polysaccharides as a competitive colonization factor. Nat Commun 17, 3855 (2026). https://doi.org/10.1038/s41467-026-69022-x
Parole chiave: microbioma intestinale, Mediterraneibacter gnavus, capsula batterica, malattia infiammatoria intestinale, genetica CRISPR