Clear Sky Science · es
Un conjunto de herramientas genéticas para la bacteria intestinal humana Mediterraneibacter gnavus identifica a los polisacáridos capsulares como un factor competitivo de colonización
Por qué importa el “abrigo” de un microbio intestinal
Nuestros intestinos albergan trillones de microbios que pueden beneficiarnos o perjudicarnos. Un habitante común, la bacteria Mediterraneibacter gnavus, suele encontrarse en mayor abundancia en personas con enfermedades inflamatorias intestinales como la enfermedad de Crohn. Sin embargo, no todas las cepas de esta especie se comportan igual. Este estudio plantea una pregunta simple pero importante: ¿qué genes hacen que algunas cepas de M. gnavus sean mejores para vivir en el intestino, y cómo influye eso en la inflamación?
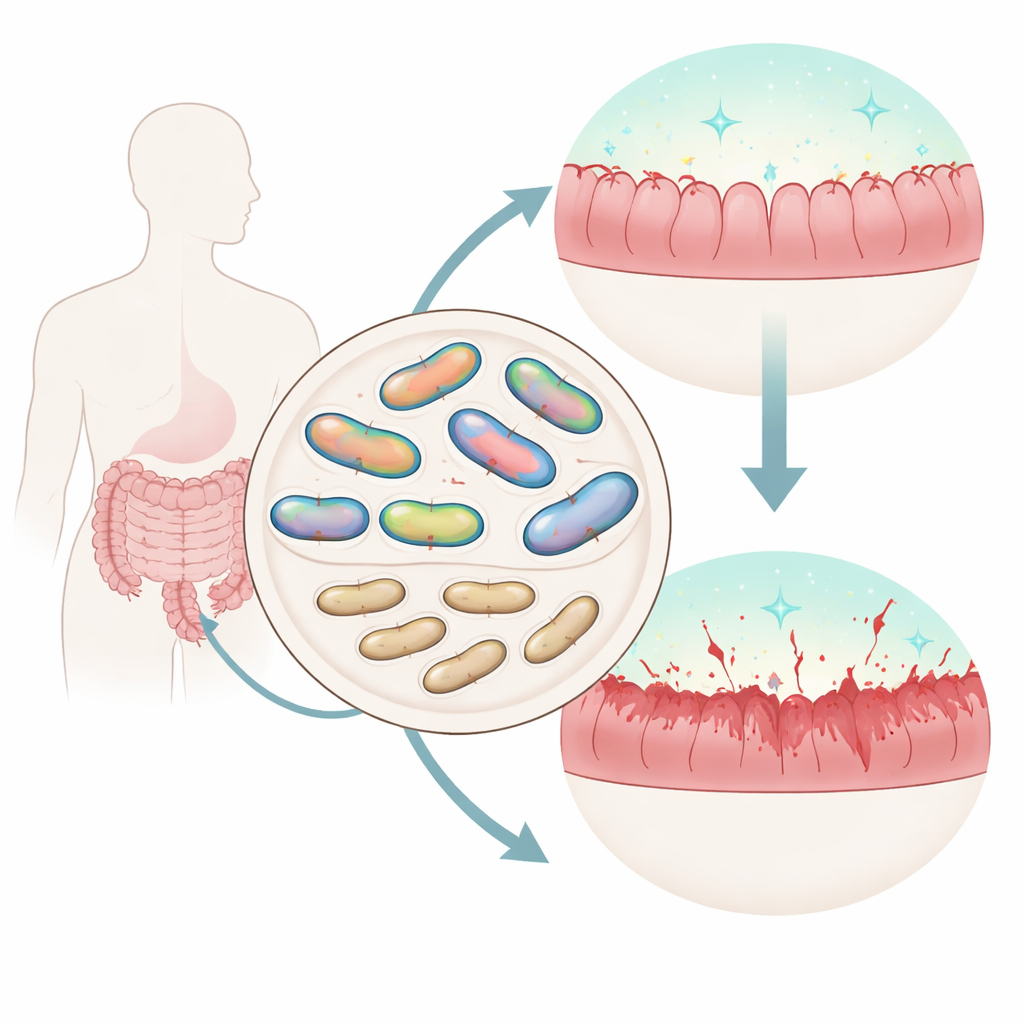
Construyendo una caja de herramientas para editar un microbio difícil
Muchas bacterias intestinales son difíciles de manipular genéticamente, lo que ha ralentizado los esfuerzos por entender la función de genes individuales. Los investigadores primero resolvieron este obstáculo técnico para M. gnavus. Crearon plásmidos centinela que pueden mover ADN entre E. coli y M. gnavus, junto con interruptores para activar genes solo cuando se necesite y un conjunto de etiquetas fluorescentes brillantes para rastrear las células bacterianas. También adaptaron dos sistemas para modificar el genoma de forma permanente: un método de inserción de ADN móvil y un enfoque basado en CRISPR/Cas9. En conjunto, estas herramientas les permitieron eliminar o interrumpir genes específicos, marcar cepas con color y comprobar los efectos tanto en placas de laboratorio como en ratones.
Localizando genes que moldean la superficie bacteriana
Con esta caja de herramientas, el equipo se centró en genes llamados sortasas, que actúan como grapadoras moleculares que fijan proteínas y azúcares a la pared celular bacteriana. M. gnavus posee ocho genes sortasa predichos. Al desactivar la mayoría de ellos uno por uno, los científicos demostraron que una enzima, SrtB3, es esencial para anclar potentes proteínas que activan el sistema inmune —llamadas superantígenos— a la superficie celular. Cuando se perdió SrtB3, estas proteínas dejaron de estar fijadas; en su lugar, se filtraron al medio circundante y la unión de anticuerpos en la superficie celular cayó bruscamente. Esto confirmó que tipos individuales de sortasa se especializan en manejar conjuntos distintos de moléculas de superficie.
Una cápsula azucarada que potencia la colonización intestinal
Los hallazgos más llamativos se centraron en otra sortasa, SrtB4. Bajo el microscopio, las células normales de M. gnavus parecen rodeadas por un pálido “halo”: una cápsula hecha de azúcares complejos que forma un recubrimiento blando alrededor de cada bacteria. Cuando el gen srtB4 se desactivó, ese halo desapareció. Tinciones químicas y microscopía electrónica confirmaron una pérdida importante de polisacárido capsular, y las células se aglomeraron fuertemente en lugar de formar pellets sueltos. Al mirar junto a srtB4 en el cromosoma, los investigadores descubrieron un racimo de genes predichos para construir y unir esta cápsula. La interrupción de varios de estos genes vecinos produjo el mismo aspecto sin cápsula, vinculando todo el conjunto a la fabricación de la cápsula.
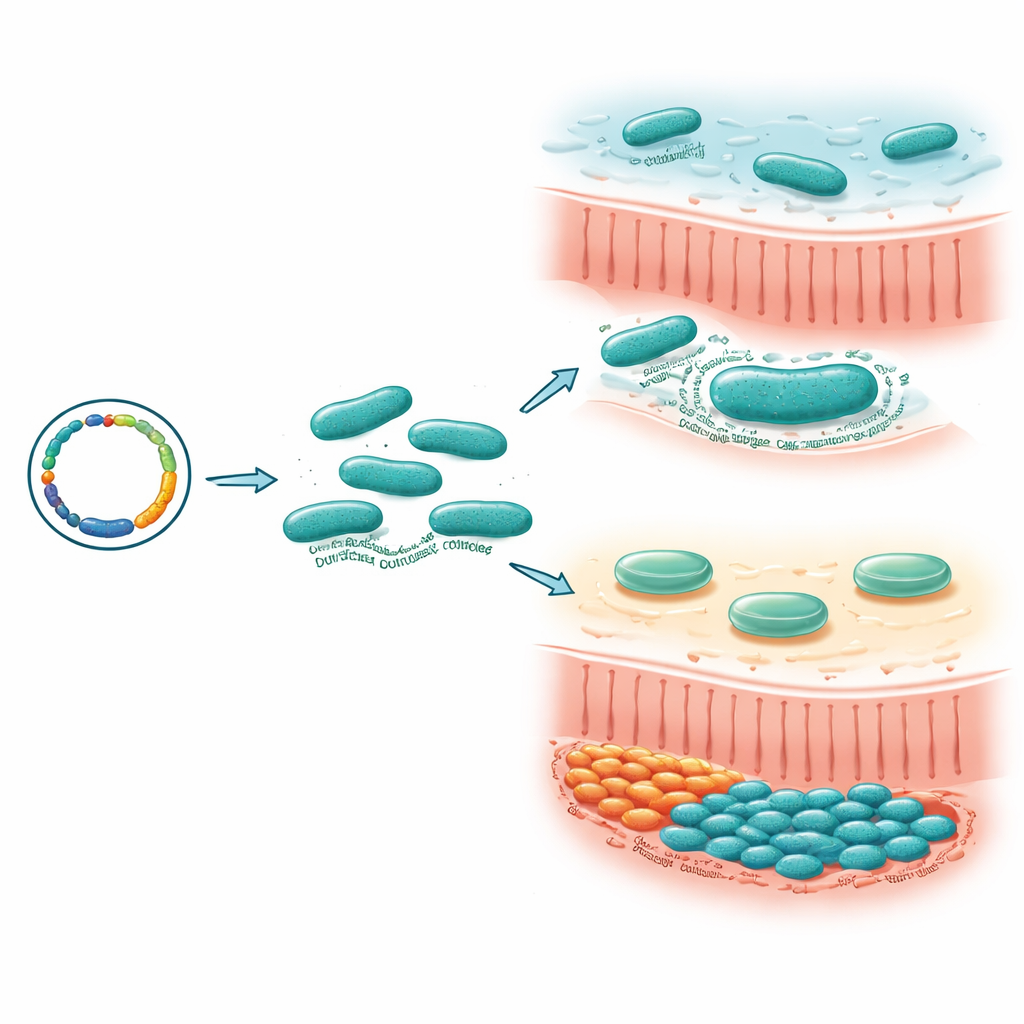
De la competencia en el intestino de ratón a la inflamación
Para probar por qué importa la cápsula, el equipo enfrentó cepas normales y mutantes entre sí dentro de ratones libres de gérmenes. Cuando las cepas carentes de cápsula se mezclaron con sus contrapartes encapsuladas y se administraron a los animales, los mutantes perdieron terreno rápidamente y casi desaparecieron del intestino, aunque crecían bien en cultivo de laboratorio. Esto mostró que la cápsula otorga a M. gnavus una marcada ventaja competitiva durante la colonización intestinal real. Pero la historia no terminó con la colonización. En cultivo celular, las cepas sin cápsula desencadenaron niveles mucho más altos de señales inflamatorias por parte de células inmunitarias de ratón que la cepa encapsulada. En un modelo murino de colitis inducida químicamente, los animales colonizados con el mutante sin cápsula sufrieron mayor pérdida de peso y puntuaciones de enfermedad más severas, aunque el número total de bacterias fue similar.
Vínculos con la enfermedad humana y posibles implicaciones
Finalmente, los autores compararon muchos genomas completos de cepas de M. gnavus aisladas de personas. Encontraron que el racimo de genes relacionado con la cápsula que contiene srtB4 estaba presente con mucha más frecuencia en cepas de individuos sanos que en cepas de pacientes con enfermedad de Crohn. Otras cepas que carecían de este racimo tampoco fabricaron una cápsula visible en el laboratorio. Aunque se necesita un muestreo más amplio, este patrón sugiere que las cepas portadoras de cápsula pueden ser mejores residentes a largo plazo que provocan menos inflamación, mientras que las cepas “desnudas” sin cápsula podrían dañar más el revestimiento intestinal.
Mensaje clave para la salud intestinal
Este trabajo muestra que un único bloque de genes que controla un recubrimiento exterior azucarado puede determinar si M. gnavus gana la batalla por colonizar el intestino y cuánto provoca inflamación. La nueva caja de herramientas genética ahora hace posible diseccionar muchas otras características de este microbio y sus parientes. Para los no especialistas, la idea clave es que no todos los miembros de una especie bacteriana son iguales: diferencias genéticas sutiles en estructuras superficiales, como las cápsulas, pueden inclinar la balanza entre un compañero benigno y un desencadenante dañino de enfermedad.
Cita: Obana, N., Nakato, G., Nomura, N. et al. A genetic toolkit for the human gut bacterium Mediterraneibacter gnavus identifies capsular polysaccharides as a competitive colonization factor. Nat Commun 17, 3855 (2026). https://doi.org/10.1038/s41467-026-69022-x
Palabras clave: microbioma intestinal, Mediterraneibacter gnavus, cápsula bacteriana, enfermedad inflamatoria intestinal, genética CRISPR