Clear Sky Science · pt
Produção da proteína recombinante de seda de aranha MaSp2 usando a bactéria fotossintética marinha não‑sulfurada Rhodovulum sulfidophilum em condições autotróficas
Transformando Luz do Sol e Água do Mar em Fios Resistentes
Imagine fabricar “seda de aranha” de alto desempenho sem criar aranhas, usando apenas luz, água do mar e gases do ar. Este estudo explora como uma bactéria marinha pode ser convertida em uma pequena fábrica movida a energia solar que produz os blocos de construção da seda de aranha enquanto depende de dióxido de carbono e nitrogênio da atmosfera. O trabalho aponta para novas formas de produzir materiais avançados com muito menos dependência de terras agrícolas, água doce e insumos de origem fóssil.
Um Pequeno Trabalhador do Mar
Os pesquisadores trabalham com um micro-organismo chamado Rhodovulum sulfidophilum, uma bactéria púrpura que vive em água do mar e captura energia da luz. Ao contrário das plantas, ela não libera oxigênio, mas realiza uma forma de fotossíntese. Também pode capturar gás nitrogênio do ar, transformando‑o nas moléculas ricas em nitrogênio de que a vida precisa. Como prospera em água salgada e pode usar substâncias inorgânicas simples, essa bactéria é uma plataforma promissora para produzir produtos úteis sem competir com a agricultura por água doce ou terras férteis.
Por que a Seda de Aranha É Tão Atraente
A seda de aranha fascina cientistas e engenheiros porque é simultaneamente muito resistente e extraordinariamente flexível. A seda de sustentação usada pelas aranhas em suas teias é construída a partir de proteínas especiais chamadas spidroínas. Neste estudo, o foco é uma dessas proteínas, MaSp2. Na natureza, as aranhas dissolvem essas proteínas em alta concentração e então as fiandeiam em fibras com uma estrutura interna complexa. Como aranhas não podem ser facilmente criadas em escala — tendem a se devorar — os pesquisadores geralmente recorrem a micróbios modificados, como leveduras ou bactérias de laboratório, para produzir proteínas de seda. No entanto, esses sistemas tipicamente dependem de meios ricos em açúcares e nitrogênio, o que limita sua sustentabilidade.
Construindo uma Oficina de Seda Movida a Sol
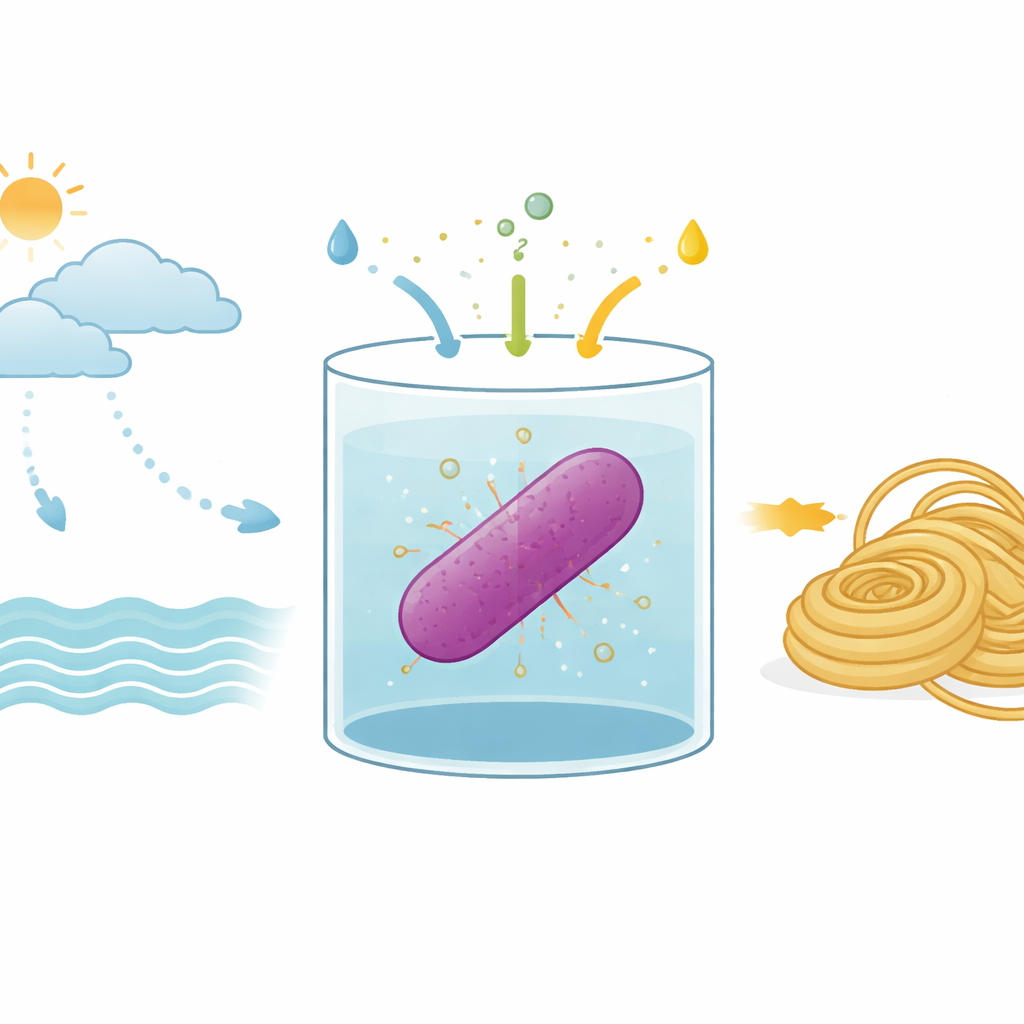
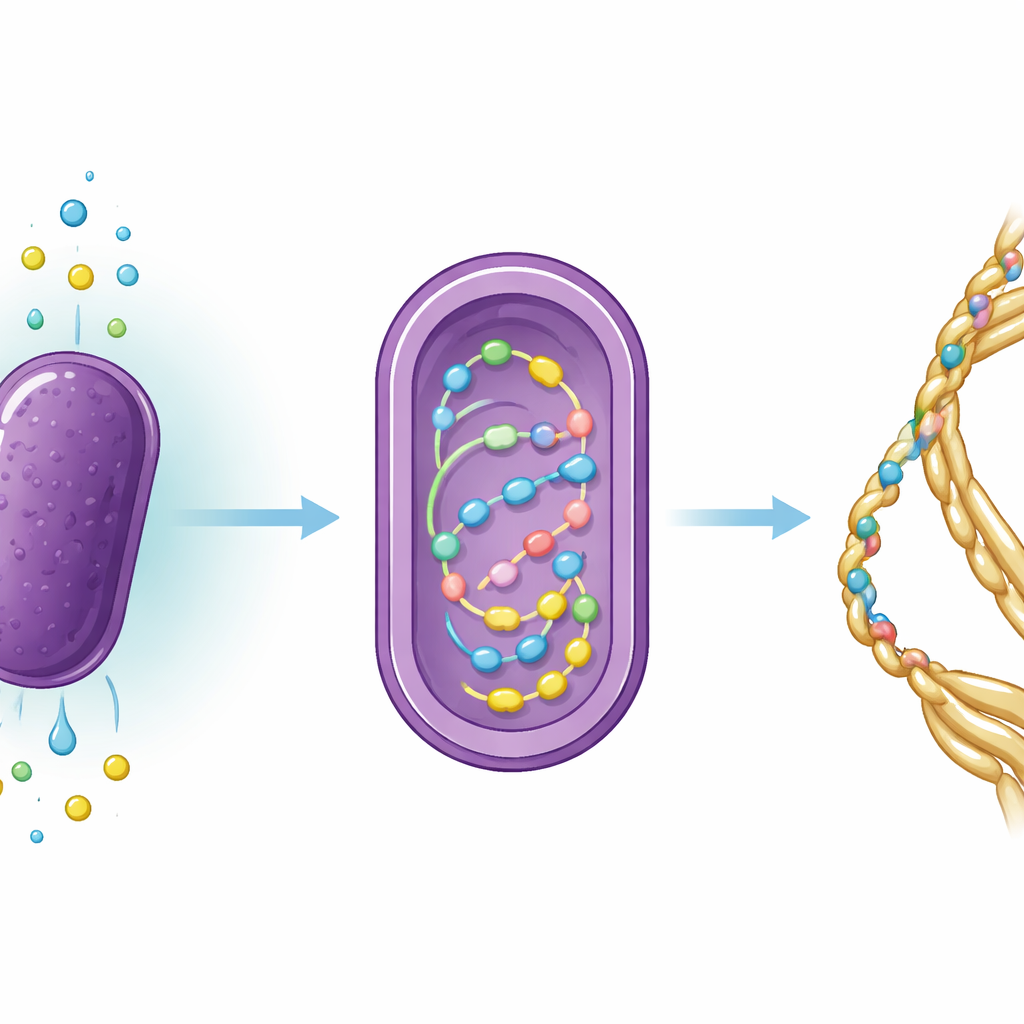
A equipe redesenhou R. sulfidophilum para que carregue um anel de DNA codificando a proteína de seda MaSp2. Em seguida, estabeleceram condições de crescimento que forçam as bactérias a depender quase inteiramente de ingredientes inorgânicos: dióxido de carbono como fonte de carbono, gás nitrogênio como fonte de nitrogênio e um composto de enxofre reduzido, tiossulfato de sódio, como doador de elétrons que ajuda a impulsionar reações semelhantes à fotossíntese. Em um vaso de 10 litros preenchido com água do mar artificial, borbulharam dióxido de carbono e nitrogênio, controlaram cuidadosamente o pH para que o dióxido de carbono se dissolvesse e iluminaram a cultura com luz infravermelha distante ajustada ao maquinário de captação de luz da bactéria. Quando adicionaram tiossulfato, o crescimento celular aumentou marcadamente em comparação com tentativas anteriores que não receberam esse insumo de enxofre.
Medindo Crescimento e Produção de Seda
Ao longo de vários dias, os pesquisadores monitoraram a velocidade de multiplicação das bactérias e quanto carbono e nitrogênio passaram da água do mar para as células. Os microrganismos cresceram por cerca de quatro dias antes de se estabilizarem, e análises químicas mostraram que eles absorveram constantemente tanto carbono quanto nitrogênio. A proporção desses elementos dentro das células sugeriu que o nitrogênio estava relativamente escasso, indicando que a etapa energeticamente cara de fixação do nitrogênio gasoso limitava a produtividade global. A equipe então quebrou as células e usou um método de purificação por ligação a metais para isolar a proteína MaSp2 recombinante. Embora as bactérias tenham produzido apenas quantidades de microgramas de proteína de seda solúvel por litro — quantidades ínfimas segundo padrões industriais — o trabalho provou que condições de cultivo totalmente inorgânicas e baseadas em água do mar podem sustentar tanto o crescimento quanto a produção de seda recombinante.
Caminhos para Melhorar o Desempenho
Além da prova de conceito imediata, os autores descrevem várias alavancas que poderiam aumentar os rendimentos. Melhorar a fotossíntese, por exemplo ajustando a intensidade da luz ou o equilíbrio de nutrientes, poderia gerar mais da energia necessária para a fixação de nitrogênio e a síntese de aminoácidos. Ajustar finamente o controle genético da proteína de seda — por exemplo, ativando a expressão apenas depois que as células atingirem alta densidade, ou otimizando a sequência para a maquinaria de tradução da bactéria — também poderia reduzir o estresse sobre as células e aumentar a produção. A capacidade da bactéria de usar vários compostos de enxofre reduzidos sugere que fluxos de resíduos industriais contendo enxofre poderiam um dia alimentar tais cultivos, fechando ainda mais o ciclo de reciclagem de recursos. Ao mesmo tempo, os autores observam que o uso em larga escala de bactérias marinhas geneticamente modificadas exigiria medidas de segurança rigorosas para evitar seu escape no ambiente.
O Que Isso Significa para Materiais Futuros
Em termos simples, este estudo mostra que é possível fazer uma bactéria marinha produzir a proteína da seda de aranha enquanto vive quase inteiramente de ar, luz, água do mar e uma fonte inorgânica de enxofre. Os rendimentos atuais são baixos, mas a via básica funciona, e os autores identificam passos claros para tornar o processo mais eficiente. Se aperfeiçoado, esse tipo de sistema de produção movido a energia solar e baseado em água do mar poderia oferecer uma forma de fabricar materiais proteicos fortes e flexíveis com pegada muito menor, ajudando a desvincular materiais avançados da agricultura tradicional e dos recursos fósseis.
Citação: Suzuki, M., Numata, K. Production of the recombinant spider silk MaSp2 protein using the marine purple photosynthetic nonsulfur bacterium Rhodovulum sulfidophilum under autotrophic conditions. NPG Asia Mater 18, 13 (2026). https://doi.org/10.1038/s41427-026-00638-7
Palavras-chave: seda de aranha, bactérias fotossintéticas, biomanufatura sustentável, cultivo em água do mar, proteínas recombinantes