Clear Sky Science · it
Produzione della proteina ricombinante di seta del ragno MaSp2 usando il batterio fotosintetico marino non solforoso Rhodovulum sulfidophilum in condizioni autotrofe
Trasformare la luce solare e l’acqua di mare in fili resistenti
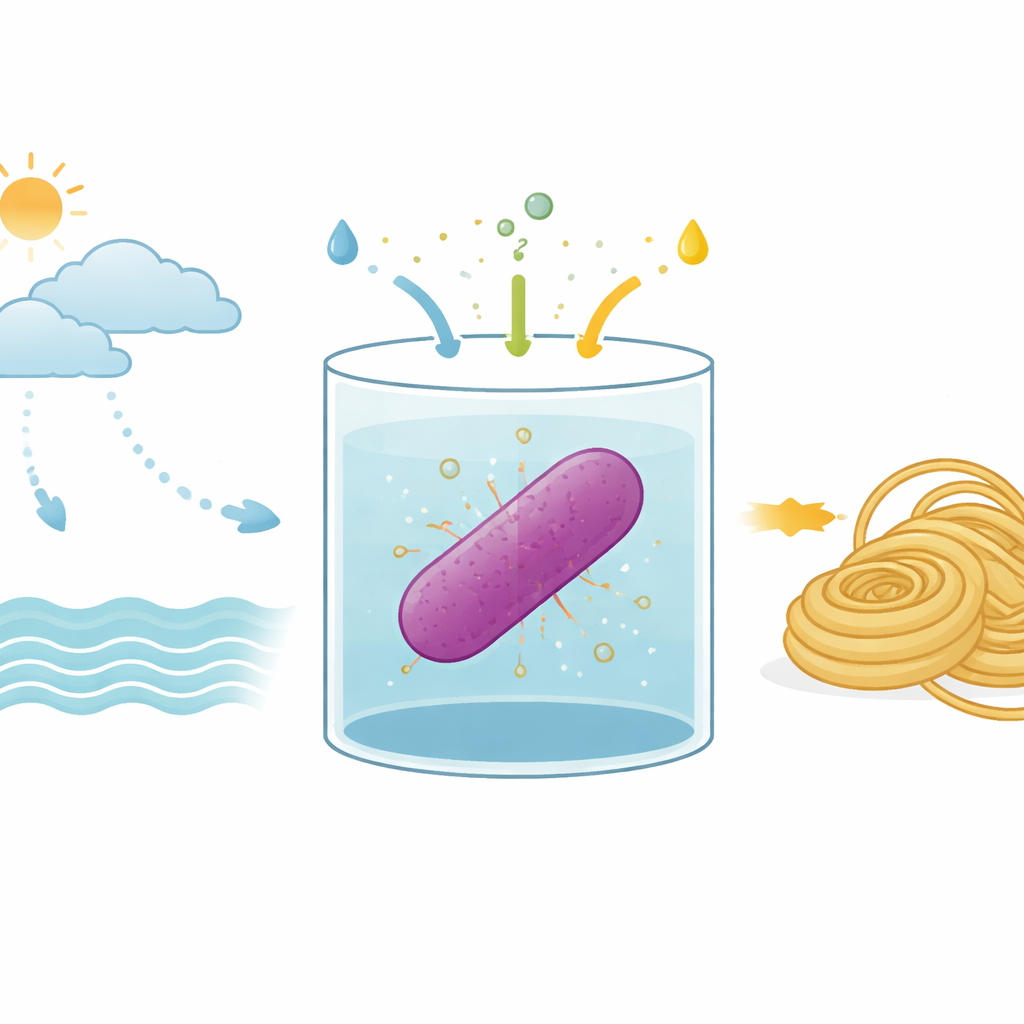
Immaginate di produrre una «seta di ragno» ad alte prestazioni senza allevare ragni, usando solo luce, acqua di mare e gas dell’atmosfera. Questo studio esplora come un batterio marino possa essere convertito in una piccola fabbrica solare che sintetizza i mattoni della seta di ragno avvalendosi di anidride carbonica e azoto atmosferico. Il lavoro indica nuove strade per produrre materiali avanzati con molto meno dipendenza da terreni agricoli, acqua dolce e ingredienti di origine fossile.
Un piccolo operaio dal mare
I ricercatori lavorano con un microbo chiamato Rhodovulum sulfidophilum, un batterio viola che vive in acqua di mare e cattura energia dalla luce. A differenza delle piante, non rilascia ossigeno ma esegue comunque una forma di fotosintesi. Può anche fissare l’azoto gassoso dall’aria, trasformandolo nelle molecole ricche di azoto necessarie alla vita. Poiché prospera in acqua salata e può usare sostanze inorganiche semplici, questo batterio è una piattaforma promettente per produrre composti utili senza competere con l’agricoltura per acqua dolce o terreni fertili.
Perché la seta di ragno è così interessante
La seta di ragno ha da tempo affascinato scienziati e ingegneri perché è al contempo molto resistente e straordinariamente flessibile. La dragline silk usata dai ragni nelle loro ragnatele è costituita da proteine speciali chiamate spidroine. In questo studio l’attenzione è su una di queste proteine, MaSp2. In natura i ragni dissolvono queste proteine ad alta concentrazione e poi le filano in fibre con una struttura interna complessa. Poiché i ragni non sono facilmente allevabili—tendono a mangiarsi tra loro—i ricercatori si rivolgono in genere a microbi ingegnerizzati come lieviti o batteri da laboratorio per produrre proteine della seta. Tuttavia, quei sistemi dipendono tipicamente da terreni ricchi di zuccheri e azoto, il che ne limita la sostenibilità.
Costruire una officina della seta guidata dal sole
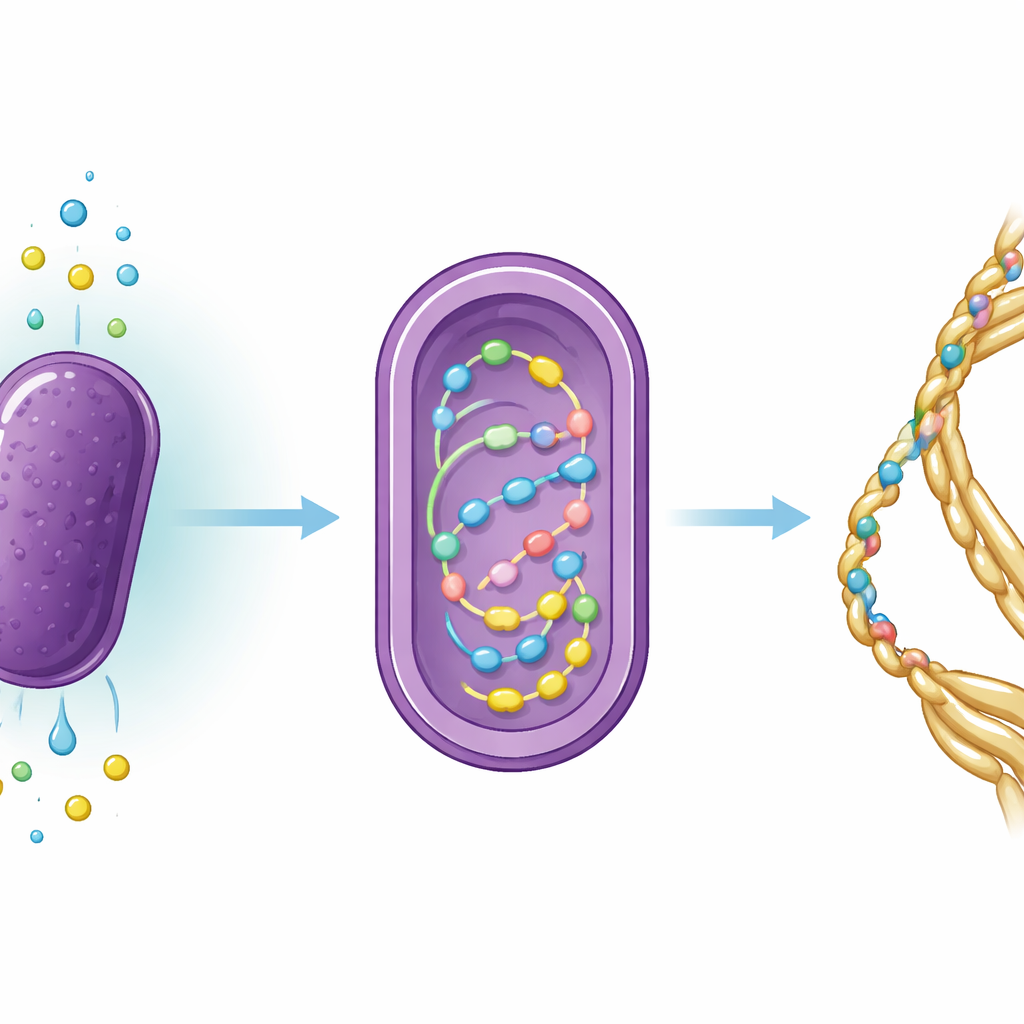
Il team ha riprogettato R. sulfidophilum in modo che porti un anello di DNA che codifica per la proteina di seta MaSp2. Poi hanno impostato condizioni di crescita che costringono i batteri a fare quasi esclusivo uso di ingredienti inorganici: anidride carbonica come fonte di carbonio, azoto gassoso come fonte di azoto e un composto solforato ridotto, il tiosolfato di sodio, come donatore di elettroni che aiuta a guidare reazioni simili alla fotosintesi. In un recipiente da 10 litri riempito con acqua di mare artificiale, hanno fatto scorrere anidride carbonica e azoto, controllato attentamente il pH in modo che l’anidride carbonica si dissolvesse, e illuminato la coltura con luce rosso–lontana sintonizzata sul apparato di raccolta della luce del batterio. Quando hanno aggiunto tiosolfato, la crescita cellulare è aumentata notevolmente rispetto a tentativi precedenti privi di questo apporto di zolfo.
Misurare la crescita e la produzione di seta
Per diversi giorni i ricercatori hanno monitorato la velocità di moltiplicazione dei batteri e la quantità di carbonio e azoto trasferiti dall’acqua di mare alle cellule. I microrganismi sono cresciuti per circa quattro giorni prima di stabilizzarsi, e le analisi chimiche hanno mostrato che hanno continuamente assorbito sia carbonio sia azoto. Il rapporto tra questi elementi all’interno delle cellule suggeriva che l’azoto fosse relativamente scarso, facendo intuire che il passo ad alto dispendio energetico della fissazione dell’azoto gassoso stesse limitando la produttività complessiva. Il team ha poi lisi le cellule e usato un metodo di purificazione basato sul legame ai metalli per isolare la proteina MaSp2 ingegnerizzata. Sebbene i batteri abbiano prodotto solo quantità di microgrammi di proteina della seta solubile per litro—quantità piccolissime rispetto agli standard industriali—il lavoro ha dimostrato che condizioni di coltura completamente inorganiche e basate su acqua di mare possono sostenere sia la crescita sia la produzione ricombinante di seta.
Strade per migliorare le prestazioni
Oltre alla prova di principio immediata, gli autori descrivono diversi leve che potrebbero aumentare le rese. Migliorare la fotosintesi, ad esempio regolando l’intensità luminosa o l’equilibrio dei nutrienti, potrebbe generare più energia necessaria per la fissazione dell’azoto e la sintesi degli amminoacidi. Raffinare il controllo genetico della proteina di seta—per esempio attivando l’espressione solo dopo che le cellule hanno raggiunto una certa densità, o ottimizzando la sequenza per la macchina di traduzione del batterio—potrebbe anche ridurre lo stress sulle cellule e aumentare la produzione. La capacità del batterio di utilizzare vari composti solforati ridotti suggerisce che in futuro flussi di scarto industriali contenenti zolfo potrebbero alimentare tali colture, chiudendo ulteriormente il ciclo del riciclo delle risorse. Allo stesso tempo, gli autori notano che l’uso su larga scala di batteri marini geneticamente modificati richiederebbe rigorose misure di sicurezza per prevenire fughe nell’ambiente.
Cosa significa per i materiali del futuro
In termini semplici, questo studio mostra che è possibile far produrre a un batterio marino la proteina della seta di ragno mentre vive praticamente solo di aria, luce, acqua di mare e una fonte inorganica di zolfo. Le rese attuali sono basse, ma il percorso di base funziona e gli autori identificano passi chiari per rendere il processo più efficiente. Se migliorato, questo tipo di sistema di produzione solare e basato su acqua di mare potrebbe offrire un modo per fabbricare materiali proteici resistenti e flessibili con un impatto molto inferiore, contribuendo a scollegare i materiali avanzati dall’agricoltura tradizionale e dalle risorse fossili.
Citazione: Suzuki, M., Numata, K. Production of the recombinant spider silk MaSp2 protein using the marine purple photosynthetic nonsulfur bacterium Rhodovulum sulfidophilum under autotrophic conditions. NPG Asia Mater 18, 13 (2026). https://doi.org/10.1038/s41427-026-00638-7
Parole chiave: seta di ragno, batteri fotosintetici, bioproduzione sostenibile, coltivazione in acqua di mare, proteine ricombinanti