Clear Sky Science · es
Producción de la proteína recombinante de seda de araña MaSp2 utilizando la bacteria fotosintética marina no sulfurosa Rhodovulum sulfidophilum en condiciones autótrofas
Convertir la luz solar y el agua de mar en hilos resistentes
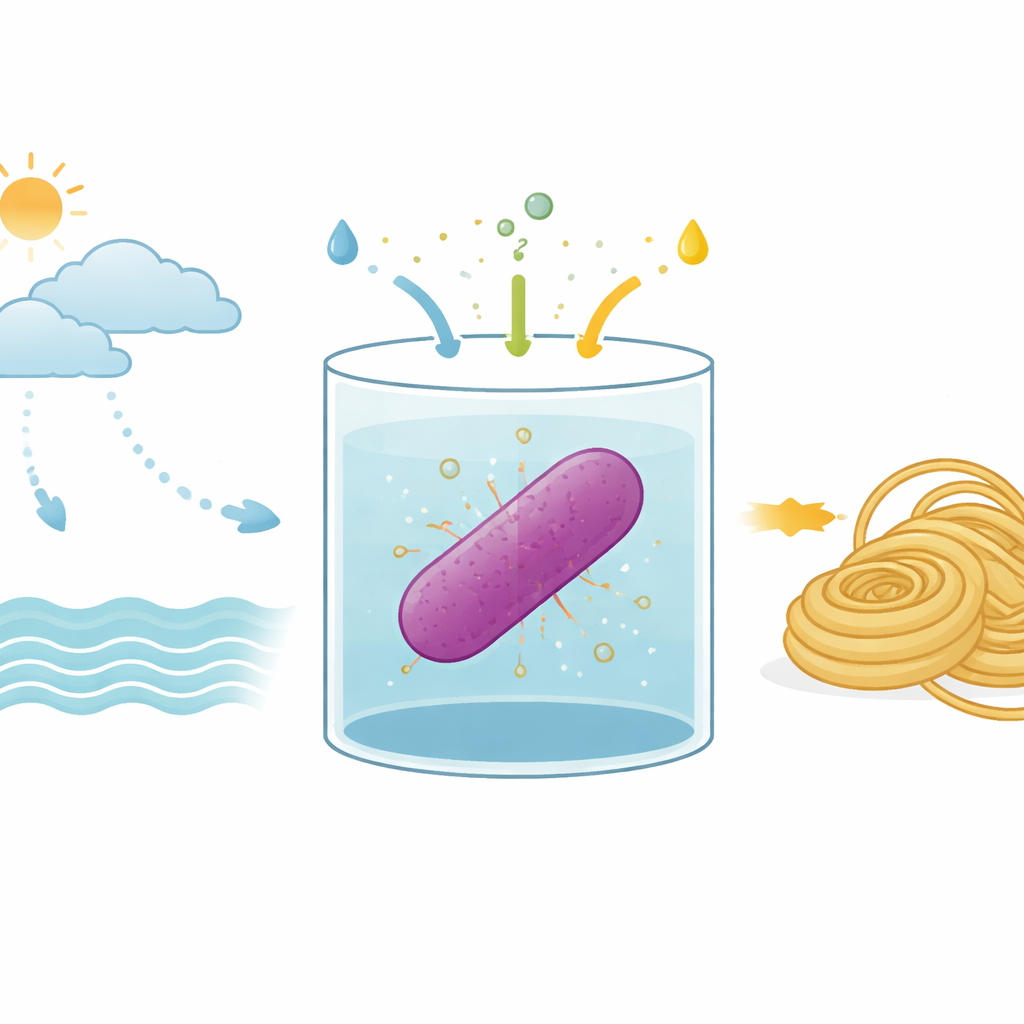
Imagine producir “seda de araña” de alto rendimiento sin criar arañas, usando solo luz, agua de mar y gases de la atmósfera. Este estudio explora cómo una bacteria marina puede transformarse en una pequeña fábrica solar que sintetiza los bloques constructores de la seda de araña apoyándose en dióxido de carbono y nitrógeno atmosféricos. El trabajo apunta a nuevas vías para producir materiales avanzados con mucha menos dependencia de tierras agrícolas, agua dulce e insumos fósiles.
Un pequeño obrero del mar
Los investigadores trabajan con un microbio llamado Rhodovulum sulfidophilum, una bacteria púrpura que vive en agua de mar y aprovecha la energía de la luz. A diferencia de las plantas, no libera oxígeno pero realiza una forma de fotosíntesis. También puede captar gas nitrógeno del aire y convertirlo en las moléculas ricas en nitrógeno que necesita la vida. Debido a que prospera en agua salada y puede utilizar sustancias inorgánicas simples, esta bacteria es una plataforma prometedora para fabricar productos útiles sin competir con la agricultura por agua dulce o tierras fértiles.
Por qué la seda de araña resulta tan atractiva
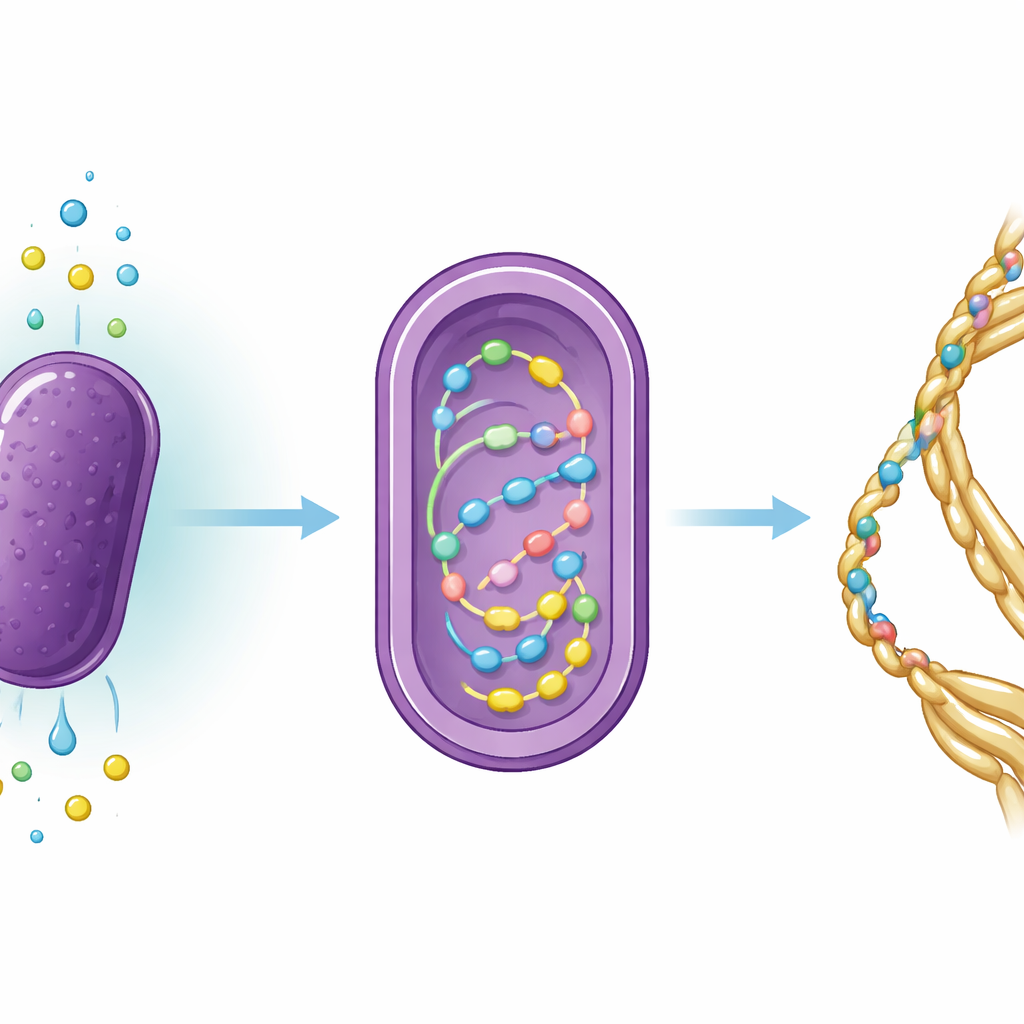
La seda de araña ha fascinado durante mucho tiempo a científicos e ingenieros porque combina gran resistencia con notable flexibilidad. La seda de arrastre que usan las arañas en sus telas está compuesta por proteínas especiales llamadas espidrinas. En este estudio, el foco está en una de esas proteínas, MaSp2. En la naturaleza, las arañas disuelven estas proteínas a alta concentración y luego las hilvanan en fibras con una estructura interna compleja. Dado que las arañas no son fáciles de criar—tienen tendencia a comerse unas a otras—los investigadores suelen recurrir a microbios modificados como levaduras o bacterias de laboratorio para producir proteínas de seda. Sin embargo, esos sistemas normalmente dependen de medios ricos en azúcares y nitrógeno, lo que limita su sostenibilidad.
Construir un taller de seda impulsado por energía solar
El equipo rediseñó R. sulfidophilum para que lleve un anillo de ADN que codifica la proteína de seda MaSp2. Luego establecieron condiciones de cultivo que obligan a las bacterias a depender casi por completo de ingredientes inorgánicos: dióxido de carbono como fuente de carbono, gas nitrógeno como fuente de nitrógeno y un compuesto de azufre reducido, tiosulfato de sodio, como donador de electrones que ayuda a impulsar reacciones similares a la fotosíntesis. En un vaso de 10 litros lleno de agua de mar artificial, burbujearon dióxido de carbono y nitrógeno, controlaron cuidadosamente el pH para favorecer la disolución del dióxido de carbono e iluminaron el cultivo con luz rojo‑lejana ajustada a la maquinaria de captación de luz de la bacteria. Al añadir tiosulfato, el crecimiento celular aumentó notablemente en comparación con intentos previos que carecían de esta aportación de azufre.
Medir el crecimiento y la producción de seda
A lo largo de varios días, los investigadores monitorizaron la velocidad de multiplicación bacteriana y la cantidad de carbono y nitrógeno que se incorporaba desde el agua de mar a las células. Los microbios crecieron durante aproximadamente cuatro días antes de estabilizarse, y los análisis químicos mostraron una absorción sostenida de carbono y nitrógeno. La proporción de estos elementos dentro de las células sugirió que el nitrógeno estaba relativamente limitado, lo que indica que el paso energéticamente costoso de fijar el gas nitrógeno podría estar restringiendo la productividad global. El equipo luego lisó las células y utilizó un método de purificación basado en unión a metales para aislar la proteína MaSp2 recombinante. Aunque las bacterias produjeron solo cantidades de microgramos de proteína de seda soluble por litro—cantidades muy pequeñas según estándares industriales—el trabajo demostró que condiciones de cultivo totalmente inorgánicas y basadas en agua de mar pueden sostener tanto el crecimiento como la producción de seda recombinante.
Vías para mejorar el rendimiento
Más allá de la prueba de concepto inmediata, los autores describen varias palancas que podrían aumentar los rendimientos. Mejorar la fotosíntesis, por ejemplo ajustando la intensidad lumínica o el equilibrio de nutrientes, podría generar más de la energía necesaria para la fijación del nitrógeno y la síntesis de aminoácidos. Ajustar finamente el control genético de la proteína de seda—por ejemplo, activar la expresión solo después de que las células hayan alcanzado alta densidad, u optimizar la secuencia para la maquinaria de traducción de la bacteria—podría también reducir el estrés celular y aumentar la producción. La capacidad de la bacteria para utilizar diversos compuestos de azufre reducido sugiere que corrientes residuales industriales que contienen azufre podrían algún día alimentar tales cultivos, cerrando aún más el ciclo de reciclaje de recursos. Al mismo tiempo, los autores señalan que el uso a gran escala de bacterias marinas genéticamente modificadas requeriría medidas de seguridad estrictas para evitar su escape al medio ambiente.
Qué significa esto para los materiales del futuro
En términos sencillos, este estudio muestra que es posible inducir a una bacteria marina a producir la proteína de seda de araña viviendo casi exclusivamente de aire, luz, agua de mar y una fuente inorgánica de azufre. Los rendimientos actuales son bajos, pero la vía básica funciona y los autores identifican pasos claros para hacer el proceso más eficiente. Si se mejora, este tipo de sistema de producción impulsado por el sol y basado en agua de mar podría ofrecer una forma de fabricar materiales proteicos fuertes y flexibles con una huella mucho menor, ayudando a desvincular los materiales avanzados de la agricultura tradicional y de los recursos fósiles.
Cita: Suzuki, M., Numata, K. Production of the recombinant spider silk MaSp2 protein using the marine purple photosynthetic nonsulfur bacterium Rhodovulum sulfidophilum under autotrophic conditions. NPG Asia Mater 18, 13 (2026). https://doi.org/10.1038/s41427-026-00638-7
Palabras clave: seda de araña, bacterias fotosintéticas, bioproducción sostenible, cultivo en agua de mar, proteínas recombinantes