Clear Sky Science · de
Produktion des rekombinanten Spinnenseiden‑Proteins MaSp2 mit der marinen, violetten, photosynthetischen Nichtschwefel‑Bakterie Rhodovulum sulfidophilum unter autotrophen Bedingungen
Sonnenlicht und Meerwasser in starke Fasern verwandeln
Stellen Sie sich vor, man könnte hochleistungsfähige „Spinnenseide“ herstellen, ohne Spinnen zu züchten, und lediglich Licht, Meerwasser und Gase aus der Luft nutzen. Diese Studie untersucht, wie ein marines Bakterium in eine winzige, solarbetriebene Fabrik verwandelt werden kann, die die Bausteine der Spinnenseide produziert, während es sich auf Kohlendioxid und Stickstoff aus der Atmosphäre stützt. Die Arbeit weist auf neue Wege hin, fortschrittliche Materialien mit deutlich geringerem Bedarf an Ackerland, Süßwasser und fossilen Rohstoffen herzustellen.
Ein winziger Arbeiter aus dem Meer
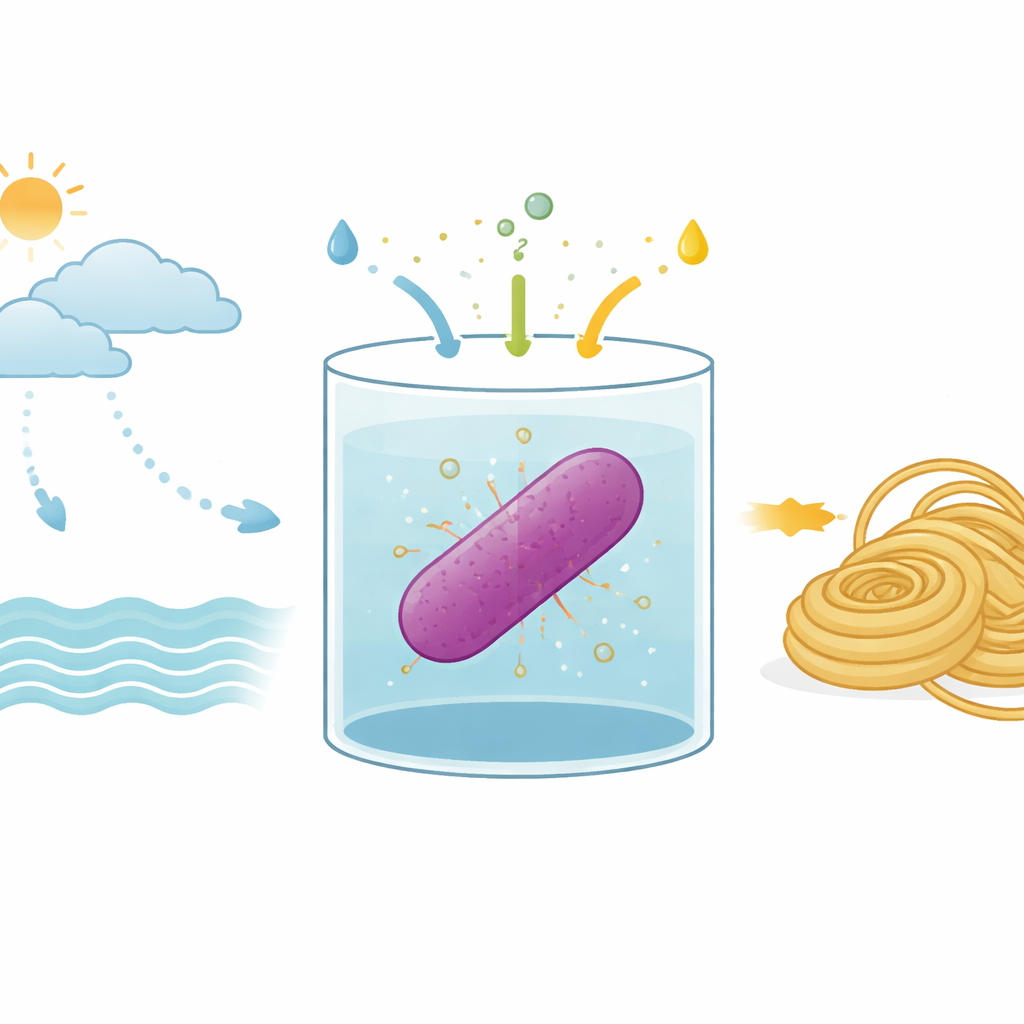
Die Forschenden arbeiten mit einem Mikroorganismus namens Rhodovulum sulfidophilum, einem violetten Bakterium, das im Meerwasser lebt und Energie aus Licht gewinnt. Im Gegensatz zu Pflanzen setzt es kein Sauerstoff frei, betreibt aber eine Form der Photosynthese. Es kann außerdem Stickstoffgas aus der Luft binden und in stickstoffreiche Moleküle umwandeln, die das Leben benötigt. Da es in salzhaltigem Wasser gedeiht und einfache anorganische Verbindungen nutzen kann, ist dieses Bakterium eine vielversprechende Plattform, um nützliche Produkte zu erzeugen, ohne mit der Landwirtschaft um Süßwasser oder fruchtbare Flächen zu konkurrieren.
Warum Spinnenseide so attraktiv ist
Spinnenseide fasziniert Wissenschaftlerinnen und Ingenieure seit langem, weil sie zugleich sehr stark und bemerkenswert elastisch ist. Die Zugfäden, die Spinnen in ihren Netzen verwenden, bestehen aus speziellen Proteinen, den Spidroinen. In dieser Studie liegt der Fokus auf einem solchen Protein, MaSp2. In der Natur lösen Spinnen diese Proteine in hoher Konzentration und spinnen sie dann zu Fasern mit komplexer innerer Struktur. Da Spinnen schwer zu züchten sind — sie neigen dazu, sich gegenseitig zu fressen — greifen Forschende üblicherweise auf gentechnisch veränderte Mikroben wie Hefen oder gängige Laborbakterien zurück, um Seidenproteine herzustellen. Diese Systeme sind jedoch meist auf zucker‑ und stickstoffreiche Nährmedien angewiesen, was ihre Nachhaltigkeit einschränkt.
Ein solarbetriebenes Seidenatelier aufbauen
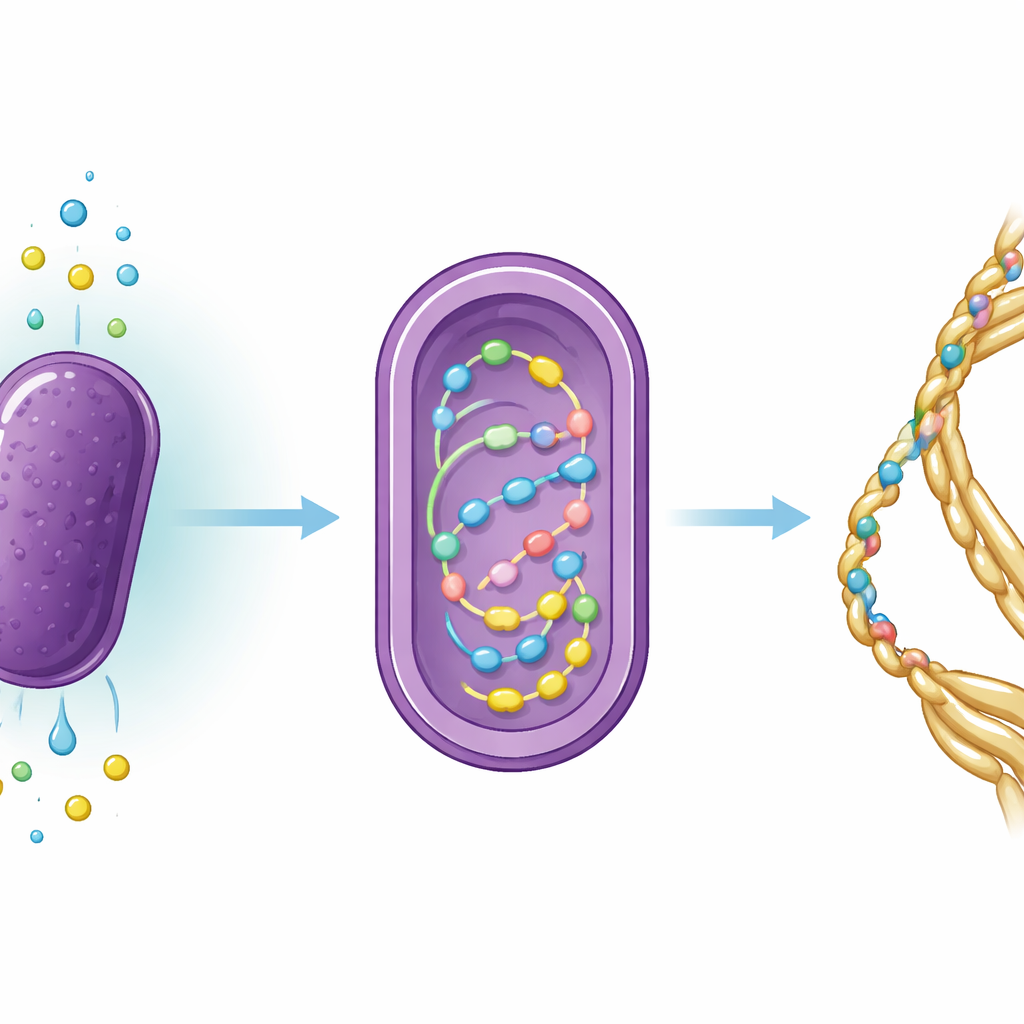
Das Team hat R. sulfidophilum so umgestaltet, dass es einen DNA‑Ring (Plasmid) trägt, der das MaSp2‑Spinnenseidenprotein codiert. Anschließend richteten sie Wachstumsbedingungen ein, die die Bakterien zwingen, sich nahezu ausschließlich von anorganischen Bestandteilen zu ernähren: Kohlendioxid als Kohlenstoffquelle, Stickstoffgas als Stickstoffquelle und eine reduzierte Schwefelverbindung, Natriumthiosulfat, als Elektronendonator, der die photosyntheseähnlichen Reaktionen antreibt. In einem 10‑Liter‑Gefäß mit künstlichem Meerwasser leiteten sie Kohlendioxid und Stickstoff ein, kontrollierten den pH‑Wert so, dass das Kohlendioxid sich löste, und bestrahlten die Kultur mit langwelligem rotem Licht, das auf die lichtabsorbierenden Systeme des Bakteriums abgestimmt war. Als sie Thiosulfat zusetzten, stieg das Zellwachstum deutlich im Vergleich zu früheren Versuchen ohne diesen Schwefel‑Input.
Wachstum und Seidenausstoß messen
Über mehrere Tage verfolgten die Forschenden, wie schnell sich die Bakterien vermehrten und wie viel Kohlenstoff und Stickstoff aus dem Meerwasser in die Zellen gelangte. Die Mikroben wuchsen etwa vier Tage lang, bevor das Wachstum abflachte, und chemische Analysen zeigten, dass sie beständig sowohl Kohlenstoff als auch Stickstoff aufnahmen. Das Verhältnis dieser Elemente in den Zellen deutete darauf hin, dass Stickstoff relativ knapp war, was darauf hindeutet, dass der energieaufwendige Schritt der Stickstofffixierung die Gesamtproduktivität begrenzte. Das Team brach anschließend die Zellen auf und isolierte das gentechnisch eingebrachte MaSp2‑Protein mittels eines metallbindenden Reinigungsverfahrens. Obwohl die Bakterien nur Mikrogramm‑Mengen löslichen Seidenproteins pro Liter produzierten — verschwindend geringe Mengen nach industriellen Maßstäben — zeigte die Arbeit, dass vollständig anorganische, meerwasserbasierte Kulturbedingungen sowohl Wachstum als auch rekombinante Seidenproduktion ermöglichen können.
Wege zu besserer Leistung
Über den unmittelbaren Machbarkeitsnachweis hinaus skizzieren die Autorinnen und Autoren mehrere Stellschrauben, mit denen die Ausbeuten gesteigert werden könnten. Eine Verbesserung der Photosynthese — etwa durch Anpassung der Lichtintensität oder des Nährstoffverhältnisses — könnte mehr Energie für Stickstofffixierung und Aminosäuresynthese bereitstellen. Eine Feinabstimmung der genetischen Kontrolle des Seidenproteins — zum Beispiel die Aktivierung der Expression erst nach Erreichen hoher Zelldichten oder die Optimierung der Sequenz für die Translationsmaschinerie des Bakteriums — könnte die Belastung der Zellen reduzieren und den Ertrag steigern. Die Fähigkeit des Bakteriums, verschiedene reduzierte Schwefelverbindungen zu nutzen, legt nahe, dass industrielle Abwässer mit Schwefelgehalt künftig solche Kulturen ernähren könnten, was den Ressourcen‑Kreislauf weiter schließen würde. Gleichzeitig weisen die Autorinnen und Autoren darauf hin, dass ein großflächiger Einsatz gentechnisch veränderter mariner Bakterien strenge Sicherheitsmaßnahmen erfordern würde, um ein Entweichen in die Umwelt zu verhindern.
Was das für zukünftige Materialien bedeutet
Einfach ausgedrückt zeigt diese Studie, dass es möglich ist, ein marines Bakterium dazu zu bringen, Spinnenseidenprotein herzustellen, während es nahezu ausschließlich von Luft, Licht, Meerwasser und einer anorganischen Schwefelquelle lebt. Die aktuellen Ausbeuten sind gering, doch der grundlegende Weg funktioniert, und die Autorinnen und Autoren benennen klare Schritte, um das Verfahren effizienter zu machen. Wenn Verbesserungen gelingen, könnte dieses solarbetriebene, meerwasserbasierte Produktionssystem eine Möglichkeit bieten, starke, flexible Proteinmaterialien mit deutlich kleinerer ökologischer Bilanz herzustellen und so fortschrittliche Materialien von traditioneller Landwirtschaft und fossilen Ressourcen zu entkoppeln.
Zitation: Suzuki, M., Numata, K. Production of the recombinant spider silk MaSp2 protein using the marine purple photosynthetic nonsulfur bacterium Rhodovulum sulfidophilum under autotrophic conditions. NPG Asia Mater 18, 13 (2026). https://doi.org/10.1038/s41427-026-00638-7
Schlüsselwörter: Spinnenseide, photosynthetische Bakterien, nachhaltige Bioproduktion, Meerwasser‑Kultivierung, rekombinante Proteine